Влияние одноименного иона на степень диссоциации слабых кислот и оснований

Если к раствору слабой кислоты прибавить ее соль, то степень диссоциации кислоты понижается, следовательно, концентрация водородных ионов уменьшается. Диссоциация слабой кислоты подавляется также в присутствии сильной кислоты: в этом случае уменьшается концентрация ее анионов. Аналогичным образом можно рассчитать концентрацию ОН- и б в растворах слабых оснований (ВОН) в присутствии их солей (ВХ… Читать ещё >
Влияние одноименного иона на степень диссоциации слабых кислот и оснований (реферат, курсовая, диплом, контрольная)
Если к раствору слабой кислоты прибавить ее соль, то степень диссоциации кислоты понижается, следовательно, концентрация водородных ионов уменьшается. Диссоциация слабой кислоты подавляется также в присутствии сильной кислоты: в этом случае уменьшается концентрация ее анионов.
Аналогичное явление имеет место в растворах слабых оснований при добавлении сильных электролитов, содержащих одноименный ион.
В растворе слабой кислоты НА в присутствии ее соли МА равновесие реакции (1.1) смещается в сторону образования недиссоциированных молекул НА. Концентрации ионов, образующихся при диссоциации кислоты, будут в данном случае очень малы. Поэтому концентрацию недиссоциированных молекул кислоты можно считать равной общей концентрации кислоты СНА, а концентрация анионов А- может быть принята равной концентрации соли (СА-), которая в растворе практически полностью диссоциирована.
[НА] = СНА,.
[А-] = СА-.
Подставив эти значения в уравнение (1.20), найдем [Н+] и б.
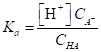
(1.87).

(1.88).
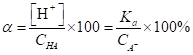
(1.89).
Аналогичным образом можно рассчитать концентрацию ОН- и б в растворах слабых оснований (ВОН) в присутствии их солей (ВХ). В этом случае концентрацию ВОН принимают равной общей концентрации основания Свон, а концентрацию катионов В+ — концентрации соли (Св+).
[ВОН] = СВОН; [В+] = СВ+.
Подставив эти значения в выражение для константы диссоциации слабого основания, получим.
Отсюда.
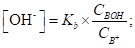
(1.91).
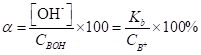
(1.92).
Рассмотрим равновесие в растворе слабой одноосновной кислоты при заданном рН. Общая концентрация кислоты складывается из концентрации недиссоциированных молекул НА и ионов А-.
Сна = [НА] + [А-]. (1.93).
Из уравнения (1.20) следует.
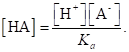
(1.94).
Подставив это значение в уравнение (1.93), получим.
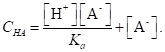
(1.95).
Решая это уравнение относительно [А-], найдем.
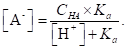
(1.96).
Уравнение (1.96) позволяет рассчитать концентрацию анионов слабой кислоты при заданной концентрации водородных ионов.
При избытке сильной кислоты, когда концентрация значительно превышает значение Ка уравнение (1.96) принимает вид.
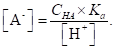
(1.97).
В растворах многоосновных кислот при данном рН наряду с недиссоциированными молекулами кислоты HnA могут присутствовать ионы различного состава (Нn-1А-, Нn-2А2-, … Аn-), и общая концентрация кислоты будет равна.
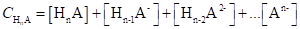
(1.98).
Рассмотрим расчеты равновесных концентраций анионов и недиссоциированных молекул на примере слабой двухосновной кислоты Н2А. В этом случае.
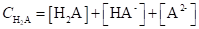
(1.99).
Запишем выражения для констант диссоциации кислоты Найдем значения [Н2А] и [НА-].
Подставим эти значения в уравнение (1.99).
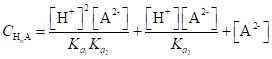
(1.100).
Решая последнее уравнение относительно [А2-], получим.
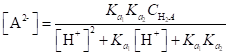
(1.101).
Аналогично можно найти значения [HA-] и [Н2А].
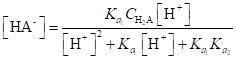
(1.102).
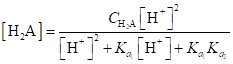
(1.103).
В общем случае в растворе любой слабой многоосновной кислоты НnА в соответствии с уравнением (1.98) и учетом констант диссоциации кислоты равновесные концентрации недиссоциированных молекул и анионов могут быть рассчитаны по следующим уравнениям:
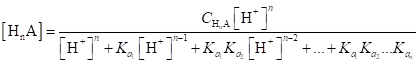
(1.104).
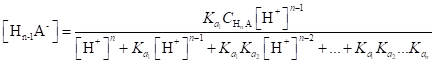
(1.105).
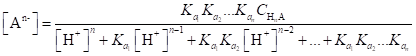
(1.106).
Пример 21. Вычислить б, [Н+] и рН 0.4 М раствора уксусной кислоты, к литру которого добавлено 16.4 г ацетата натрия.
Решение. Находим концентрацию ацетата натрия (СА-) в М, (М. м. CH3COONa = 82).
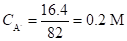
По уравнению (1.89) вычисляем б.
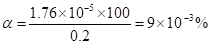
Находим концентрацию Н+-ионов по уравнению (1.88).
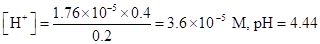
Пример 22. Как изменится рН и б 1.0 М раствора NH3 после добавления к нему сухого хлорида аммония в таком количестве, что раствор становится 0.2М в отношении NH4C1?
Решение. До добавления соли в исходном растворе концентрация ОН- была равна.
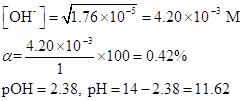
После введения соли.
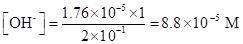
pOH = 4.06; pH = 14−4.06 = 9.94.
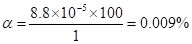
Пример 23. Вычислить концентрацию ацетат-иона и степень диссоциации уксусной кислоты, если к 20 мл 0.5 М раствора ее прибавить 30 мл 10%-ного раствора НСl.
Решение. Находим концентрации СН3СООН (СНА) и Н+:
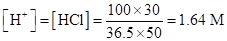
Поскольку [H+] значительно превышает константу диссоциации уксусной кислоты, для расчета концентрации ацетат-иона можно использовать уравнение (1.97).
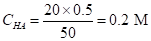
Находим степень диссоциации б:
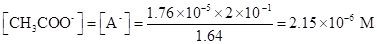
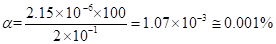
Пример 24. Вычислить концентрации HS- и S2--ионов в насыщенном растворе H2S, если рН раствора равен 4.
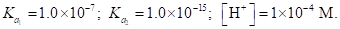
Решение. В насыщенном растворе. Константы диссоциации сероводородной кислоты равны Применив уравнение (1.101) и уравнение (1.102), найдем:
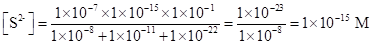
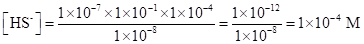
Пример 25. Рассчитать равновесную концентрацию НРО42- при рН = 7, если общая концентрация соли равна 0.1 М.
Решение.
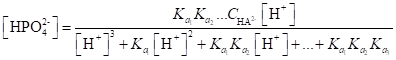
=.
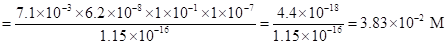
Задачи Вычислить степень диссоциации Взяты поровну 0.3%-ные растворы аммиака и хлорида аммония.
Взяты поровну 0.5%-ные растворы уксусной кислоты и ацетата калия.
Взяты поровну 1%-ные растворы муравьиной кислоты и гидроксида калия.
Взяты поровну 3%-ные растворы азидоводородной кислоты и гидроксида калия.
Взяты поровну 0.8%-ные растворы ацетата натрия и иодоводородной кислоты.
Взяты поровну 0.7%-ные растворы аммиака и иодоводородной кислоты.
Смешано 370 мл 0,5%-ного раствора уксусной кислоты и 450 мл 1.2%-ного раствора ацетата натрия.
Смешано 415 мл 0.9%-ного раствора уксусной кислоты и 472 мл 2%-ного ацетата лития.
Взяты поровну 0.25%-ные растворы бензойной кислоты и ее калиевой соли.
Взяты поровну 0.3%-ный раствор бензойной кислоты и 0.1%-ный раствор гидроксида калия.
Смешаны поровну 2%-ные растворы гидразина N2H4 и хлорида гидразиния (1+).
Смешано 969 мл 0,2%-ного раствора уксусной кислоты и 315 мл 0.3%-ного раствора ацетата лития.
Смешано 126 мл 1%-ного раствора муравьиной кислоты и 173 мл 2%-ного раствора формиата натрия.
Смешано 112 мл 0.5%-ного раствора аммиака и 639 мл 1.5%-ного раствора хлорида аммония.
Смешано 83 мл 0.6%-ного раствора аммиака, 76 мл 0.3%-ного раствора хлорида аммония и 269 мл воды.
Вычислить степень диссоциации и концентрацию водородных ионов Смешано 99 мл 3%-ного раствора муравьиной кислоты, 88 мл 0.3%-ного раствора формиата лития и 777 мл воды.
Смешано 77 мл 1%-ного раствора муравьиной кислоты, 77 мл 0.5%-ного раствора формиата калия и 777 мл воды.
. Смешано 50 мл 1%-ного раствора гидроксиламина, 50 мл 0,2%-ного раствора его хлористоводородной соли и 900 мл воды.
Смешано 15 мл 0,5%-ного раствора дихлоруксусной кислоты, 25 мл 1.5%-ного раствора ее калиевой соли и 110 мл воды.
Смешано 150 мл 2,7%-ного раствора уксусной Кислоты, 50 мл 1,5%-ного раствора гидроксида натрия и 50 мл воды.
Смешано 187 мл 3%-ного раствора формиата калия, 63 мл 0.5%-ного раствора НСl и 465 мл воды.
Смешано 15 мл 1.5%-ного раствора хлорида аммония, 15 мл 1.5%-ного раствора КОН и 15 мл воды.
Смешано 183 мл 9%-ного раствора моноиодацетата калия, 43 мл 5%-ного раствора хлороводородной кислоты и 457 мл воды.
Смешано 183 мл 9%-ного раствора моноиодацетата калия, 43 мл 5%-ного раствора бромоводородной кислоты и 457 мл воды.
Смешано 210 мл 10%-ного раствора монохлорацетата натрия, 150 мл 1.3%-ного раствора хлороводородной кислоты и 40 мл воды.
Вычислить степень диссоциации и концентрацию ионов слабых кислот и оснований.
95. К 0,2 М раствору уксусной кислоты добавлена хлороводородная кислота до рН = 1.
К 20 мл 0.2 М раствора уксусной кислоты добавлено 5 мл 1 М раствора хлороводородной кислоты.
К 50 мл 1%-ного раствора муравьиной кислоты добавлено 5 мл 10%-ного раствора хлороводородной кислоты.
К 20 мл 0,5 М раствора азидоводородной кислоты добавлено 5 мл 5%-ной хлороводородной кислоты.
К 0.05 М раствору циановой кислоты добавлено хлороводородной кислоты до рН = 0.5.
К 1%-ному раствору циановой кислоты добавлен равный объем 1 М хлороводородной кислоты.
К 0.05 М раствору щавелевой кислоты добавлена сильная кислота до рН = 2,0. Найти концентрацию С2О42-
Рассчитать концентрацию С2О42- в 0.05 М растворе щавелевой кислоты при рН = 4.3.
Вычислить концентрации H2S и HS- в 0.1 М растворе сероводородной кислоты при рН = 5.
рН раствора, через который был пропущен сероводород до концентрации 0.1 М, равен 8.3. Рассчитать концентрации HS- и S2- в этом растворе.
Вычислить равновесную концентрацию Н3РО4 в растворе, если общая концентрация ее равна 0.1 М, а рН раствора равен 2.0.
Рассчитать равновесные концентрации H3AsO4 и H2As04- в 0.03 М растворе мышьяковой кислоты, рН которого равен 2.
Рассчитать концентрацию иона СО32- в 0.1 М растворе карбонатов с рН = 9.
Вычислить концентрации H2SO3 и HSO3- в 0.1 М растворе сульфитов при рН = 4.
Вычислить концентрацию иона SO32- в 0.1 М растворе сульфитов при рН = 7.2.
К 20 мл 0.75%-ного раствора аммиака прибавлено 10 мл 2.5%-ного раствора гидроксида натрия.
К 50 мл 0.1%-ного раствора аммиака прибавлен 1 г гидроксида калия.
К 0.25 М раствору анилина добавлена щелочь до рН = 8.0.
113. К 25 мл 0.1 М бутиламина прибавлено 25 мл 1 М раствора гидроксида натрия.