Вода.
Общая и неорганическая химия

Вода, которая присоединена в этих случаях, называется конституционной (в отличие от кристаллизационной в кристаллогидратах). Вода активно взаимодействует с основными и кислотными оксидами, образуя, соответственно, гидроксиды (основания) и кислоты: Такой процесс возможен в присутствии веществ, отщепляющих ион водорода. Вода реагирует с галогенами с образованием смесей кислот: Рис. 11.1. Строение… Читать ещё >
Вода. Общая и неорганическая химия (реферат, курсовая, диплом, контрольная)
Физические свойства. Чистая вода представляет собой бесцветную прозрачную жидкость без запаха и вкуса. Из всех жидких и твердых веществ она обладает наибольшей теплоемкостью. Вода существует в трех агрегатных состояниях: твердое — лед, жидкое и газообразное — водяной пар. При 0 °C твердая и жидкая фазы находятся в состоянии динамического равновесия, следовательно, температура плавления льда равна 0 °C. При 100 °C в равновесии находятся жидкая и газообразная фазы, поэтому температура кипения воды соответствует 100 °C. При +4°С вода имеет наибольшую плотность, равную 1 г/см3. Выше или ниже этой температуры плотность воды меньше 1 г/см3. Эта особенность отличает воду от всех других веществ, плотность которых с понижением температуры увеличивается. При переходе воды из жидкого в твердое состояние происходит увеличение объема и уменьшение плотности: из 92 объемов жидкой воды образуется 100 объемов льда. Лед легче воды, поэтому всегда всплывает на поверхность. Молекула воды построена по типу треугольника, в вершине которого находится электроотрицательный атом кислорода, а в углах оснований — водород. Валентный угол равен 104°27'. Такая особенность молекулы воды подтверждается и тем, что ее электрический момент диполя равен 0,61 • 10 29 Кл м.
Орбитали неподеленных пар электронов направлены в сторону, противоположную той, где находятся протоны (рис. 11.1). Заряды расположены вокруг центра атома кислорода тетраэдрически: знак «+» обозначает пониженную электронную плотность (места, где находятся протоны), а знак «-» — повышенную (места расположения орбиталей неподеленных пар).
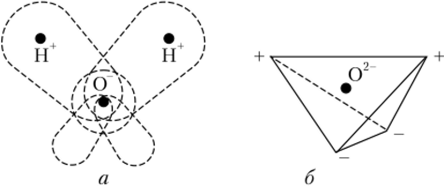
Рис. 11.1. Строение молекулы воды:
а — расположение орбиталей; б — общая форма Поляризация молекулы воды объясняется тем, что электроотрицательный атом кислорода оттягивает на себя электрон от каждого атома водорода, а ядра водорода фактически лишены своих электронов. Такая полярная молекула может взаимодействовать с другой молекулой с образованием водородной связи. Это явление получило название ассоциации воды.
В состоянии пара молекулярная масса воды равна 18, что соответствует формуле Н20. В остальных случаях молекулярная масса воды в кратное число раз больше 18. Так, при 4 °C она равна 36, при 0 °C — 54. Следовательно, при 4 °C ассоциировано две молекулы — (Н20)2, а при 0 °C — три молекулы — (Н20)3.
Химические свойства. Полярность и малые размеры молекулы воды определяют ее сильные гидратирующие свойства. Так как диэлектрическая проницаемость воды очень велика (81), она оказывает сильное ионизирующее действие на растворенные в ней электролиты, вызывая их диссоциацию.
Молекула воды способна присоединяться к различным ионам, образуя гидраты. Эти соединения характеризуются специфическим строением, напоминая комплексные соединения. Один из важнейших продуктов взаимодействия — ион гидроксония НэО+, образующийся вследствие присоединения иона Н* к неподеленной паре электронов атома кислорода. Вследствие этого процесса образующийся ион гидроксония приобретает положительный заряд:

Такой процесс возможен в присутствии веществ, отщепляющих ион водорода.
Вода как на холоде, так и при нагревании активно взаимодействует со многими металлами, стоящими в ряду стандартных электродных потенциалов до водорода. В этих реакциях образуются соответствующие оксиды или гидроксиды и вытесняется водород:
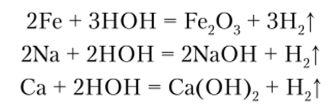
Вода реагирует с галогенами с образованием смесей кислот:
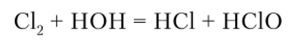
В окислительно-восстановительных реакциях вода обычно выполняет роль среды. При действии сильных окислителей (например, хлора) вода проявляет восстановительные свойства, а при действии восстановителей (Са, Na) — окислительные.
Вода активно взаимодействует с основными и кислотными оксидами, образуя, соответственно, гидроксиды (основания) и кислоты:
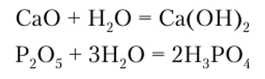
Вода, которая присоединена в этих случаях, называется конституционной (в отличие от кристаллизационной в кристаллогидратах).