Очистка выбросов от паров и газов

Адсорбционный метод — это процесс избирательного поглощения из жидкости (газа) одного или нескольких компонентов, как правило, поверхностью твердого тела (адсорбентом). Адсорбция является поверхностным процессом и поэтому завершается в доли секунды. По аналогии с абсорбцией адсорбция может быть физической и химической. Физическая адсорбция вследствие своей обратимости нашла применение главным… Читать ещё >
Очистка выбросов от паров и газов (реферат, курсовая, диплом, контрольная)
Методы очистки вентиляционных и технологических выбросов от вредных газообразных и паровых примесей зависят от свойств самих примесей, их концентраций, от санитарно-гигиенических, градостроительных и других требований. Наибольшее применение для указанных целей нашли абсорбционный и адсорбционный методы, ионообменная очистка, термическое дожигание.
Абсорбционный метод очистки воздуха от газообразных примесей основан на избирательном поглощении, как правило, всем объемом жидкого вещества, одного или нескольких компонентов из газовой смеси. Различают физическую абсорбцию и хемосорбцию. При физической абсорбции молекулы абсорбата (извлекаемого газа) не вступают в химическую реакцию с молекулами абсорбента (жидкий поглотитель). При хемосорбции молекулы абсорбента и абсорбата образуют новое химическое соединение.
В качестве абсорбента может быть использована любая жидкость, но обычно при физической абсорбции применяют воду, а при химической — растворы аммиака, карбоната натрия, калия и т. д.
Физическая абсорбция в большинстве случаев обратима. На этом свойстве абсорбционных процессов основано выделение поглощаемого газа или пара из раствора — десорбция. Процесс перехода вещества из одной фазы в другую (массопередача) протекает до тех пор, пока между фазами при определенных условиях не установится состояние подвижного равновесия, то есть такого состояния, когда из абсорбата в абсорбент переходит столько вещества (абсорбция), сколько из абсорбента в абсорбат (десорбция). Равновесный состав фаз для идеальных газов выражается законом Генри: парциальное давление извлекаемого газа над раствором р^ Па, пропорционально его мольной доле см в растворе: 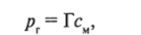
где Г — коэффициент пропорциональности, или постоянная Генри, зависящая от температуры, свойств газа и жидкости, в которой газ растворен, Па.
Уравнение материального баланса абсорбционного процесса можно выразить следующим равенством:
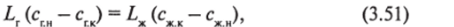
где LM — расход инертного газа и раствора абсорбента, м3/с; сги, сгк — начальная и конечная концентрация абсорбата в газовой смеси, кмоль/м3 инертного газа; сжк, сжн — начальная и конечная концентрации извлекаемого газа в растворе, кмоль/м3 абсорбента.

Скорость абсорбции (количество вещества, перенесенного из одной фазы в другую), <7б, кмоль/с, пропорциональна коэффициенту массопередачи р, м/с, площади массового контакта А, м2, и движущей силе процесса Ас, кмоль/м3:
Движущая сила процесса массопередачи (она может быть выражена также разностью парциальных давлений, мольных долей и относительных концентраций) рассчитывается как по газовой, так и по жидкой фазам:
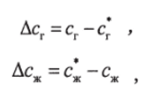
по газовой фазе:
по жидкой фазе:
* •.
где Сг, Сг — равновесные концентрации в газообразной и жидкой фазах, кмоль/м3.
Коэффициент массопередачи р в зависимости от способа выражения движущей силы может быть отнесен как к газовой р(, так и к жидкой Рж фазам и определяется уравнениями аддитивности фазовых сопротивлений:
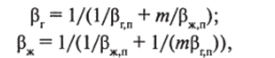
где т — Г/р — коэффициент распределения или контакта газового равновесия (здесьр — общее давление в системе, Па); ргп — коэффициент массоотдачи от потока газа к поверхности контакта фаз, м/с; ржп — коэффициент массопередачи от жидкости к поверхности контакта, м/с.
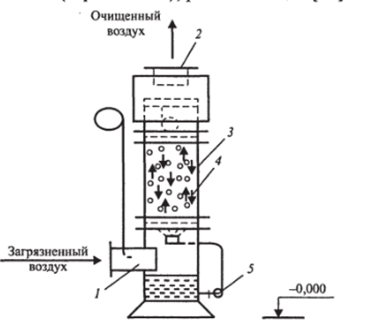
Рис. 3.20. Схема турбулентно-контактного абсорбера:
- 1 — входной патрубок; 2 — выходной патрубок; 3 — корпус;
- 4 — подвижная насадка; 5 — насос
Аппараты для осуществления абсорбционных процессов называются абсорберами (рис. 3.20). Так как абсорбция протекает на поверхности раздела фаз, то абсорберы должны иметь развитую поверхность соприкосновения между жидкостью и газом. По способу образования этой поверхности аппараты для проведения абсорбционных процессов разделяют на следующие группы: поверхностные и пленочные; насадочные; барботажные (тарельчатые); распыляющие [53].
При расчете абсорбера заданными обычно бывают расход газа, его начальная и конечная концентрации или степень извлечения (очистки) газа, начальная концентрация абсорбента. Основными определяемыми величинами являются расход абсорбента ?ж, площадь сечения А^ и высота h абсорбера, аэродинамическое сопротивление Ар аппарата.
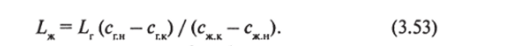
Расход абсорбента находят из равенства (3.51), задаваясь конечной концентрацией жидкости сжк, исходя из оптимального удельного ее расхода:
Аэродинамическое сопротивление абсорбера зависит от конструктивных особенностей аппарата, аэродинамического режима его работы, связанного со скоростью газа, и определяется по зависимости (3.35).
Если абсорбция проводится под повышенным давлением, то аэродинамическое сопротивление абсорбера составляет незначительную долю общего давления в системе и не оказывает существенного влияния на экономические показатели установки.

Площадь сечения, Ааб, м2, абсорбера определяют по условной скорости газа v, м/с, в сечении установки:
Высота активной части абсорбера Л, м, рассчитывается из общего уравнения массопередачи по формуле:
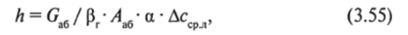
где, а — удельная поверхность контакта фаз, м_|.
Адсорбционный метод — это процесс избирательного поглощения из жидкости (газа) одного или нескольких компонентов, как правило, поверхностью твердого тела (адсорбентом). Адсорбция является поверхностным процессом и поэтому завершается в доли секунды. По аналогии с абсорбцией адсорбция может быть физической и химической. Физическая адсорбция вследствие своей обратимости нашла применение главным образом для улавливания и возвращения (десорбция) в производство паров органических растворителей. В качестве адсорбентов используют следующие пористые материалы: активные (активированные) угли, силикагели, алюмогели, цеолиты (молекулярные сита) [33].
Явление адсорбции осуществляется в результате притяжения между молекулами адсорбента и адсорбата на границе раздела соприкасающихся фаз. Внутри каждой фазы молекулы испытывают практически одинаковую силу притяжения друг к другу, а на границе раздела фаз силовые поля не уравновешены и на молекулы адсорбата влияют силы притяжения молекул носителя и адсорбента. В результате такого взаимодействия возникает результирующая сила, направленная к поверхности адсорбента, и происходит процесс перехода молекул адсорбата из газовой фазы в поверхностный слой адсорбента.
Количество газа, адсорбируемого определенным количеством данного адсорбента, зависит от вида газа и от условий протекания процесса, в первую очередь от давления газа и его температуры. Влияние давления газа на его адсорбируемое количество можно изобразить кривыми, называемыми изотермами адсорбции. Для аналитического выражения адсорбционной изотермы применяют различные зависимости, в частности эмпирическое уравнение Фрейндлиха:
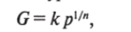
где G — количество адсорбированного газа, кг/с; р — давление газа при достижении равновесий, Па; к, п — эмпирические параметры, постоянные для конкретных адсорбента и адсорбата.
Изотермы адсорбции определяются опытным путем. Вид изотермы адсорбции зависит от многих факторов, главными из которых являются: удельная поверхность адсорбента, структура адсорбента, свойства поглощаемого вещества, температура процесса и т. д.
Адсорбция сопровождается уменьшением парциального давления пара (газа) поглощаемого вещества и выделением теплоты, поэтому количество поглощаемого вещества возрастает с повышением давления и понижением температуры процесса.
Характер и скорость протекания процесса адсорбации зависит от того, проводится процесс периодически или непрерывно, так как в первом случае слой адсорбента будет неподвижным, а во втором — движущимся. В зависимости от характера процесса адсорбции, применяемые для этих целей аппараты (адсорберы) подразделяются на адсорберы с неподвижным слоем поглотителя и адсорберы с движущимся или кипящим слоем поглотителя (рис. 3.21). В адсорберах с неподвижным слоем поглотителя процесс извлечения адсорбата из газовоздушной смеси обычно проводят в четыре стадии: собственно адсорбция, десорбция, сушка поглотителя и охлаждение поглотителя. Принцип работы адсорберов с движущимся или кипящим слоем поглотителя аналогичен абсорбционным аппаратам.
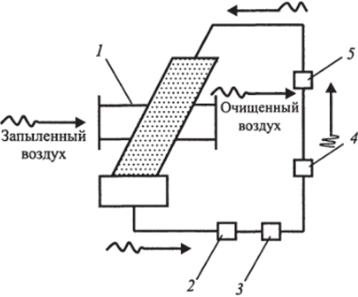
Рис. 3.21. Схема адсорбера:
1 — адсорбер, 2 — дссорбср, 3 — сушилка, 4 — охладитель, 5 — питатель Расчет адсорберов включает определение его геометрических размеров (площадь сечения, высота) и расход адсорбента.
Площадь сечения адсорбера определяют по формуле:

где Lcm — расход паровой или газовой смеси, проходящей через слой адсорбента, м3/с; уф — фиктивная скорость парогазовой смеси, определяемая для периодически действующих аппаратов по технико-экономическим показателям, а для непрерывно действующих аппаратов — исходя из создания заданного гидродинамического режима, например устойчивого псевдоожиженного слоя зерен адсорбента, м/с.
Высота адсорбера зависит от высоты слоя адсорбента /, м, которая определяется по формулам:
для аппаратов периодического действия.


и для аппаратов непрерывного действия где — скорость перемещения фронта (зоны массопередачи), м/с, определяемая из уравнения материального баланса; т — время адсорбционного действия слоя (опытная величина), с; т0 — потеря времени адсорбционного действия слоя (опытная величина), с; V— объем слоя адсорбента, определяемый из материального баланса процесса, м3; Аи — площадь сечения слоя адсорбента, м2.
Важным и неотъемлемым от процесса адсорбции, проводимого в замкнутом цикле, является десорбция — извлечение адсорбированного вещества из твердого поглотителя. Основными методами десорбции являются:
- • вытеснение из адсорбента поглощенных компонентов с помощью агентов, обладающих более высокой адсорбционной способностью, чем поглощенные компоненты;
- • испарение поглощенных компонентов путем нагрева слоя адсорбента.
При расчете десорбции определяют, как правило, на основании опытных данных продолжительность процесса (для аппаратов периодического действия) и расход десорбирующего агента (водяного пара, воздуха и т. п.).
Для очистки вентиляционных выбросов от газов с полярными молекулами применяются иониты. По своей физико-химической сути этот процесс близок к абсорбции. Иониты представляют собой нерастворимые твердые вещества, способные обменивать содержащиеся в них ионы на другие ионы, присутствующие в другой жидкой или газообразной фазе. Формула ионитов может быть представлена в виде: HR, ROH (R означает полимерное состояние вещества). Иониты могут быть естественными — алюмосиликаты (глины), и искусственными — ионообменные смолы (NaA, СаА, NaX. СаХ). Иониты используются в виде зерен с гранулами различной формы. С очищаемым веществом иониты могут реагировать по следующим схемам:
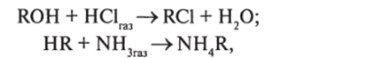
то есть могут избирательно улавливать тот или иной кислый или щелочной компонент из газовой смеси.
Регенерация полученной при ионообменной очистке солевой формы осуществляется промывкой слабым (5%) раствором кислоты или щелочи для перевода ионита в первоначальную форму, например, по схеме: 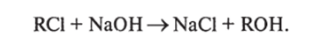
Ионообменная очистка газов осуществляется в аппаратах двух типов: аппараты с кипящим слоем или аппараты со слоевым фильтром. В первых аппаратах применяют иониты в виде зерен размером 0,2−2,0 мм, во вторых — в виде волокнистого материала с диаметром волокон от 5 до 35 мкм. Аппаратурное оформление процессов ионообменной очистки вентиляционных выбросов во многом аналогично оформлению других сорбционных процессов — адсорбции, абсорбции, десорбции и т. п.
Ионообменная очистка высокоэффективна, может происходить в присутствии водяных паров, иметь высокую емкость по улавливаемому компоненту. Однако эффективность очистки значительно снижается при повышении температуры газа и увеличении его запыленности.
Термическая очистка (термический метод обезвреживания) широко применяется для очистки вентиляционных и газообразных технологических выбросов от паров цианистой и синильной кислот, оксида углерода, водорода, органических растворителей (толуол, бензин, бензол и т. д.) [53].
Термический метод обезвреживания может быть прямым, когда загрязняющее вещество сгорает в пламени при высоких (1000−1500 °С) температурах, и косвенным, когда при температурах 150—250°С в присутствии катализаторов происходит окисление загрязнителя и его восстановление до нетоксичных составляющих. Возможно также применение термосорбционной очистки газов — термического метода обезвреживания выбросов в атмосферу с сорбированием несжигаемых компонентов в очищаемых газах.