Азот.
Химия

Наибольшее практическое значение имеет реакция между азотом и водородом с образованием аммиака, так как он служит основным источником азота для промышленности и сельского хозяйства. Получение соединений азота было трудной проблемой еще в начале XX в. Немецкий химик Ф. Габер (F. Haber) внес существенный вклад в решение проблемы связывания атмосферного азота (Нобелевская премия по химии 1918 г… Читать ещё >
Азот. Химия (реферат, курсовая, диплом, контрольная)
Считается, что азот открыт в 1772 г. почти одновременно несколькими учеными как газ, содержащийся в воздухе, но не поддерживающий дыхания. Название элемента происходит от греч. а — отрицательная приставка, где — жизнь («безжизненный»). Такую оценку азота можно считать справедливой только в отношении простого вещества, но азот как элемент необходим для жизни, так как вместе с углеродом, водородом и кислородом он образует белки и другие жизненно важные вещества. В организме человека содержится в среднем 1,8 кг азота.
Азот довольно широко распространен в биосфере. Наибольшее количество азота находится в виде простого вещества N2 в воздухе. Твердых минералов у азота почти нет. Лишь в исключительно сухой пустыне на севере Чили найдены залежи нитрата натрия, названного чилийской селитрой. Значительное количество азота содержится в биомассе растений и животных и в органических остатках (каменный уголь содержит 1,0—1,8% азота). В обычных условиях на поверхности Земли большая часть азота из отмерших растений постепенно превращается в газообразный азот и переходит в атмосферу. Некоторая доля имеющихся в почве соединений азота вымывается водой и попадает в водоемы. Поэтому растения часто оказываются в условиях недостатка азота, несмотря на то что они окружены богатой азотом атмосферой! Такая ситуация не возникает в случае кислорода, который тоже находится в атмосфере и активно используется растениями и животными. Это различие между азотом и кислородом связано с необыкновенной прочностью молекул N2. Они с трудом участвуют как в обычных химических, так и в биохимических реакциях.
По строению атома азот — трехвалентный элемент. В устойчивых соединениях азот, как правило, образует не менее трех химических связей. Однако азот не может повысить свою валентность за счет перехода в возбужденное состояние. Единственная возможность перехода азота в четырехвалентное состояние — это потеря одного электрона:
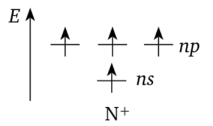
В таком состоянии азот может находиться только в соединениях с более электроотрицательными элементами — кислородом и фтором.
Атом азота имеет валентную электронную пару на подуровне 2s и как донор (основание) часто образует дополнительную химическую связь по донорно-акцепторному механизму. Примером таких соединений служат соли аммония и комплексные соединения с аммиаком в качестве лиганда. В соединениях с большинством химических элементов азот проявляет отрицательные степени окисления, в соединениях с кислородом — положительные степени окисления, в том числе и +5.
Для азота известно только одно простое вещество N2. Молекулы N2 имеют на два электрона меньше, чем молекулы кислорода:
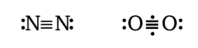
Два дополнительных электрона в молекуле кислорода 02 уменьшают прочность связи. Связь между атомами азота без этих электронов становится по-настоящему тройной, и молекула N2 оказывается самой устойчивой и наименее реакционноспособной из всех молекул. Энергия связи в молекуле N2 составляет 946 кДж/моль.
Прочностью молекул N2 определяются не только свойства этого вещества, но и поведение химических соединений азота. Они, как правило, не очень устойчивы. Про азот можно сказать, что при каждом удобном случае он стремится выделиться из соединения и образовать простое вещество N2.
Получение азота. Лабораторный способ получения азота заключается в разложении нитрита аммония при слабом нагревании как твердого вещества, так и его раствора:
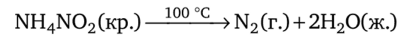
При сгорании органических соединений азота также образуется простое вещество:
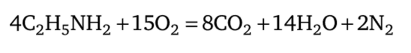
В промышленности азот получают из воздуха ректификацией при низкой температуре (температура кипения азота -195,8 °С). Используют также азот воздуха после удаления кислорода химическим способом. В этом случае азот содержит примесь благородных газов.
Химические свойства азота. При обычных условиях азот реагирует только с активным металлом литием. На воздухе поверхность металла быстро покрывается смесью оксида и нитрида лития:
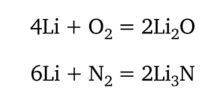
С кислородом азот начинает реагировать при нагревании до 2000 °С:
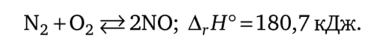
Эта реакция обратимая и эндотермическая. Выход оксида азота (Н) составляет лишь несколько процентов. В небольшом количестве оксид N0 образуется в атмосфере при грозовых разрядах.
Наибольшее практическое значение имеет реакция между азотом и водородом с образованием аммиака, так как он служит основным источником азота для промышленности и сельского хозяйства. Получение соединений азота было трудной проблемой еще в начале XX в. Немецкий химик Ф. Габер (F. Haber) внес существенный вклад в решение проблемы связывания атмосферного азота (Нобелевская премия по химии 1918 г.), разработав катализатор для синтеза аммиака — металлическое железо, активированное добавками оксидов алюминия и калия. В 1913 г. был пущен первый завод по производству аммиака, а в настоящее время годовое производство аммиака превышает 100 млн т. Приблизительно столько же азота возвращается в атмосферу за год в результате процессов гниения в почве и сжигания топлива.
В параграфе 3.6 были рассмотрены принципы выбора условий проведения процесса синтеза аммиака. Экономически приемлемое сочетание выхода продукта и скорости его образования может быть достигнуто только при применении катализатора и высокого давления. Теперь на разных аммиачных заводах применяют давление 300—500 атм и температуру около 300 °C. При этом выход аммиака составляет не многим более 10%. Однако смесь азота и водорода после отделения полученного аммиака снова направляют в контактный аппарат с катализатором, и таким образом доля превращения сырья в аммиак повышается.
В химии уже длительное время изучается возможность получения соединений азота при обычной температуре и обычном давлении, так как применение устройств высокого давления дорого и опасно: они могут взрываться. Известны микроорганизмы — нитробактерии, содержащие фермент нитрогеназу, при участии которого азот восстанавливается в бактериальной клетке, превращаясь в необходимые органические соединения. Но искусственно воспроизвести работу этих чрезвычайно сложных ферментов или похожих на них веществ пока не удается.
Классификация важнейших соединений азота приведена на рис. 6.3.
Соединения азота. Аммиак. Рассмотрим свойства важнейшего соединения азота — аммиака. В лаборатории газообразный аммиак получают из его водного раствора или из растворов солей аммония под действием щелочи:
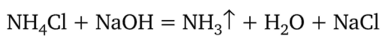
Аммиак представляет собой бесцветный газ с резким характерным запахом, сжижающийся под давлением ~7 атм. У аммиака очень большая растворимость в воде: 700 объемов аммиака в 1 объеме воды при температуре 0 °C. Раствор аммиака с массовой долей 10% называется нашатырный спирт. Вдыхание воздуха с небольшой примесью аммиака возбуждающе действует на нервную систему. Это используют для приведения человека в сознание при обмороке.
Молекула аммиака пирамидальная с атомом азота в вершине. Азот находится в 5р3-гибридном состоянии. Три гибридные орбитали участвуют в образовании связей с водородом, а четвертую занимает неподеленная электронная пара азота: 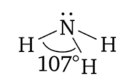
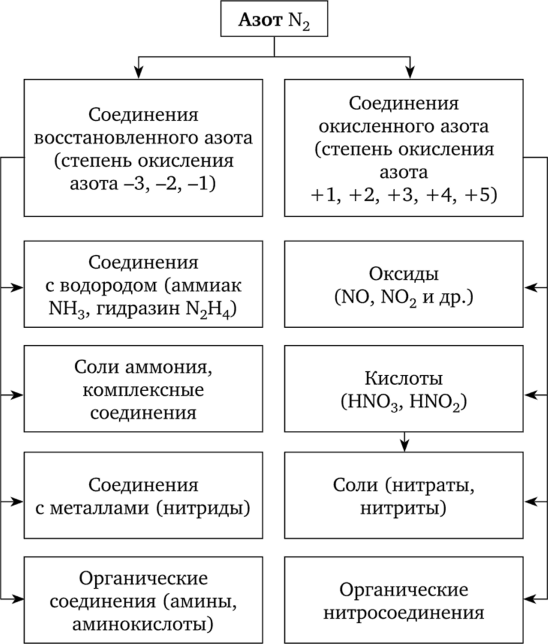
Рис. 6.3. Классификация соединений азота
Аммиак горит в кислороде и окисляется многими веществами с выделением азота:
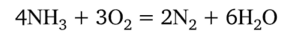
Большое практическое значение имеет каталитическое окисление аммиака до оксида азота (Н). Катализатором служит сплав благородных металлов платины и родия. Образующийся оксид N0 необходим для производства азотной кислоты:
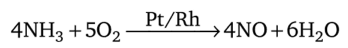
В водном растворе аммиак проявляет основные свойства, так как атом азота — донор электронной пары:
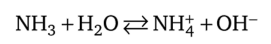
В этой реакции образуется полностью ионизированный гидроксид аммония. Тем не менее аммиак ведет себя как слабое основание, так как в гидроксид аммония превращается всего лишь ~1% растворенного аммиака.
При реакциях с сильными кислотами в растворах или в газообразном состоянии аммиак образует соли аммония:
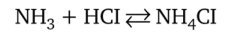
Хлорид аммония называется нашатырь. Соли аммония находят разнообразное практическое применение. Сульфат и нитрат применяют в больших количествах в качестве азотных удобрений. По растворимости в воде эти соли похожи на соли калия. Сходство их объясняется близостью ионных радиусов NH4 и К+. В отличие от солей щелочных металлов соли аммония в небольшой степени гидролизуются и создают кислую среду (pH ~ 5). Под действием щелочей из них выделяется аммиак.
Кристаллические соли аммония разлагаются при нагревании. Если анион соли устойчив, то реакция разложения обратима:
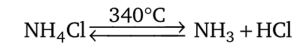
Карбонат аммония медленно разлагается при обычной температуре, и его белый порошок постепенно исчезает. Эту соль применяют в кулинарии при выпечке бездрожжевого теста:
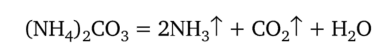
Соли аммония с окисляющими анионами при нагревании разлагаются необратимо:
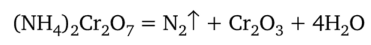
Оксиды азота. Известно несколько оксидов азота, образование и превращение которых можно представить в виде следующей схемы:
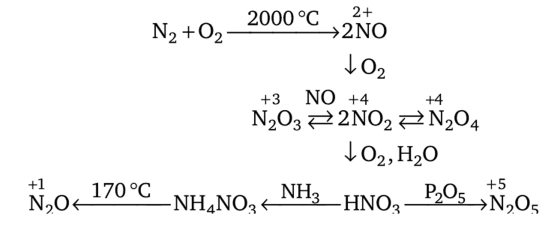
Напишите уравнения реакций, соответствующих приведенной выше схеме.
В оксидах азот трехили четырехвалентен. Степени окисления азота, указанные на схеме, в ряде случаев являются усредненными, так как атомы азота в некоторых молекулах (N20, N203) находятся в разных состояниях. Например, структурная формула оксида азота (1) следующая:
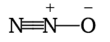
Все оксиды азота неустойчивы и проявляют окислительные свойства по отношению к металлам, некоторым неметаллам, углеводородам. Магний и уголь горят в газообразных оксидах азота:
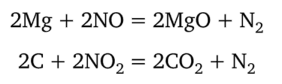
Оксиды азота ядовиты. Поэтому большим благом является отсутствие реакции между азотом и кислородом при обычных условиях вблизи поверхности Земли. Но все же образование оксидов азота оказывается побочным явлением при сгорании моторного топлива. Поэтому выхлопные газы автомобилей содержат кроме других ядовитых веществ и оксиды азота (главным образом N02).
Оксиды азота N203 и N205 называют ангидридами, так как они реагируют с водой с образованием кислот:
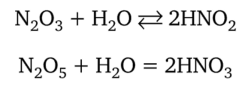
Оксид азота (1У) тоже реагирует с водой, но более сложно. Сначала одновременно образуются азотистая и азотная кислоты:
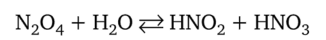
Кислоты можно «зафиксировать» нейтрализацией:
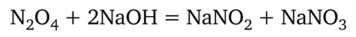
Азотистая кислота неустойчива и разлагается по реакции 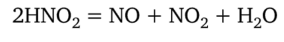
Реакция ускоряется при нагревании. Поэтому при повышении температуры идет суммарная реакция.
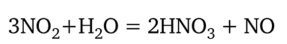
Оксид азота (II) реагирует с кислородом (см. схему выше). Поэтому одновременное действие воды и кислорода на оксид азота (IV) приводит к образованию только азотной кислоты:
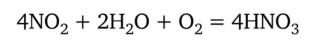
Данная реакция представляет собой заключительную стадию промышленного получения азотной кислоты. Поскольку на самом деле реакция протекает многостадийно и довольно медленно, на заводах, производящих азотную кислоту, всегда происходит выброс оксидов азота в атмосферу. Из заводской трубы выходит рыжеватый дым — «лисий хвост». Окраска дыма обусловлена присутствием N02. На значительном пространстве вокруг большого завода от оксидов азота погибают леса. Особенно чувствительны хвойные породы деревьев.
Кислородные кислоты азота. Рассмотрим свойства кислородных кислот азота. Азотистая кислота слабая и неустойчивая, в ее растворе устанавливаются равновесия:
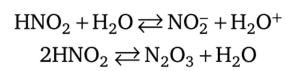
Более устойчивы соли азотистой кислоты — нитриты. Один из способов получения нитритов — термическое разложение нитратов:
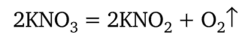
Нитриты ядовиты, так как окисляют в гемоглобине железо (II) до железа (Ш), и гемоглобин теряет способность присоединять и переносить кислород в крови. Применение большого количества азотных удобрений значительно ускоряет рост растений, но при этом они содержат в повышенной концентрации нитраты и нитриты. Из-за этого употребление обычных овощей иногда приводит к отравлениям.
В кислой среде нитриты действуют так же, как сама азотистая кислота. Чаще они бывают окислителями, но могут и сами окисляться сильными окислителями.
Наибольшее практическое значение имеет сильная, относительно устойчивая и летучая азотная кислота. Ее применяют в больших количествах для производства удобрений, нитрования органических веществ, а также для растворения металлов. В лаборатории азотную кислоту можно получить обменным разложением нитратов:
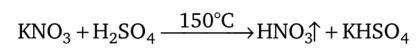
Обычно азотную кислоту применяют в виде водного раствора. При содержании HN03 65—69% раствор называют концентрированной азотной кислотой; растворы с более высоким содержанием HN03 — дымящей азотной кислотой; растворы с содержанием HN03 менее 10% — разбавленной азотной кислотой.
Азотная кислота — довольно сильный окислитель по отношению к металлам и неметаллам, а в отношении органических веществ — нитрующее вещество, добавляющее в молекулу группу N02.
Концентрированная азотная кислота пассивирует поверхность металлов — железа, алюминия и хрома. Это значит, что они перестают реагировать с кислотой. Азотную кислоту можно транспортировать в стальных цистернах.
По силе окислительных свойств в кислой среде ион N03 сильнее, чем ион Н+. Отсюда вытекает важное следствие.
При действии азотной кислоты на металлы вместо водорода выделяются различные оксиды азота, а в реакциях с активными металлами азот восстанавливается до иона NH4.
Соли азотной кислоты (нитраты) известны для всех металлов. Их часто используют для проведения обменных реакций в растворах. При нагревании нитратов активных металлов они превращаются в нитриты с выделением кислорода (см. выше). Нитраты менее активных металлов при термическом разложении дают оксид металла, оксид азота (IV) и кислород: