Ионно-координационная полимеризация.
Высокомолекулярные соединения

Кинетика полимеризации в гетерогенных системах (а многие из них являются трехфазными: «газообразный мономер — растворитель — твердый катализатор») осложняется физическими процессами абсорбции газа жидкой фазой и диффузии растворенного вещества к твердой поверхности катализатора. Для гетерогенных систем характерна линейная зависимость скорости полимеризации от площади поверхности катализатора или… Читать ещё >
Ионно-координационная полимеризация. Высокомолекулярные соединения (реферат, курсовая, диплом, контрольная)
В ряде случаев ионной полимеризации возможно образование макромолекул со значительным содержанием изотактических и синдиотактических последовательностей звеньев, что обусловлено предварительной координацией молекулы мономера на активном центре перед актом присоединения (см. п. 3.2.2,3.2.3). Наиболее ярко явление координации и стереорегулирования проявляется при использовании катализаторов стереоспецифической полимеризации на основе органических производных металлов I—III групп периодической таблицы и их комплексов с соединениями переходных металлов IV—VII групп (табл. 3.18). Общим свойством многочисленных каталитических систем подобного типа является образование комплексов «катализатор — мономер», которое предшествует гетеролитическому разрыву связи в мономере в актах роста цепи.
Первым катализатором стереоспецифической полимеризации была открытая в 1954 г. К. Циглером и затем детально исследованная Дж. Натта система (С2Нд)зА1 + ТЮЦ. Как было установлено, инициатором полимеризации является не каждое из исходных веществ и не их смесь, а продукты их взаимодействия. Ионно-координационные катализаторы используют для полимеризации аолефинов, диеиов и некоторых других мономеров — полярных и циклических. Общий принцип образования инициирующих центров на основе этих катализаторов состоит во взаимодействии соединения переходного металла с металлорганическим соединением (чаще — алюминийорганическим). В результате образуются комплексы, содержащие связь «переходный металл — углерод», что достигается алкилированием переходного металла металлорганическим соединением. На примере классической системы Циглера — Натта протекающие между компонентами катализатора превращения можно представить в виде схемы.
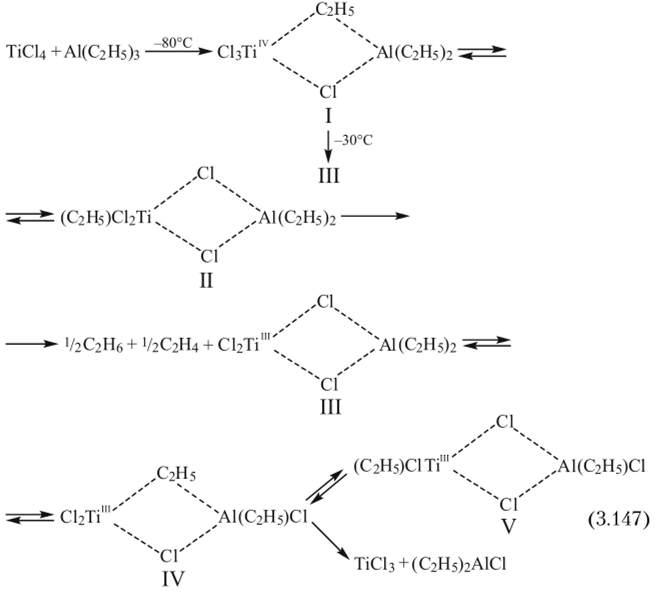
Как очевидно, превращения первичного комплекса I зависят от температуры: при -80°С происходит обратимая изомеризация с возникновением ст-связи Ti-C (комплекс II). Выше -30°С реакция сопровождается восстановлением Tilv в Ti111 и выделением равных количеств этана и этилена. Комплекс III также способен к изомеризации в IV и затем в V, причем последнее соединение содержит a-связь Ti—С. Все комплексы (I—V) могут быть инициаторами полимеризации. Конечными продуктами превращения в рассматриваемой системе являются нерастворимый TiCl3 и (С2Н5)2А1С1.
Определяющая роль в полимеризации на комплексных катализаторах принадлежит переходному металлу, в частности стабильности связи «металл — углерод» (Ti—С в рассматриваемом случае).
Катализаторы ионно-координационной полимеризации бывают гомогенными и гетерогенными (табл. 3.19): к гетерогенным относят системы, в которых взаимодействие исходных веществ приводит к формированию твердой фазы. Принципиальных различий в механизме действия гомогенных и гетерогенных катализаторов нет.
Общая схема стереоспецифической анионно-координационной полимеризации с изотактическим присоединением может быть представлена следующим образом:
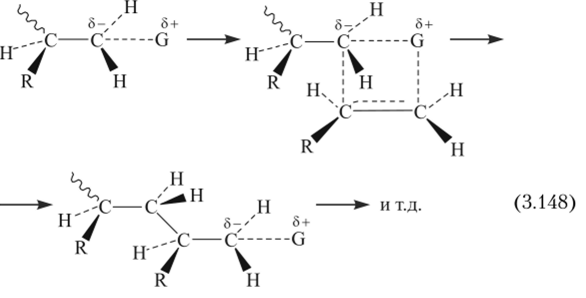
Полагают, что па конце растущей цени имеется тетраэдрический атом С, причем роль четвертого заместителя выполняет фрагмент катализатора G. Аналогично можно представить и катионно-координационную полимеризацию, только на фрагменте G будет знак б, а на атоме С — б+.
Основными факторами, влияющими на полимеризацию с участием переходных металлов, являются электроотрицательность Примеры стсрсоспсцифической полимеризации.
Таблица 3.18
Мономер | Растворитель | Катализатор | T, °c. | Строение цепи полимера |
Бутен-1 | и-Гептан | TiCl3+Zn (C2H5)2 | Изотактиче- ское | |
Изобутилвиниловый эфир | Пропан | BF30(C2H5)2 |
| То же |
Метилакрилат | Толуол | C6H5MgBr или BuLi | — 20. | |
Метилметакри лат | Толуол | BuLi | -78 | |
C2H5A1-N (C6H5)2 | -78 | Синдиотак- тическос | ||
Пропилен | к-Гептан | (С2Н5)зА1 + TiCl4 | Изотактиче- ское | |
Анизол | (;/-QII9)2AlCl + VC14 | -78 | Синдиотак- тичсскос |
Некоторые гомогенные и гетерогенные каталитические системы на основе переходных металлов.
Таблица 3.19
Соединение переходного металла | Метал лоорганическое соединение | Валентное состояние переходного металла | |
Б ИСХОДНОМ. состоянии | б активном центре. | ||
Гомогенные системы | |||
(^MOo-C3H3)2TiCl2 | (C2H5)2A1C1 | Ti (IV) | Ti (IV) |
(W-C4 Hg)/jTi | (С2Н5)зА1. | Ti (IV) | Ti (IV) |
(C5H702)3V* | (C2H5)2A1C1 | V (III) | V (III) |
(С5Н702)3Сг* | (C2H5)2A1C1 | Cr (III) | Cr (III) |
СоС12 | (C2H5)2A1C1 | Со (II) | Со (II) |
Гетерогенные системы | |||
TiCl4 | R3A1 | Ti (IV) | Ti (III) |
TiCl4 | R2A1C1 | Ti (IV) | Ti (IV), Ti (III) |
VC13 | R3A1. | V (III) | V (III) |
TiCl3 | R2A1C1 | Ti (IV) | Ti (III), Ti (II) |
VC13 | (C2H5)2A1C1 | V (III) | V (III), V (II) |
VC13 | (CH3)3A1 | v (III). | v (III). |
Til4 | R2A1 | Ti (IV) | Ti (IV), Ti (111) |
* Ацетилацетоновый радикал СН3С (0)СН2С (0)СН2-.
металла и стабильность связи «металл — углерод». Для полимеризации олефинов наиболее пригодны металлы IV—VI групп (Ti, V, Сг — электроотрицательность 1,32, 1,45 и 1,56), для диенов — металлы VIII группы (Ni, Со — 1,70 и 1,05). Связь «переходный металл — углерод» обычно стабильна только при низких температурах; некоторые лиганды у переходного металла могут стабилизировать се. Рассмотрим в качестве примера растворимый комплекс (^MO0-C5H5)2Ti®Cl-R'(R")AlCl:
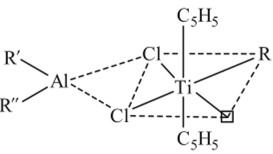
где С5Н5 — циклопентадиенильный радикал; R — алкил; R' и R" — алкил или хлор;? — вакантное место в координационной сфере атома титана.
В исходном соединении атом титана имеет тетраэдрическую конфигурацию, при этом он координационно ненасытен. При взаимодействии с алкилалюминисм образуются мостиковые трехцентровые связи между Ti и А1, титан переходит из тетраэдрической конфигурации в октаэдрическую (он оказывается расположенным в центре правильного октаэдра) с вакантным местом в одной из вершин октаэдра, по которому и координируется молекула мономера. Разрез этого комплекса представлен на рис. 3.20.
Схема роста цепи с координацией молекулы олефина у атома титана представлена ниже (плоскость «R—Ti—вакансия» совпадает с плоскостью листа):
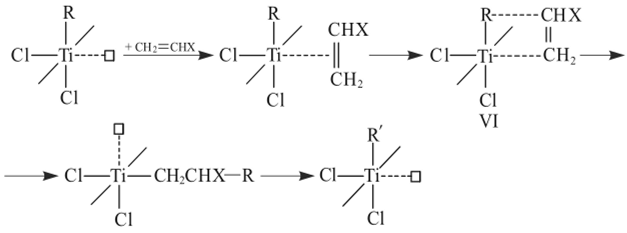
В соответствии с этим механизмом вслед за координацией мономера происходит миграция алкильной группы с образованием связи «R — мономер» (комплекс VI), при этом регенерируется вакантная орбиталь с ориентацией, отличающейся от исходной. По;
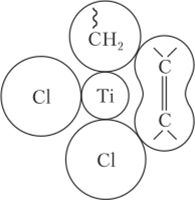
Рис. 3.20. Схематический разрез октаэдрического комплекса TiCl4 — алюминийорганичеекое соединение, но плоскости, содержащей атомы металлов следующее присоединение молекулы мономера к такому комплексу должно привести к формированию синдиотактической последовательности звеньев. Для протекания изотактического присоединения необходимо, чтобы полимерная цепь мигрировала в исходное положение с регенерацией исходной вакантной орбитали.
Кроме рассмотренного монометаллического механизма роста цепи существует и второй — биметаллический, предполагающий рост цепи с участием обоих атомов металлов в комплексе. В соответствии с ним происходит координация молекулы мономера по полярной связи «титан — углерод»:
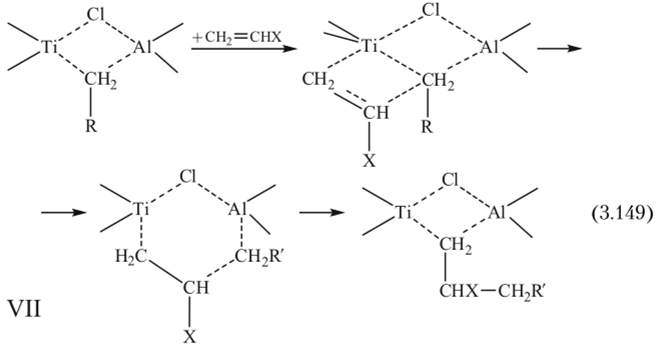
и последующее внедрение в цепь через переходное 6-членное состояние VII. За исключением стадии миграции цепи при обмене ее с вакансией мономолекулярный механизм представляется более предпочтительным, хотя экспериментально строго доказать тот или иной пока не удалось.
Полимеризация в присутствии гомогенных катализаторов наиболее изучена на системе «этилен — дициклопентадиенильные производные титана» — R3A1. Полученные данные показывают, что скорость полимеризации в указанной системе не зависит от длины радикала R, связанного в комплекс с атомом Ti, и от отношения Al/Ti. Полагают, что все атомы титана действуют как активные центры, поэтому уравнение для скорости полимеризации имеет вид.

Для температуры 60 °C kv = 2 лДмоль • с). Решающее влияние на скорость полимеризации в гомогенной системе на основе (цикло- Qjl Ii)2TiX2 (X — хлор или алкил) оказывает прочность связи Ti-C. Если она становится стабильной (система (СГ)1 1Г))С1-Л1С1:!),.
то полимеризация замедляется, а если очень активной, то эта связь распадается прежде, чем начнется полимеризация (система (СзНз^ТДСзЕ^О-ВзЛ!). Восстановление Tilv BTi111 в гомогенных системах ведет к полной дезактивации катализатора, что проявляется в быстром уменьшении скорости процесса (не путать катализ комплексами, содержащими Ti111, в гетерогенной полимеризации, см. табл. 3.19). Восстановление представляет собой диспропорционирование двух растущих цепей:
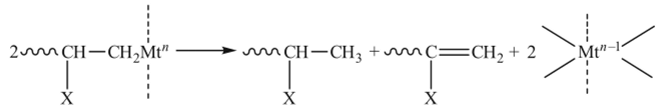
Это превращение аналогично реакции образования этана и этилена в схеме (3.147).
Кроме этого варианта ограничения цепи возможна и ее передача на металлорганическое соединение. Для системы «этилен — (^СНз^АКПДСзН^ТЗС^» с помощью меченного по углероду алюминийорганического соединения удалось определить скорость инициирования и показать, что концентрация растущих цепей сначала увеличивается и, пройдя через максимум, начинает уменьшаться в соответствии с уравнением откуда.
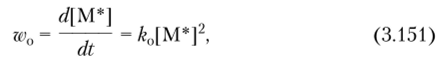
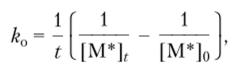
где [ М* |о и [ М * ], — начальная и текущая концентрации растущих цепей.
Па основании данных по суммарной константе полимеризации в указанной системе и уравнения скорости роста.

были определены следующие константы индивидуальных реакций:
- • kH-103 при Т = 0; 15; 30 °C равно соответственно 0,28; 1,12; 4,90 с-1 (?" = 64,5 кДж/моль);
- • kp при Т = 0; 15; 30 °C равно соответственно 1,50; 5,19; 13,60 лДмоль-с) (Ер = 50,7 кДж/моль);
- • k0 при Т = 0; 15; 30 °C равно соответственно 0,49; 2,19; 9,01 лДмоль-с) (Е0 = 68,2 кДж/моль).
Бимолекулярный характер обрыва цепи в рассматриваемой гомогенной полимеризации подтвержден наличием у половины образовавшихся цепей концевых двойных связей. Коэффициент полимеризации с учетом выражений (3.151) и (3.152) и при условии [Tilv]0 = [М*]0 равен.

Текущую концентрацию растущих цепей можно определить решением дифференциального уравнения 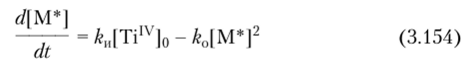
и далее рассчитать молекулярную массу.
Приведенные кинетические данные не имеют универсального характера и являются лишь иллюстрацией особенностей полимеризации на гомогенных каталитических системах.
Полимеризация на гетерогенных системах. Гетерогенные катализаторы образуются либо из растворимых исходных компонентов (например, TiClj + R:iAl), либо тогда, когда один из них нерастворим (TiCl3). Число гетерогенных систем чрезвычайно велико; часть из них приведена в табл. 3.27. Механизм действия таких систем, в принципе, одинаков с гомогенными, но гетерогенные системы обладают большей стереоспецифичностью, связанной с определенным регулирующим действием кристаллической поверхности.
Кинетика полимеризации в гетерогенных системах (а многие из них являются трехфазными: «газообразный мономер — растворитель — твердый катализатор») осложняется физическими процессами абсорбции газа жидкой фазой и диффузии растворенного вещества к твердой поверхности катализатора. Для гетерогенных систем характерна линейная зависимость скорости полимеризации от площади поверхности катализатора или от его массы. Отклонения от линейности, как правило, обусловлены указанными физическими факторами. Поэтому кинетику гетерогенной полимеризации изучают при равновесии между газовой и жидкой фазами, а также в условиях эффективного перемешивания. Обычно рассматривают процесс, состоящий из адсорбции мономера (константа адсорбционного взаимодействия Км) и металлорганического соединения (константа КА) из раствора на поверхности соединения переходного металла с последующим ростом, передачей или обрывом цепи с участием адсорбированных веществ. Превращения на гетерогенных катализаторах схематически представлены ниже (волнистая линия — поверхность соединения переходного металла):
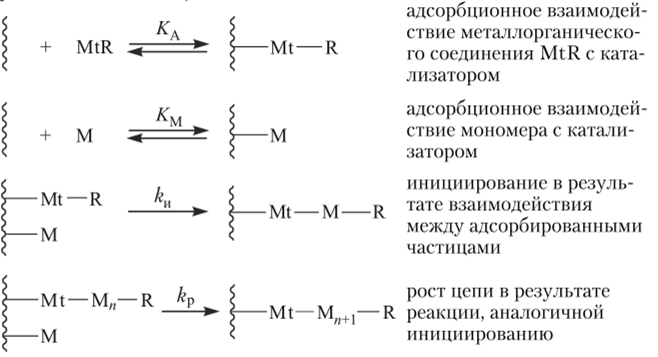
Ограничение цепи может происходить в результате передачи цепи на мономер:

(Р — неактивная макромолекула), самопроизвольным внутренним переносом протона:
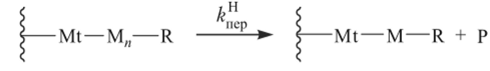
а также реакцией активного центра и мономера с образованием неактивной частицы:
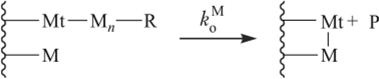
Возможны также ограничения цепи вследствие ее передачи на переходный металл катализатора или на соединения, содержащие подвижные атомы водорода (Н2, вода, спирты и т. п.).
Как следует из схемы (3.147), протекают различные процессы алкилирования и восстановления переходного металла, причем каждый из каталитических комплексов I—V, обладающих различной активностью, может участвовать в инициировании полимеризации. Как следствие, скорость полимеризации в зависимости от условий может возрастать или убывать во времени (рис. 3.21), а результирующий полимер будет иметь широкое ММР.
Кривая 1 соответствует процессу с участием сравнительно крупных частиц катализатора, состоящих из агрегатов мелких кристаллов. При механическом разрушении под действием растущих полимерных цепей большие частицы распадаются на более мелкие, увеличиваются число и поверхность частиц катализатора и растет до некоторого постоянного значения скорость процесса.
Если катализатор предварительно измельчить, то промежуток времени до достижения стационарного состояния сокращается (кривая 2). В некоторых случаях скорость полимеризации резко возрастает, но затем уменьшается до постоянного значения (кривая 3). Причиной этого может быть течение процесса на различных активных центрах, в том числе и растворимых; часть этих и других типов центров быстро исчерпывается, и скорость принимает значение, характерное для обычного гетерогенного процесса. Иногда наблюдается уменьшение скорости после достижения ею постоянного значения (кривая 4): это может быть следствием начинающегося разложения катализатора в случае полимеризации.
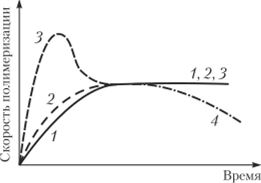
Рис. 3.21. Типичные кинетические кривые полимеризации на гетерогенных системах Циглера — Натта.
при повышенной температуре или диффузионных ограничений (замедленное проникновение молекул мономера к активным центрам через слой уже образовавшегося полимера).
При построении кинетических моделей полимеризации на гетерогенных каталитических системах обычно используют допущения относительно механизма взаимодействия активных центров поверхности с мономером. В наиболее простой модели полагают, что концентрация активных центров не зависит от числа молекул металлалкила и мономера, адсорбированных поверхностью катализатора, а полимер образуется при взаимодействии активных центров с мономером из объема реакционной смеси. В этом случае при достаточно высокой концентрации активных центров скорость роста определяют, но уравнению.

где kp — константа скорости роста цепи; [М] — концентрация мономера в объеме; |С]0 — концентрация активных центров на поверхности катализатора.
При условии что концентрация активных центров на поверхности зависит от количества адсорбированного металлалкила и рост цепи происходит с участием адсорбированного мономера, скорость реакции роста цепи равна.

где (2м и (2л — доли поверхности катализатора, занятые адсорбированным мономером и металлалкилом соответственно; S — общая поверхность катализатора.
Адсорбция мономера и металлалкила описывается законом Лэнгмюра — Хиншельвуда.
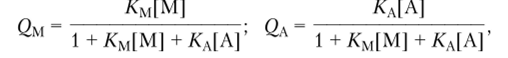
где /См и КА — константы адсорбционного равновесия.
Однако экспериментальные данные по полимеризации олефинов более удовлетворительно описываются выражением.

Среднечисловая степень полимеризации за время t выражается уравнением 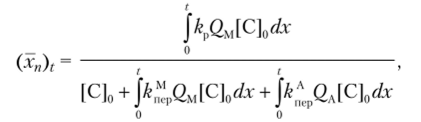
где /е"рр и &", р — константы передачи цепи на мономер и металлалкил соответственно.
Например, при полимеризации этилена на системе (С2Н5)2А1С1 + + TiC1.3 при 40 °C концентрация активных центров составляет 10-2 мольДмоль TiCl3), kp — 80 лДмоль-с), kQ — 0,3 лДмоль-с),.
^"ер ~ 1 • 10 '2 лДмОЛЬ • с), k"ep ~ 3 Л/(МОЛЬ? С). ТаКИМ обрЭЗОМ, ЧИСЛО растущих центров составляет лишь 0,1 —1,0% от общего количества атомов переходного металла. Процесс близок к полимеризации по типу «живущих» цепей — время жизни растущих цепей может достигать нескольких часов (в случае гомогенных катализаторов — 5—10 мин).
Образующиеся на гетерогенных каталитических системах полимеры, как правило, характеризуются широким ММР: для полиэтилена отношение Мю/Мп достигает 5—20, а для полипропилена — 5—15. Очень широкое ММР свидетельствует не только о процессах ограничения цепей, но и о различной реакционной способности активных центров. Так, было показано, что в процессе полимеризации этилена на системе (С2Н5)2А1С1—TiCI^ цепи, выросшие на центрах с атомом TiIV, значительно короче сформированных на Т1ш-центрах.
Полимеризация под действием я-аллильных комплексов переходных металлов. Рассмотренные выше катализаторы ионнокоординационной полимеризации характеризуются крайне нестабильной ст-связью «переходный металл — углерод» (Ti-C, см. уравнение (3.147)). В качестве катализаторов ионной полимеризации можно использовать и л-комплексы, в которых л-связь «металл — углерод» не является очень прочной: я-аллильные и л-кротильные производные Ni, Со, Сг (возможно, в комбинации с галогенидами металлов — AlCl3, TiCl/" VC13). Строение л-аллильных комплексов общей формулы f (CH2=CHCH2)MtX]2 (X — галоген, Mt — Ni, Со) следующее:
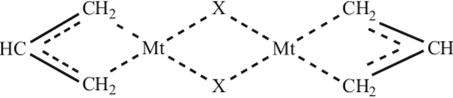
л-Аллильные комплексы переходных металлов получили наибольшее распространение для полимеризации диенов; по строению эти комплексы моделируют структуру активного центра растущей цепи (на примере полимеризации бутадиена):
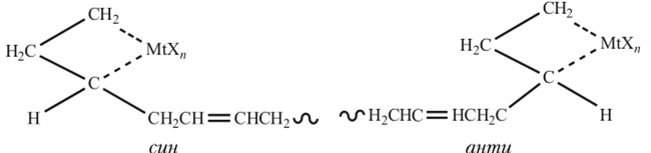
причем здесь возможно различное расположение цепи относительно комплекса: стш-конфигурация приводит к формированию 1,4-транс-последовательности звеньев, а «//тм-конфигурация — к 1,4−1<�мс-чередованию звеньев.
Механизм полимеризации под действием л-алл ильных комплексов представляет собой последовательность актов координации мономера на комплексе, образования a-связи и вхождение мономера в цепь с регенерацией л-аллильного комплекса:
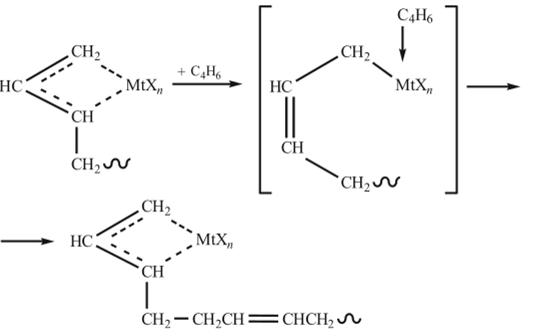
Если координация диена с атомом металла происходит по обеим двойным связям, то формируется цис-конфигурация цепи, если, но одной — то преимущественно реализуется термодинамически более выгодная транс-форма. Существенное влияние на строение цепи полидиена оказывает и природа лиганда X в комплексе. Ниже приведено содержание цис- и транс-звеньев в нолибутадиене, синтезированном на л-аллилникельгалогенидах (CH2=CHCH2NiX)2 в растворе в бензоле в зависимости от лиганда:
- • для лиганда хлора (С1) содержание 1,4-^ис-звеньев составляет 89%; 1,4-транс-звеньев — 7%; 1,2-звеньев — 4%;
- • для лиганда брома (Вг) содержание 1,4-г<�мс-звеньев составляет 46%; 1,4-траис-звеньев — 53%; 1,2-звеньсв — 1%;
- • для лиганда йода (I) 1,4-цис-звенья отсутствуют; содержание 1,4-трянс-звеньев составляет 97%; 1,2-звеньев — 3%.
Ионно-координациоиная полимеризация полярных мономеров. Полярные группы мономеров, полимеризующихся по ионнокоординационному механизму, способны легко вступать во взаимодействие со связью «С — переходный металл» или с металлорганическим соединением, разрушая их. Кроме того, функциональные группы полярных мономеров могут образовывать прочные комплексы с координационно-ненасыщенными производными переходных металлов, а это препятствует координации на них мономеров по связи С=С.
Полимеризация полярных мономеров происходит при устранении возможности образования указанных прочных комплексов путем экранирования полярных ipynn или существенного понижения их донорской активности. Мономеры типа CH2=CH (CH2)"XSiMe3 или CH2=CH-(CH2)"NR2 (R — СН (СН3)2; X — О, NH; п = 29) эффективно полимеризуются под действием титан-алюминиевых комплексов с образованием высокомолекулярных изотактических полимеров. Триметилсилильные ненасыщенные мономеры представляют собой соединения с пониженной электронодонорностью атомов О или N за счет сопряжения их электронов с вакантными (/-орбиталями атома кремния. Указанное взаимодействие устраняет или существенно затрудняет комплексообразование с катализатором за счет полярных групп, и эти мономеры полимеризуются как обычные а-олефины. Имеются сведения о полимеризации иод действием инициаторов на основе переходных металлов таких полярных мономеров, как метилметакрилат, акрилонитрил, хотя природу этих реакций нельзя считать полностью выявленной; полагают, что процесс идет по анионному механизму.