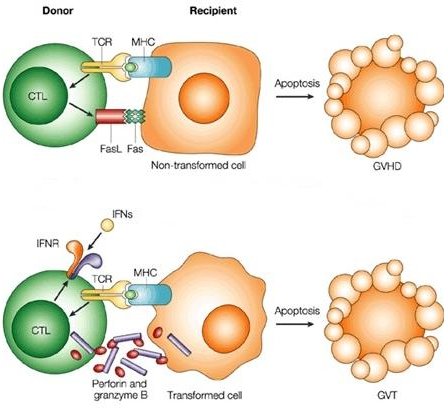
Современное представление о механизмах РТПХ (трансплантат против хозяина)

Антигенпредставляющие (дендритные) клетки при аллергических реакциях Дендритные клетки, клетки Лангерганса, моноциты и макрофаги играют важную роль в аллергическом воспалении, так как представляют аллергены Т-лимфоцитам и способствуют накоплению эффекторных клеток в очагах воспаления. Антигенпрезентирующие клетки (АПК) — это разнородная группа клеток, объединенных общей способностью представлять… Читать ещё >
Современное представление о механизмах РТПХ (трансплантат против хозяина) (реферат, курсовая, диплом, контрольная)
Т-лимфоциты донора при попадании в организм больного с нарушенным иммунитетом (вследствие врожденных причин, облучения или химиотерапии) могут активироваться HLA реципиента и индуцировать реакцию трансплантат против хозяина (РТПХ). Гибель клеток реципиента обусловлена цитотоксической активностью клеток донора (например, NK-клеток) и действием лимфокинов (например, ФНО), выделяемых активированными лимфоцитами. Необходимые условия развития РТПХ включают присутствие компетентных клеток в трансплантате, ослабление иммунитета реципиента и отсутствие реакции против трансплантата, HLA которого отличаются от таковых реципиента. Различают острую (развивающуюся не позднее, чем через 100 дней после трансплантации кроветворных стволовых клеток (ТКСК)) и хроническую (более позднюю) реакцию трансплантат против хозяина (РТПХ). При этом может возникать эффект «трансплантат против опухоли», снижающий риск рецидива при лейкозе. В случаях злокачественных заболеваний рассчитывают именно на такой эффект РТПХ, что позволяет использовать низкодозовые (немиелоаблативные) режимы кондиционирования. Достаточная для приживления донорских клеток иммуносупрессия обеспечивает возможность уничтожения клеток опухоли. РТПХ отражает потерю «толерантности», которая в норме обусловлена элиминацией аллореактивных лимфоцитов в тимусе, модуляцией рецепторов Т-клеток, анергией аллореактивных клеток и Т-супрессорами. Острая реакция трансплантат против хозяина (РТПХ) возникает вследствие выделения воспалительных цитокинов (ИФН, ИЛ, ФНО) клетками реципиента, поврежденными предшествующими воздействиями (режимом кондиционирования). АПК реципиента представляют измененные собственные антигены донорским Т-лимфоцитам в богатой цитокинами среде, что приводит к активации и пролиферации донорских Т-клеток. Активированные CD4 и CD8 донорские Т-лимфоциты выделяют дополнительное количество цитокинов («цитокиновая буря»), в результате активируются цитотоксические Т-лимфоциты и NK-клетки, вызывающие гибель клеток и тканей реципиента. Клинически острая реакция трансплантат против хозяина (РТПХ) характеризуется эритродермией, внутрипеченочным холестазом и энтеритом. В типичных случаях сразу же после трансплантации кроветворных стволовых клеток (ТКСК) возникает зудящая пятнисто-папулезная сыпь на ушах, ладонях и ступнях. В дальнейшем она может распространяться на туловище и конечности, становясь сливной, буллезной и эксфолиативной.
Лихорадка возникает не всегда. Острую РТПХ следует отличать от токсических проявлений режимов кондиционирования, лекарственной сыпи, а также вирусных и иных инфекционных экзантем. Нарушения функции печени проявляются холестатической желтухой с повышением уровня печеночных ферментов в крови. Дифференциальную диагностику проводят с гепатитом, веноокклюзивной болезнью печени или лекарственными эффектами. Кишечные симптомы острой РТПХ (схваткообразная боль в животе и понос, часто с примесью крови) сходны с симптомами, связанными с режимом кондиционирования или инфекцией.
Могут иметь место эозинофилия, лимфоцитоз, энтеропатия с потерей белка, аплазия костного мозга (нейтропения, тромбоцитопения, анемия). Развитию острой реакции трансплантат против хозяина (РТПХ) способствуют различия донора и реципиента по HLA, неправильный подбор донора по полу и возрасту, наличие родов в анамнезе донора, проведение ТКСК в активной фазе или при рецидиве лейкоза, а также чересчур высокие дозы облучения реципиента. Для профилактики и лечения РТПХ применяют различные иммуносупрессивные средства. РТПХ может возникать после переливания компонентов крови больным с относительно подавленным иммунитетом, включая перенесших ТКСК или иммуносупрессивную противораковую терапию, ВИЧ-инфицированных, страдающих врожденным иммунодефицитом и недоношенных детей. Поэтому переливаемую кровь в таких случаях необходимо предварительно облучать (25−50 Гр), бесклеточные компоненты крови (свежезамороженная плазма или криопреципитат) не требуют облучения.
Приживление трансплантата может сопровождаться хронической РТПХ. Обычно она развивается через 100 дней после трансплантации, но иногда и на 60-й день. Вероятность развития хронической реакции трансплантат против хозяина (РТПХ) после трансплантации кроветворных стволовых клеток (ТКСК) от HLA-идентичных сибсов составляет 24%, а после неродственной ТКСК — 37%.
Патогенез хронической РТПХ недостаточно выяснен, но, по-видимому, в нем принимают участие аллореактивные донорские Т-лимфоциты вместе с предшественниками Т-лимфоцитов реципиента, которые из-за аберрантной селекции в тимусе остались аутореактивными.
Хроническая реакция трансплантат против хозяина (РТПХ) напоминает мультисистемные аутоиммунные заболевания, имитируя отдельные проявления синдрома Шегрена (сухость глаз и слизистой оболочки полости рта), СКВ и склеродермии, красного плоского лишая, облитерирующего бронхиолита и первичного билиарного цирроза печени. Часто возникают инфекции (сепсис, синуситы, пневмонии), вызываемые инкапсулированными бактериями, грибами и вирусами. Это во многом определяет связанные с трансплантацией кроветворных стволовых клеток (ТКСК) заболеваемость и смертность. Профилактическое введение триметоприм/сульфаметаксазола снижает частоту пневмонии, вызываемой Pneumocystis carinii. Риск хронической реакции трансплантат против хозяина (РТПХ) возрастает с увеличением возраста донора или реципиента, после острой реакции трансплантат против хозяина (РТПХ), при введении донорских лимфоцитов, а также при использовании клеток от многорожавших доноров. В лечении хронической реакции трансплантат против хозяина (РТПХ) дополнительно используют иммуносупрессивные средства, главным образом преднизон и циклоспорин, что, в свою очередь, способствует развитию инфекционных заболеваний. Обширные поражения кожи, тромбоцитопения (число тромбоцитов менее 100 000 в 1 мкл) и быстрое развитие реакции значительно ухудшают прогноз. Для профилактики и лечения отторжения аллотрансплантатов и реакции трансплантат против хозяина (РТПХ) используют иммунносупрессивные средства. Поскольку отторжение аллотрансплантата обусловлено активацией Т-лимфоцитов реципиента (вследствие отличия его HLA от антигенов донора), без иммуносупрессии можно обойтись лишь при трансплантации тканей от однояйцовых близнецов, а также при некоторых тяжелых иммунодефицитах у реципиента. Трансплантация внутренних органов требует пожизненной иммуносупрессии, тогда как реципиенты стволовых клеток должны получать иммунодепрессанты в течение 6−12 мес., пока не произойдет приживление аллотрансплантата. Специальный отбор стволовых клеток и Т-лимфоцитов донора исключает реакцию трансплантат против хозяина (РТПХ) и позволяет применять более мощные иммунодепрессанты, а это, в свою очередь, делает возможным трансплантацию от менее совместимых доноров.
Идеальный иммунодепрессант должен подавлять активность не только лимфоцитов реципиента, обусловливающих отторжение, но и лимфоцитов донора, от которых зависит развитие реакции трансплантат против хозяина (РТПХ). В то же время он не должен нарушать иммунные реакции против инфекционных агентов и опухолевых клеток (т. е., реакцию «трансплантат против опухоли»).
При разных заболеваниях используют различные режимы подготовки (кондиционирования) больных к трансплантации кроветворных стволовых клеток. Большинство применяемых средств обладает не только иммуносупрессивной, но и противоопухолевой активностью. Чаще всего используют циклофосфамид (и его изомер ифосфамид) — производное хлорметина, которое требует метаболической активации для превращения в бифункциональный алкилирующий метаболит.
Широко применяется также тотальное облучение, которое обладает мощной противоопухолевой и иммуносупрессивной активностью и воздействует на все ткани. С тотальным облучением сочетают средства, противоопухолевая активность которых превышает иммуносупрессивную: бусульфан, этопозид, мелфалан, кармустин, цитарабин, тиоТЭФ и карбоплатин. Такое сочетание обеспечивает достаточную иммуносупрессию для быстрого приживления трансплантата, позволяя избежать чрезмерной токсичности и сохраняя возможность элиминации злокачественного клона. При использовании меньших доз этих агентов в сочетании с флударабином трансплантат также приживляется в 90−100% случаев, но часто развивается РТПХ. Все еще неясно, дает ли реакция — «трансплантат против опухоли» те же результаты, что и стандартная высокодозовая химиотерапия.
Немиелоаблативные режимы наиболее эффективны, по-видимому, при незлокачественных заболеваниях, при которых достаточно присутствие нормальных донорских клеток (трансплантата).
Снижение числа Т-лимфоцитов перед трансплантацией стволовых клеток. Для профилактики отторжения трансплантата и реакции трансплантат против хозяина (РТПХ), как и для лечения реакции трансплантат против хозяина (РТПХ), используют разные подходы. Поскольку в развитии РТПХ участвуют донорские Т-лимфоциты, трансплантат лишают этих клеток с помощью моноклональных антител или физических методов (например, агглютинация соевым лектином). Это приводит к резкому снижению частоты РТПХ, но одновременно возрастает вероятность отторжения трансплантата и рецидива заболевания, так как донорские Т-лимфоциты играют важнейшую роль в элиминации оставшихся Т-лимфоцитов реципиента и в реакции «трансплантат против опухоли».
Изучаются и другие подходы (например, добавление отдельных субпопуляций Т-лимфоцитов), которые могли бы способствовать приживлению трансплантата и сохранять его противоопухолевую активность, но в то же время предотвращать РТПХ.
Метотрексат — конкурентный ингибитор дигидрофолатредуктазы обладает не только противораковым, но и мощным иммуносупрессивным действием.
Введение
метотрексата на 1, 3, 6 и 11-й день после трансплантации надежно предотвращает РТПХ, еще более эффективно его сочетание с циклоспорином. Метотрексат может усиливать воспаление слизистых оболочек, возникающее в период подготовки к трансплантации, а больным с нарушенной функцией почек или отеками (например, плевральным выпотом) приходится одновременно назначать фолинат кальция. При выраженной почечной недостаточности можно использовать структурно сходный с метотрексатом другой антагонист фолиевой кислоты — триметрексат, который элиминируется печенью.
Циклоспорин — это липофильный (гидрофобный) циклический пептид, состоящий из 11 аминокислотных остатков и обладающий мощным и специфическим иммуносупрессивным свойством. Он блокирует активацию Т-лимфоцитов, нарушая синтез ИЛ-2 на уровне транскрипции. Циклоспорин ингибирует также синтез ИЛ-1, ИЛ-3 и ИФН-у. В высоких дозах он препятствует формированию рецептора ИЛ-2, и хотя его миелосупрессивный и противовоспалительный эффекты ограничены действием на Т-лимфоциты, этот препарат весьма эффективно предотвращает отторжение трансплантата. Циклоспорин разрушается печеночной ферментной системой цитохрома Р450, и его уровень в крови зависит от присутствия других лекарственных средств. Кетоконазол, эритромицин, варфарин, верапамил, этанол, имипенем с циластатином, метоклопрамид, итраконазол и флуконазол повышают уровень циклоспорина, а фенитоин, фенобарбитал, карбамазепин, вальпроат натрия, нафциллин, октреотид, триметоприм и рифампицин снижают. Помимо иммуносупрессивного циклоспорин обладает множеством побочных эффектов: он действует на нервную систему, вызывая тремор, парестезии, головную боль, спутанность сознания, сонливость, судороги и кому. Кроме того, он вызывает гипертрихоз, гипертрофию десен, анорексию, тошноту и рвоту. Нарушения функции печени проявляются холестазом, желчнокаменной болезнью и геморрагическим некрозом, дисфункция эндокринной системы — кетозом, гиперпролактинемией, повышением уровня тестостерона, гинекомастией, нарушением сперматогенеза. Действие циклоспорина сопровождается гипомагниемией, гиперурикемией, гипергликемией, гиперкалиемией, гипохолестеринемией, артериальной гипертонией, активацией симпатической нервной системы, поражением мелких сосудов (напоминающим гемолитико-уремический синдром), ускорением атерогенеза. Применение циклоспорина в большой мере ограничивается его нефротоксическими эффектами — повышением уровня креатинина, олигурией, почечной гипертонией, задержкой жидкости, снижением скорости клубочковой секреции (из-за сужения афферентных артериол), повреждением почечных канальцев и мелких сосудов почек. Развитие интерстициального фиброза и атрофии почечных канальцев часто требует снижения дозы циклоспорина или замены его другими иммунодепрессантами. Аминогликозиды, амфотерицин В, ацикловир, дигоксин, фуросемид, индометацин и триметоприм усиливают нефротоксические эффекты циклоспорина. Эти реакции можно ослабить, подобрав дозы, поддерживающие определенный уровень препарата в крови. Его уровень зависит также от всасывания в ЖКТ, на что влияют понос, кишечные расстройства (вследствие РТПХ, вирусных инфекций или лечебных мероприятий) и нарушение печеночных функций.
Несмотря на липофильность циклоспорина, ожирение не сказывается на его распределении в организме и дозы следует назначать, исходя из идеальной массы тела больного. Иммуносупрессивная активность циклоспорина после трансплантации кроветворных стволовых клеток (ТКСК) не уступает таковой метотрексата, и сочетание обоих средств дает лучший эффект, чем каждое из них в отдельности. Такролимус. Такролимус представляет собой макролид с иммуносупрессивной активностью, продуцируемый грибами Streptomyces tsukubaensis. По химической структуре он отличается от циклоспорина, но действует на иммунную систему аналогичным образом. Несмотря на связывание специфическими белками, такролимус влияет на экспрессию ИЛ-2 и его рецептора точно так же, как Циклоспорин. Некоторое преимущество такролимуса связано с его накоплением в печени и более активным подавлением печеночных проявлений реакция трансплантат против хозяина (РТПХ).
Побочные эффекты и лекарственные взаимодействия такролимуса также сходны с таковыми Циклоспорина. Каждое из этих веществ усиливает токсичность другого. Кортикостероиды. Для лечения или профилактики реакции трансплантат против хозяина (РТПХ) и предотвращения отторжения часто используют преднизон, обычно в сочетании с другими иммунодепрессантами. Кортикостероиды индуцируют синтез растворимого антагониста рецепторов интерлейкинов и тем самым препятствуют активации и пролиферации Т-лимфоцитов под действием ИЛ-1 и ИЛ-6. Поскольку секреция ИЛ-2 отчасти зависит от ИЛ-1 и ИЛ-6, кортикостероиды опосредованно блокируют эффекты и этого интерлейкина. Стимулируя продукцию ингибитора фосфолипазы А2 липокортина, кортикостероиды угнетают образование воспалительных простагландинов и ускоряют противовоспалительные реакции. Кроме того, они разрушают небольшие группы активированных лимфоцитов и тормозят миграцию моноцитов в очаги воспаления. Неспецифические иммуносупрессивные эффекты кортикостероидов (равно как и других иммунодепрессантов) значительно повышают риск оппортунистических инфекций у больного. Длительное применение этих соединений чревато замедлением роста, изменением внешности (кушингоидный облик), артериальной гипертонией, катарактой, желудочно-кишечными кровотечениями, панкреатитом, психозами, гипергликемией, остеопорозом, асептическим некрозом головки бедра. Антитела. Антитимоцитпарный иммуноглобулин — это препарат гетерологичных антител к тимоцитам человека, получаемых из сыворотки лошадей, кроликов и других животных. Эти антитела обладают мощным иммуносупрессивным свойством и используются как в подготовке больных к трансплантации, так и в лечении резистентной РТПХ. Побочные эффекты антитимоцитарного иммуноглобулина включают лихорадку, снижение АД, крапивницу, тахикардию, одышку, озноб, миалгию и сывороточную болезнь. Возможно развитие анафилактического шока. Для ослабления этих эффектов применяют дифенгидрамин, ацетаминофен и гидрокортизон. Отдельно или в сочетании с цитотоксическими средствами используют и другие антитела, например к CD33 (гемтузумаб озогамицин) или к CD20 (ритуксимаб).
Они действуют не только на клетки иммунной системы, но и на опухолевые клетки, экспрессирующие эти белки. При рецидивах РТПХ препараты таких антител обеспечивали полную ремиссию. В настоящее время их применяют в сочетании с обычными средствами подготовки больных к трансплантации. Ритуксимаб — препарат выбора при пост трансплантационной лимфопролиферативной болезни, вызванной вирусом Эпштейна-Барр. В лечении рефрактерной РТПХ могут оказаться полезными и антитела к цитокинам (ФНО, ИЛ-1, ИФН-у), блокирующие цитокиновый каскад. Применявшийся вначале как седативное средство, талидомид прошел первые две фазы клинических испытаний на больных с хронической рефрактерной РТПХ или с высоким риском развития этой реакции. В первом случае он оказался эффективным в 59% наблюдений (общая выживаемость 76%), а во втором — в 48%. В III фазе клинических испытаний выявилась плохая переносимость высоких доз препарата, потребовавшая их снижения. Профилактический эффект отсутствовал. С ростом числа и выживаемости детей, перенесших трансплантацию кроветворных стволовых клеток (ТКСК) по различным показаниям, все большее значение приобретают отделенные последствия трансплантации кроветворных стволовых клеток (ТКСК), которые сказываются на здоровье и качестве жизни. Эти последствия включают задержку роста и развития, нарушение нейроэндокринных и репродуктивных функций, вторичные опухоли, хроническую РТПХ, катаракты, лейкоэнцефалопатию и дисфункцию иммунной системы. Нервная система после трансплантации кроветворных стволовых клеток (ТКСК). В нарушении функций нервной системы после трансплантации кроветворных стволовых клеток (ТКСК) могут играть роль инфекции, печеночная энцефалопатия, а также лекарственные средства и облучение. Циклоспорин может вызывать головную боль, которая обычно купируется пропранололом, а также тремор, спутанность сознания, нарушения зрения, судороги и явную энцефалопатию. После отмены препарата большинство этих нарушений исчезает. Клинический синдром лейкоэнцефалопатии характеризуется сонливостью, нарушением речи, атаксией, судорогами, спутанностью сознания, дисфагией и децеребрационной ригидностью. Симптомы могут быть минимальными, но наиболее тяжелая форма лейкоэнцефалопатии приводит к коме и смерти. При МРТ и КТ выявляют множественные участки дегенерации и некроза белого вещества мозга. Лейкоэнцефалопатия наблюдается почти исключительно у больных, которым перед трансплантацией проводили интратекальную химиотерапию или облучение черепа. Среди этих больных это осложнение развивается в 7% случаев. Частота катаракт после однократного тотального облучения (в дозе 8−10 Гр) составляет примерно 80%, после фракционированного облучения — 20−50%, а после одной только химиотерапии — 20%. Хроническая РТПХ часто сопровождается сухим конъюнктивитом. В этих случаях применяют искусственные слезы или другие увлажняющие глаза средства.
Вторичные злокачественные опухоли после трансплантации кроветворных стволовых клеток (ТКСК). Риск вторичных форм рака в 6−8 раз выше, чем в популяции. Наибольшее число случаев наблюдается в течение первого года после трансплантации. Примерно 50% вторичных опухолей, развивающихся в эти сроки, составляют неходжкинские лимфомы, причем в 2/3 из них обнаруживается вирус Эпштей-на-Барр.
Из 3182 больных лейкозом детей, перенесших ТКСК в 1964;1992 гг., солидные опухоли развились у 25, тогда как среди такого же числа детей в общей популяции можно ожидать лишь один случай. 14 из 25 опухолей (n = 14) локализовались в щитовидной железе и головном мозге. К факторам риска вторичного рака относятся иммунодефициты, использование антитимоцитарного иммуноглобулина, трансплантация лишенного Т-лимфоцитов костного мозга, молодой возраст больных в момент трансплантации и предварительное тотальное облучение. Индуцированные вирусом Эпштейна-Барр В-клеточные лимфомы характеризуются агрессивным течением и резистентностью к большинству лечебных мероприятий. В этих случаях эффективными оказываются инфузии донорских Т-лимфоцитов или антител к CD20.
Рост и половое созревание детей после трансплантации стволовых клеток Женщина в свои 48 лет выглядит, как девочка! Вот ее хитрость: на ночь… Паразиты выйдут сами, если с утра натощак съедать 1 ложку… Этот домашний способ уничтожит все морщины на лице, необходимо раз в день Найдено самое мощное средство от морщин! Все морщины разгладятся за месяц, если… Длительные наблюдения за детьми, перенесшими перед трансплантацией тотальное облучение, обнаруживают значительную задержку роста и снижение уровня гормона роста, что может отражаться на окончательном росте больного. Через 8 лет после тотального облучения рост больных был на 2−3 SD ниже нормального среднего показателя для данного возраста. Если проводилось не только тотальное облучение, но и облучение черепа, то рост был уже на 3 SD ниже нормы. Снижение скорости роста отмечено как у мальчиков, так и у девочек. Фракционированное облучение влияет на рост слабее, чем однократное. В первом случае рост оказывается ниже среднего для данного возраста на 1 SD, а во втором — на 2 SD. У облученных детей отсутствовало и пубертатное ускорение роста, что было связано с низким уровнем гормона роста и половых гормонов. Окончательный рост определяется до наступления половой зрелости. У 175 детей, тотально облученных в возрасте до 6 лет, 6−12 и 12−15 лет и не получавших гормон роста, окончательный рост отставал от нормального соответтвенно на 3,49, 1,92 и 0,37 SD. Отставание в росте может быть связано также с хронической РТПХ и ее лечением. В тех случаях, когда дети получали только бусульфан без тотального облучения, рост практически сохранялся, но уровень половых гормонов снижался в той же степени, что и после облучения. Использование перед трансплантацией одного только циклофосфамида (при апластической анемии) почти не влияло на рост и развитие Детей. Замедление роста наблюдалось и при облучении длинных костей и позвоночника при нейробластоме. Лечение рекомбинантным гормоном роста начиная с 12-летнего возраста предотвращало дальнейшее замедление роста, но окончательный рост больных все же оказывался ниже нормы. У всех детей, перенесших трансплантацию кроветворных стволовых клеток (ТКСК), измерять рост следует ежегодно. Современные исследования направлены на выявление дефицита гормона роста у детей раннего возраста с тем, чтобы с помощью заместительной гормональной терапии обеспечить нормальное ускорение роста в период полового созревания. Важную роль при этом играют половые гормоны, которые одновременно стимулируют появление вторичных половых признаков. Запаздывание полового развития отмечается примерно у 75% детей, перенесших перед трансплантацией тотальное облучение. Это связано с первичной недостаточностью гонад. Лабораторные исследования обнаруживают повышенный уровень ФСГ и ЛГ на фоне низкого содержания эстрадиола и тестостерона. Такие больные требуют тщательного наблюдения с ежегодной оценкой стадий полового развития по Таннеру и эндокринных функций. При первичной недостаточности гонад только совместное применение гормона роста и половых гормонов может обеспечить пубертатное ускорение роста.
Щитовидная железа, иммунная система после трансплантации стволовых клеток Тотальное облучение с дополнительным облучением щитовидной железы или без него может стать причиной гипотиреоза. После однократного тотального облучения субклинический гипотиреоз развивается у 28−56% детей, а явный — у 9−13%. При фракционированном облучении частота того и другого значительно меньше (10−14 и менее 5% соответственно). Риск гипотиреоза связан, по-видимому, только с облучением и не зависит от возраста, пола или развития РТПХ у больных. Облучение повреждает именно щитовидную железу, а не гипофиз или гипоталамус. При явном гипотиреозе очень эффективно лечение тироксином, но следует ли лечить компенсированный (субклинический) гипотиреоз, менее очевидно. Риск рака щитовидной железы сохраняется независимо от лечения гипотиреоза. Поскольку гипотиреоз может развиться и через много лет, функцию щитовидной железы следует оценивать ежегодно. При одной только химиотерапии (без облучения) щитовидная железа страдает в гораздо меньшей степени. Восстановление иммунной системы после трансплантации стволовых клеток Химиотерапия перед трансплантации кроветворных стволовых клеток (ТКСК) полностью лишает ребенка Ви Т-клеточного иммунитета. На восстановление функции иммунной системы после трансплантации костного мозга уходит много месяцев и лет. Трансплантированные В-лимфоциты приобретают способность отвечать на митогенную стимуляцию уже через 2−3 мес. Но поскольку продукция антител требует взаимодействия В-лимфоцитов с Т-клетками, уровень IgM достигает нормы лишь через 4−6 мес. после трансплантации, уровень IgG — через 7−9 мес., а уровень IgA может оставаться сниженным целых 2 года. Восстановление числа Т-лимфоцитов также занимает много месяцев. Количество CD8-клеток восстанавливается примерно через 4 мес., но число CD4 Т-лимфоцитов остается низким на протяжении 6−9 мес., и в эти сроки после трансплантации обнаруживается обратное соотношение СD4/СD8-клеток. Трансплантация лишенного Т-лимфоцитов костного мозга, посттрансплантационная иммуносупрессия и хроническая РТПХ удлиняют этот интервал. При хронической РТПХ постоянно снижено число цитотоксических Т-лимфоцитов и Th-клеток, увеличено количество Т-супрессоров. Больным с нарушенным иммунитетом нельзя вводить живые вирусные вакцины. Повторная иммунизация окажется успешной только после достаточного восстановления иммунитета. В отсутствие хронической РТПХ иммунизацию дифтерийным и столбнячным анатоксинами, субъединичным коклюшным компонентом (у детей до 7-летнего возраста), инактивированной вакциной против полиомиелита, гепатита В, а также Haemophilus influenzae типа b и Streptococcus pneumoniae можно проводить лишь через 12 мес. после трансплантации, а вакциной против кори, эпидемического паротита и краснухи — только через 24 мес.
Вакцинацию против гриппа проводят каждую осень. В случаях же хронической РТПХ нужно отложить повторную иммунизацию и до выздоровления вводить IgG. Аллергены. Т-хелперы типа 2 (Th2) при аллергических реакциях. За последние 30 лет значительно увеличилась частота таких аллергических заболеваний, как бронхиальная астма, пищевая аллергия, диффузный нейродермит и аллергический ринит. Термин «аллергия» впервые был предложен фон Пирке в 1906 г. для обозначения «нарушенной реактивности на обычные антигены окружающей среды». С конца 1960;х годов, когда выяснилось, что большинство страдающих аллергией лиц реагируют на антигены продукцией антител класса IgE, термин «аллергия» используется как синоним заболеваний, опосредованных IgE. Это, безусловно, слишком упрощенное понимание механизма развития аллергических заболеваний, так как у определенного числа больных бронхиальной астмой, диффузным нейродермитом и аллергическим ринитом болезнь не связана с IgE, хотя и сопровождается эозинофилией и активацией тучных клеток. Кроме того, в патогенезе которых аллергических заболеваний (например, контактного дерматита) основную роль играют Т-лимфоциты, а реакция IgE вообще отсутствует. К заболеваниям, опосредованным IgE, часто применяют термин атопия (от греч. atopos — без места).
У таких больных имеется наследственная предрасположенность к аллергическим заболеваниям, проявляющаяся повышенной реактивностью ряда органов и тканей (например, легких, кожи, слизистой оболочки полости носа). Важно подчеркнуть, что в механизме этой повышенной реактивности участвуют как связанные с IgE, так и независимые от него компоненты воспаления, которые снижают порог ответа органов-мишеней на воздействие аллергена. Аллергенами называют антигены, вызывающие продукцию IgE-антител у генетически предрасположенных лиц. Большинство аллергенов представляет собой белки с молекулярной массой 10−70 кДа. Белки с меньшей молекулярной массой не связываются с молекулами IgE на поверхности тучных клеток или базофилов, а белки с большей молекулярной массой, как правило, не проникают через слизистые оболочки, не поглощаются АПК и поэтому не стимулируют иммунную систему. Аллергены нередко обладают активностью протеолитических ферментов и, возможно, увеличивая проницаемость слизистых оболочек, приводят к сенсибилизации организма. Многие аллергены, в том числе Der p 1 и Der p 2 из клещей домашней пыли (Dermatophagoides pteronyssinus), Fel d 1 из шерсти кошек, а также аллергены пыльцы деревьев, трав и водорослей (включая Bet v 1 березы, Phl p 1 и РЫ р 5 тимофеевки и Amb a 1, 2, 3 и 5 гигантской амброзии), выделены, их гены клонированы.
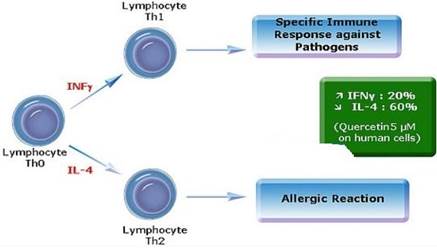
Т-хелперы типа 2 (Th2) при аллергических реакциях.
Действию потенциальных аллергенов подвергаются все люди. У лиц, не имеющих наследственной предрасположенности к аллергическим заболеваниям, в ответ на воздействие аллергенов происходит пролиферация Т-хелперов типа 1 (Тh1), секретирующих цитокины (включая ИФН-у), которые стимулируют продукцию специфических для каждого аллергена IgG-антител. ТЫ, как правило, участвуют в уничтожении внутриклеточных микроорганизмов, таких как микобактерии, поскольку выделяемые этими клетками цитокины активируют фагоциты и способствуют образованию опсонизирующих и комплементфиксирующих антител.
Генетически предрасположенные лица реагируют на аллергены быстрой пролиферацией Th2, которые секретируют цитокины, ускоряющие синтез IgE-антител и участвуют в защите организма от внеклеточных возбудителей, например паразитов. При атопических реакциях образуются аллергенспецифические IgE-антитела. Их присутствие выявляют путем анализа сыворотки или по возникновению аллергической реакции немедленного типа на внутрикожное введение экстракта аллергена. Ключевую роль в переключении синтеза классов иммуноглобулинов на синтез IgE играют продуцируемые Тh2-клетками цитокины — ИЛ-4 и ИЛ-13. ИЛ-5 и ИЛ-9 еще больше усиливают синтез IgE и стимулируют дифференцировку и пролиферацию эозинофилов. ИЛ-3, ИЛ-4 и ИЛ-9 совместно активируют образование тучных клеток. Таким образом, цитокинам Тh2-клетками принадлежит важнейшая роль в патогенезе бронхиальной астмы и других аллергических заболеваний. Действительно, ткани, остро реагирующие на аллергены, оказываются инфильтрированными Тh2-клетками. Интересно, что при хронических аллергических реакциях обычно находят инфильтрацию тканей и Тh1-, и Тh2-клетками. Это важно отметить, поскольку цитокины Тh1-клеток (такие, как ИФН-у) усиливают функцию эффекторных клеток аллергического воспаления (эозинофилов) и тем самым в какой-то мере определяют тяжесть заболевания.
Т-лимфоциты плода принадлежат в основном к Тh2-типу, и это снижает реактивность материнской иммунной системы по отношению к аллоантигенам плода. В норме у ребенка после рождения преобладают Тh1-клетки, которые и опосредуют реакции на аллергены окружающей среды. У детей же с наследственной предрасположенностью к атоническим реакциям продолжает нарастать количество Тh2-клеток, которые во время беременности могли встречаться с материнскими аллергенами вследствие их прохождения через плаценту.
Основным стимулом для реакций, опосредуемых Тh1-клетками, являются микробы. Макрофаги или дендритные клетки (ДК) под влиянием микробных продуктов, таких как эндотоксин, секретируют ИЛ-12 — важнейший активатор Thl-клеток.
Поскольку Thl-клетки тормозят развитие Тh2-клеток, факторы, стимулирующие дифференцировку Th1-клеток, ослабляют аллергические реакции. К таким факторам относятся высокоаффинные взаимодействия Т-лимфоцитов с АПК, большие количества антигена, цитокины Thl-клеток (ИЛ-12 и ИЛ-18) и микробная ДНК, содержащая цитидинфосфат-гуанозиновые повторы. Напротив, цитокины Тh2-клеток (ИЛ-4), простагландин Е2, оксид азота, низкоаффинные взаимодействия Т-лимфоцитов с АПК и небольшие количества антигена способствуют формированию Тh2-фенотипа.
Антигенпредставляющие (дендритные) клетки при аллергических реакциях Дендритные клетки, клетки Лангерганса, моноциты и макрофаги играют важную роль в аллергическом воспалении, так как представляют аллергены Т-лимфоцитам и способствуют накоплению эффекторных клеток в очагах воспаления. Антигенпрезентирующие клетки (АПК) — это разнородная группа клеток, объединенных общей способностью представлять антигены, связанные с молекулами МНС. Среди различных антиген представляющих клеток (АПК) только ДК и клетки Лангерганса способны премировать наивные Т-лимфоциты. Таким образом, именно они ответственны за первичный иммунный ответ, т. е., за сенсибилизационную фазу аллергической реакции. Антиген презентующие клетки (АПК) локализуются преимущественно в лимфоидных органах и коже. Моноциты и макрофаги, вероятно, играют большую роль в активации Т-лимфоцитов памяти и фазе реализации аллергической реакции. Дендритные клетки, расположенные в периферических тканях, таких как кожа, собственная пластинка кишки и легкие, относительно незрелы. Они обладают фагоцитарной активностью, но экспрессируют на поверхности меньше HLA и костимуляторных молекул, чем зрелые АПК. Поглотив антигены, они мигрируют в Т-клеточные области лимфатического узла, дренирующего данный участок ткани. В процессе миграции дендритные клетки претерпевают фенотипические и функциональные изменения: на их поверхности появляется больше HLA I и II классов и костимуляторных молекул, способных взаимодействовать с CD28 Т-лимфоцитов. В лимфатических узлах дендритные клетки непосредственно представляют переработанные антигены Т-лимфоцитам, запуская пролиферацию и дифференцировку последних. В соответствии со способностью индуцировать пролиферацию Тh1- или Тh2-лимфоцитов дендритные клетки подразделяют на ДК1 и ДК2. Основная роль в индукции пролиферации Thl-клеток принадлежит ИЛ-12, который секретируется ДК1. Мощным стимулятором этой секреции является ИФН-у. ДК2 не секретируют ИЛ-12 и поэтому пролиферируют именно Тh22-клетки. Гистамин и простагландин Е2 угнетают продукцию ИЛ-12 и участвуют в формировании ДК2. Особенность атопических реакций заключается в присутствии на поверхности АПК аллерген специфического IgE. Формирование комплекса рецептора I Fc-фрагмента (FceRI) с IgE и аллергеном (FceRI/IgE/аллерген) на поверхности АПК значительно облегчает захват и представление аллергена.
Клиническое значение этого феномена подтверждается тем, что для возникновения экзематозных повреждений от воздушных аллергенов, наносимых на кожу больных диффузным нейродермитом, необходимо присутствие FceRI-позитивных клеток Лангерганса, несущих на поверхности молекулы IgE. Роль низкоаффинного рецептора II Fc-фрагмента IgE (FceRII, CD23) на моноцитах-макрофагах менее ясна, хотя при некоторых условиях он, по-видимому, также облегчает захват антигена. Перекрестное связывание этого рецептора, как и FceRI, на моноцитах-макрофагах способствует выделению медиаторов воспаления.
трансплантация мозг заболевание.