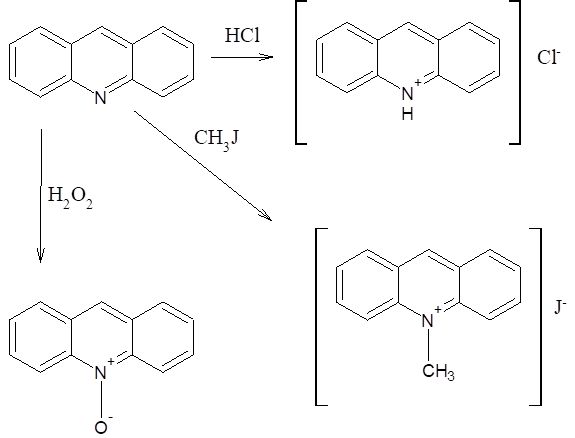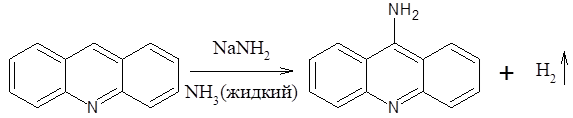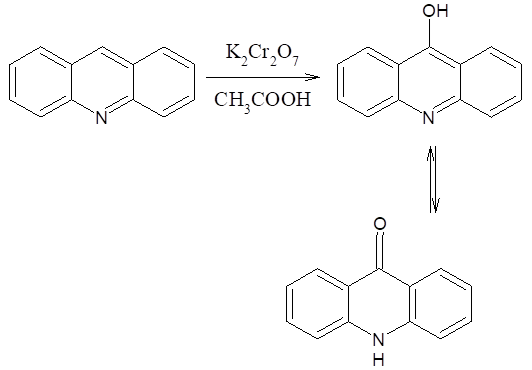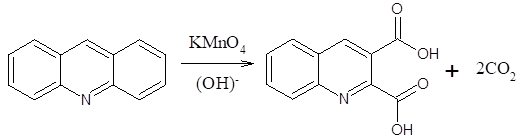Реакции с участием гетероатома. Акридин является слабым основанием. Он обладает более слабыми основными свойствами, чем пиридин и хинолин.
Акридин, подобно пиридину, взаимодействуя с кислотами, образует соли, которые называются акридиниевыми. С надкислотами образует N-оксид акридина:
Схема 5.
С электрофильными реагентами акридин взаимодействует с большим трудом и неоднозначно.
Реакции нуклеофильного замещения для акридина идут достаточно легко по положению 9. Например, при действии на акридин амида натрия образуется 9-аминоакридин (схема 6):
Схема 6.
Акридин достаточно устойчив к действию окислителей.
При действии дихромата калия в уксусной кислоте акридин окисляется в акридон-9, который является таутомерным веществом:
Схема 7.
Хотя в акрилоне-9 и содержится группа С=О, однако она не обладает кетонным характером. Это объясняется тем, что необобщенная электронная пара атома азота сопряжена с карбонилом, что снижает ее электрофильные свойства.
Молекулы акридона-9 благодаря межмолекулярным водородным связям образуют димеры. Акридон-9 в свободном состоянии представляет собой димер с высокой температурой плавления (схема 8):
Схема 8.
При окислении акридина в жестких условиях (КМnO4 в щелочной среде) затрагивается одно из бензольных ядер с образованием хинолин-2,3-дикарбоновой кислоты (схема 9):
Схема 9.
Восстановление акридина происходит подобно антрацену по наиболее активным мезо-положениям. Так, при действии натрия в спиртовом растворе или при каталитическом гидрировании акридин легко восстанавливается в 9,10-дигидроакридин (акридан) (схема 10):
Схема 10.
Акридан обладает очень слабыми основными свойствами. Так же, как и у дифениламина, неподеленная электронная пара атома азота участвует в сопряжении с р-электронами бензольных колец. Только с сильными кислотами он образует соли, которые легко гидролизуются.