Фармакотерапия тромбозов.
Клиническая фармакология

Активация фактора Хагемана (фактор XII в каскаде свертывания крови) приводит к формированию фибрина путем активации внутреннего каскада свертывания крови. Тканевые тромбопластины, высвобождающиеся при повреждении, активируют внешний каскад свертывания крови, что приводит к образованию фибрина. Фактор XIII воздействует на фибрин и вызывает образование нерастворимого фибриллярного полимера, который… Читать ещё >
Фармакотерапия тромбозов. Клиническая фармакология (реферат, курсовая, диплом, контрольная)
Коагулограмма — один из видов анализа крови. Его проводят с целью изучения ее свертывающей способности. Оценка эффективности функционирования этого механизма очень важна в случае, если пациенту предстоит потеря крови, например при родах или в ходе оперативного вмешательства. Исследование процесса свертывания крови (гемостаза) необходимо и в период беременности, после проведения операции, а также при обнаружении заболеваний печени, сосудов, патологий иммунной системы. Тромбоз отличается от свертывания крови, однако это различие несколько условно, поскольку и в том, и другом случае запускается каскадная реакция свертывания крови. Тромб всегда прикреплен к эндотелию и составлен из слоев связанных между собой тромбоцитов, нитей фибрина и форменных элементов крови, а кровяной сверток содержит беспорядочно ориентированные нити фибрина с расположенными между ними тромбоцитами и эритроцитами.
В нормальном состоянии существует топкий и динамический баланс между формированием свертка крови и его растворением (фибринолизом). Схема механизма нормального гемостаза представлена на рис. 5.3.
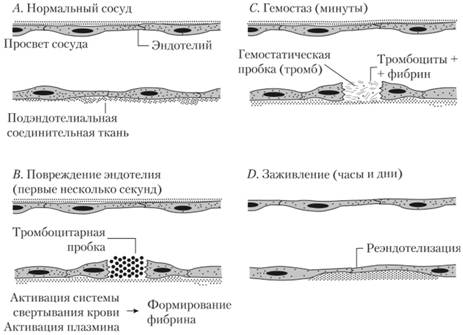
Рис. 5.3. Схема механизма нормального гемостаза:
А — в нормальном, неповрежденном сосуде подэндотелиальная соединительная ткань, особенно коллаген и эластин, отделены от кровотока; В — первые несколько секунд после повреждения тромбоциты адгезируются и агрегируются на подэндотелиальной ткани. Эндотелиальное повреждение приводит также к активации фактора Хагемана (XII фактор), что приводит к активации внутреннего пути свертывания крови. Высвобождение тканевых тромбопластинов активирует и внешний путь; С — гемостаз происходит в течении нескольких минут. Фибрин и тромбоциты формируют гемостатическую пробку (тромб). Плазмин (фибринолизин) препятствует избыточному тромбообразованию; D — при заживлении происходит ретракция сгустка, его организация и фиброз; последним этапом является реэндотелизация При травме сосуда (наиболее частый фактор, приводящий к формированию тромба) происходит повреждение эндотелия, что сопровождается формированием гемостатической тромбоцитарной пробки и активацией систем свертывания и фибринолиза.
Образованию фибринового тромба предшествует каскад протеолитических реакций, приводящий к активации фермента тромбина, который и превращает фибриноген в фибрин. Все белки, участвующие в свертывании крови, называют факторами свертывания. Они синтезируются в основном в печени и клетках крови в виде неактивных предшественников, обозначаются римскими цифрами, но имеют и индивидуальные названия. Большинство этих белков активируется в каскаде ферментативных реакций свертывания крови. Схема этапов свертывания крови представлена на рис. 5.4.
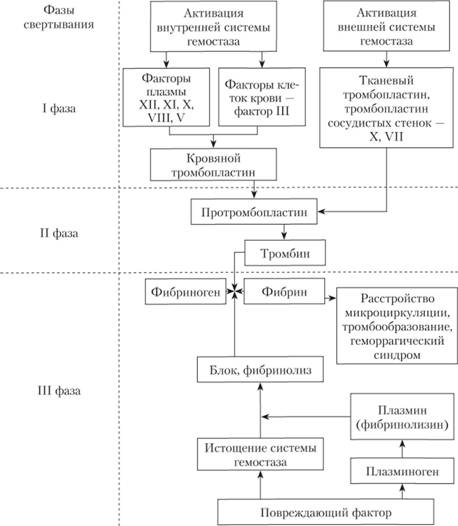
Рис. 5.4. Схема этапов свертывания крови.
При повреждении эндотелия происходит активации системы свертывания, что приводит к формированию тромба. Каскадный процесс свертывания крови представлен на рис. 5.5. Механизм реализуется при наличии на внешней поверхности плазматической мембраны клеток (МВ) тканевого фактора (ТФ) — липидно-белкового комплекса, на котором, как на матриксе, происходит гемокоагуляция.
Коагулограмма — комплексный анализ, имеющий несколько методик проведения, поэтому набор исследуемых показателей неоднозначен. Обычно в него входит определение следующих факторов:
- • время кровотечения (свертывания);
- • протромбиновое время;
- • тромбиновое время;
- • фибриноген;
- • волчаночный антикоагулянт;
- • D-димер;
- • антитромбин III;
- • активированное частичное тромбопластиновос время (АЧТВ).
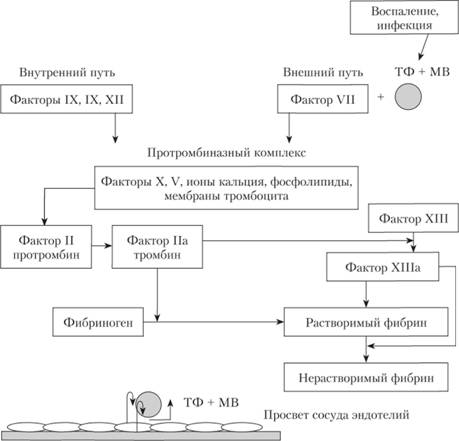
Рис. 5.5. Свертывание крови:
активация фактора Хагемана (фактор XII в каскаде свертывания крови) приводит к формированию фибрина путем активации внутреннего каскада свертывания крови. Тканевые тромбопластины, высвобождающиеся при повреждении, активируют внешний каскад свертывания крови, что приводит к образованию фибрина. Фактор XIII воздействует на фибрин и вызывает образование нерастворимого фибриллярного полимера, который вместе с тромбоцитарной пробкой обеспечивает окончательный гемостаз. При микроскопическом исследовании фибрин имеет фибриллярную сетчатую структуру, окрашивающуюся в розовый цвет, с чередующимися аморфными бледными массами тромбоцитов. ТМ + МВ — взаимодействие тканевого фактора и внешней поверхности плазматической мембраны клеток Главными из показателей коагулограммы являются протромбин и АЧТВ, они присутствуют в каждом анализе. Для исследования используют кровь, взятую натощак из локтевой вены.
Время свертывания определяется методом прокола кожи и последующей фиксации времени остановки кровотечения. В норме оно составляет 2−3 мин. Его увеличение свидетельствует о недостатке в крови тромбоцитов, нарушении их функций, причиной которых могут стать заболевания крови, печени и почек. Протромбиновое время отражает скорость перехода фермента протромбина в активную форму — тромбин. Повышение протромбинового времени отмечают при недостатке в организме витамина К, факторов свертывания крови, также оно возможно при заболеваниях печени.
Активированное частичное тромбопластиновое время — это время, за которое образуется сгусток крови после присоединения к плазме хлорида кальция и других реагентов.
АЧТВ — наиболее чувствительный показатель свертываемости крови. Норма АЧТВ в среднем — 30−40 с.
Повышенное АЧТВ может наблюдаться при болезнях печени, дефиците витамина К, при наличии в крови антикоагулянта. Если уровень хотя бы одного из факторов свертывания снижен на 30−40% от нормы, то меняется и уровень АЧТВ.
Замедление свертываемости крови вследствие увеличения продолжительности АЧТВ — симптом следующих заболеваний:
- • снижение свертываемости крови;
- • гемофилия;
- • ДВС-синдром — синдром диссиминированной внутрисосудистой свертываемости (II и III фаза);
- • антифосфолипидный синдром.
Низкий АЧТВ — симптом I фазы ДВС-синдрома.
Протромбин — сложный белок, один из важнейших показателей коагулограммы, характеризующий состояние свертывающей системы крови. Протромбин или фактор II свертывания крови — это предшественник тромбина (белка, стимулирующего образование тромба). Роль протромбина в свертывании крови отражена на рис. 5.6.
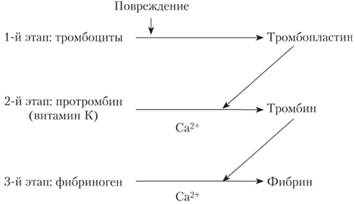
Рис. 5.6. Роль протромбина в свертывании крови.
Протромбин синтезируется в печени при участии витамина К. Уровень протромбина снижается при заболеваниях печени и желудочно-кишечного тракта.
Для характеристики системы гемостаза (свертывающей системы крови) анализ протромбинов крови является наиболее важным тестом.
Нормы протромбина: 78−142% (анализ протромбина крови по Квику).
Результаты анализа крови на протромбин могут быть представлены в различных формах.
- • Протромбиновое время. Отражает время свертывания плазмы крови, выражается в секундах.
- • Протромбин по Квику. Американский врач Арманд Квик в 1935 г. предложил этот тест с целью анализа свертываемости крови по определению уровня протромбина. Анализ отображает активность протромбина в процентах, выявленную по калибровочному графику, построенному в результате измерения протромбинового времени в разведенных растворах нормальной плазмы. На сегодняшний день этот тест — самый популярный метод анализа протромбина.
- • Протромбиновый индекс (или индекс протромбина). Определение индекса протромбина выражает отношение протромбинового времени здорового человека к протромбиновому времени больного. Выражается в процентах.
- • Международное нормализованное отношение (МНО). Протромбиновое время (период, в течение которого в крови успевает образоваться сгусток из-за добавления реактивов) крови пациента делится на время, считающееся нормальным. Потом полученный результат умножается на индекс чувствительности тромбопластина, который указан на упаковке реактива, используемого в лаборатории. В идеале значение МНО должно колебаться от 0,8 до 1,15 ед. Чем выше показатель, тем больше свертываемость. Анализ МНО рекомендован Комитетом экспертов ВОЗ, Международным комитетом, но изучению тромбозов и гемостаза и Международным комитетом, но стандартизации в гематологии для контроля при лечении непрямыми антикоагулянтами. Непрямые антикоагулянты снижают уровень протромбина в крови и замедляют свертывание крови. Антикоагулянты используются в лечении заболеваний, связанных с образованием тромбов в венах, — в лечении тромбофлебита, тромбоза, легочной эмболии, тромбоэмболических осложнений при инфаркте миокарда, коронарной недостаточности. Анализ крови на МНО позволяет врачу отслеживать эффективность воздействия лекарственной терапии при этих заболеваниях.
Повышенный уровень протромбина — симптом следующих заболеваний:
- • тромбоэмболия;
- • инфаркт миокарда, предынфарктное состояние;
- • полицитемия;
- • злокачественные опухоли.
Низкий уровень протромбина в крови дает врачу основание поставить следующий диагноз:
- • врожденный или приобретенный дефицит протромбина;
- • нехватка витамина К.
Тромбиновое время показывает быстроту перехода белка фибриногена в нерастворимую форму (фибрин) под действием тромбина. Увеличение этого временно? го промежутка происходит вследствие дефицита в крови фибриногена, присутствия ингибиторов тромбина и фибриногена, а также гепарина.
Фибриноген — белок, вырабатываемый в печени и превращающийся в нерастворимый фибрин — основу сгустка при свертывании крови. Фибрин впоследствии образует тромб, завершая процесс свертывания крови.
Фибриноген состоит из шести полипептидных цепей: Аа2, В?2 и ?2. А, В — отрицательно заряженные фрагменты, благодаря которым молекулы фибриногена не агрегируют. Д Е — глобулярные домены молекулы фибриногена. Домены отделены участками полипептидных цепей, имеющими стержнеобразную конфигурацию. Мономер фибрина, образующийся из фибриногена, имеет состав (?, ?, ?)2. Строение фибриногена показано на рис. 5.7. Схема трансформации фибриногена в фибрин представлена на рис. 5.8.
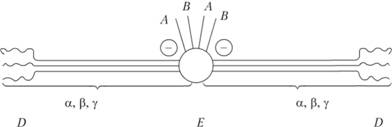
Рис. 5.7. Строение фибриногена.
Фибриноген является ценным показателем гемостаза (коагулограммы). Схема гемостаза приведена на рис. 5.9.
Анализ фибриногена — необходимый этап предоперационного обследования, пренатальной диагностики, проводится при воспалительных, сердечно-сосудистых заболеваниях.
Содержание фибриногена в крови повышается при возникновении острых воспалительных заболеваний и отмирания тканей. Фибриноген влияет и на скорость оседания эритроцитов (СОЭ).
Норма содержания фибриногена: 2−4 г/л.
Норма содержания фибриногена для новорожденных: 1,25−3 г/л.
Нормы содержания фибриногена при беременности несколько выше. В этот период наблюдается постепенное повышение фибриногена и в III триместре беременности уровень фибриногена достигает 6 г/л.
В других случаях повышенный уровень фибриногена в крови человека — симптом следующих заболеваний:
- • острые воспалительные и инфекционные заболевания (грипп, туберкулез);
- • инсульт;
- • инфаркт миокарда;
- • гипотиреоз;
- • амилоидоз;
- • пневмония;
- • злокачественные опухоли (рак легких и др.).
Повышение уровня фибриногена сопровождает ожоги, операционные вмешательства, прием эстрогенов и оральных контрацептивов.
Уровень фибриногена снижается при таких заболеваниях, как:
- • ДВС-синдром;
- • заболевания печени (гепатит, цирроз);
- • токсикоз беременности;
- • недостаток витаминов С и В12;
- • эмболия околоплодными водами (у новорожденных);
- • хронический миелолейкоз;
- • полицитемия.
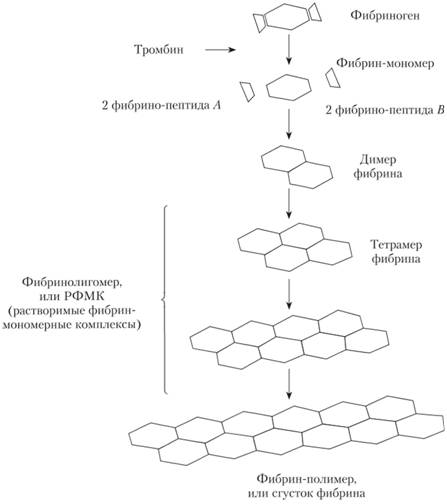
Рис. 5.8. Схема трансформации фибриногена в фибрин.
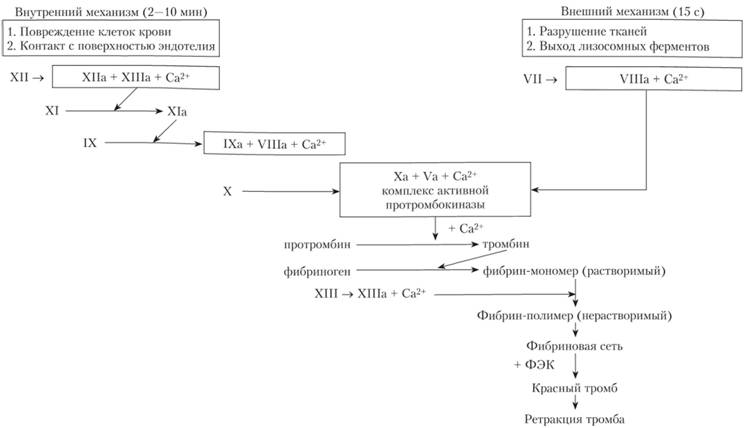
Рис. 5.9. Схема гемостаза:
ФЭК — форменниые элементы крови Уровень фибриногена также понижается при отравлениях змеиным ядом, при приеме анаболических гормонов, андрогенов и рыбьего жира.
Повышенное содержание фибриногена свидетельствует о воспалительных процессах, оно может возникать после приема женских гормонов и в период беременности. Снижение уровня фибриногена говорит о нарушениях в его синтезе, внутрисосудистом свертывании крови.
D-димер — продукт расщепления фибрина. D-димер — маркер процессов тромбообразования и фибринолиза (растворения внутрисосудистых тромбов и внесосудистых отложений фибрина).
С помощью анализа D-димера в крови врач может оценить, как проходит процесс образования и распада фибрина — тромбообразование и фибринолиз, поскольку D-димер в крови образуется лишь при условии, что происходят оба процесса.
Исследование этого показателя свертываемости крови применяется в диагностике тромботических состояний, тромбоза глубоких вен, легочной эмболии, ДВС-синдрома и при осложнениях беременности.
Норма содержания D-димера: менее 248 нг/мл.
После 80 лет уровень содержания D-димера начинает повышаться.
При беременности содержание D-димера в крови постепенно повышается, в 3−4 раза превышая норму к концу срока. Еще бо? льшие значения содержания D-димера в крови означают осложнения беременности — гестоз, преэклампсию и наблюдаются у беременных, больных диабетом, с заболеваниями почек.
Повышенный уровень D-димера характерен для массивных поражений тканей, обширных гематом, повышается вследствие хирургических вмешательств и может быть признаком серьезных заболеваний:
- • тромбоза глубоких вен;
- • ДВС-синдрома;
- • легочной тромбоэмболии;
- • инфекционных заболеваний, сепсиса;
- • онкологических заболеваний;
- • болезней печени;
- • ишемической болезни, сердечной недостаточности.
Повышен уровень D-димера и после инфаркта миокарда.
Антитромбин III — белок свертывающей системы крови, препятствующий свертыванию крови. Антитромбин контролирует свертывающую систему, обеспечивает нормальное свертывание крови и препятствует тромбообразованию в кровотоке.
Синтез антитромбина III происходит в печени и эндотелии.
Норма содержания антитромбина III: 71−115%.
Уровень антитромбина ниже нормы наблюдается у новорожденных, в пожилом возрасте, в середине менструального цикла, в последние месяцы беременности, в послеоперационном периоде и при шоковых состояниях.
Снижение уровня антитромбина III сопровождает следующие заболевания:
- • атеросклероз;
- • врожденную недостаточность антитромбина;
- • заболевания печени (хронический гепатит, цирроз);
- • ДВС-синдром;
- • хроническую печеночную недостаточность;
- • сепсис;
- • тромбоэмболию.
Уровень антитромбина III снижается и при приеме пероральных контрацептивов и эстрогенов.
Повышение уровня антитромбина III — симптом следующих заболеваний органов и систем:
- • вирусного и острого гепатита;
- • холестаза;
- • острого панкреатита;
- • рака поджелудочной железы;
- • дефицита витамина К.
Волчаночный антикоагулянт (ВА) — иммуноглобулин класса IgG. Волчаночный антикоагулянт — это антитело против фосфолипидов, ферментов крови. Волчаночный антикоагулянт получил свое название в связи с тем, что впервые был выявлен в крови у больных системной красной волчанкой.
Норма содержания волчаночного антикоагулянта в крови: 0,8−1,2 усл. ед.
Волчаночный антикоагулянт и другие антитела к фосфолипидам — один из основных признаков развития антифосфолипидного синдрома (АФС).
Волчаночные антикоагулянты, увеличиваясь в количестве в крови человека, прикрепляются к стенкам сосудов, тромбоцитам, вступают в реакции свертывания крови, провоцируя развитие тромбоза.
В зависимости от величины тромба, степени поражения сосуда, местонахождения, скорости закупорки сосуда антифосфолипидный синдром может по-разному проявлять себя. Наиболее частый симптом антифосфолипидного синдрома — тонкая сеточка сосудов на поверхности кожи. Она лучше видна на холоде. Симптомом могут быть даже язвы и омертвение участков кожи пальцев рук или ног.
Небольшое поражение сосудов при АФС вызовет легкие нарушения функции органа, большое поражение вызывает хронические заболевания органов (цирроз печени, болезнь Альцгеймера). Закупорка сосуда тромбом вызовет легочную тромбоэмболию. Антифосфолипидный синдром — одна из основных причин развития инфаркта миокарда у молодых людей до 40 лет.
Повышение уровня волчаночного антикоагулянта в крови может быть признаком следующих заболеваний:
- • аутоиммунных заболеваний;
- • системной красной волчанки;
- • бесплодия;
- • СПИДа;
- • тромбоэмболии;
- • ишемических нарушений мозгового кровообращения.
У беременных женщин повышение уровня волчаночного антикоагулянта в крови может спровоцировать развитие тромбоза артерий плаценты, что может стать причиной внутриутробной гибели плода, невынашивания беременности и преждевременных родов.
Содержание волчаночного антикоагулянта в крови может повыситься как осложнение лекарственной терапии и вследствие приема некоторых медицинских препаратов.
Определение волчаночного антикоагулянта не дает достаточных оснований для постановки врачом того или иного диагноза. Уровень ВА может изменяться под воздействием различных факторов. Обнаружение высокого уровня волчаночного антикоагулянта в крови укажет на необходимость дополнительного обследования.
Наличие в крови волчаночного антикоагулянта и, тем более, его повышенное содержание могут привести к развитию тромбозов. D-димер является продуктом распада фибрина. В норме он должен присутствовать в крови, что свидетельствует о нормальном течении процессов образования и разрушения тромбообразующего белка фибрина. Антитромбин III является ингибитором тромбина, пониженное его содержание может стать причиной тромбозов. Показатель АЧТВ используется для контроля гепаринотерапии и в норме составляет 30−40 с. Его увеличение говорит о недостатке или аномалии факторов свертывания, развитии гемофилии.
Нарушение свертываемости крови может привести к опасным последствиям: повышенная скорость гемостаза приводит к образованию тромбов, которые являются причиной инфарктов и инсультов, а снижение интенсивности процесса вызывает длительные кровотечения. Опасность состоит в том, что нарушения гемостаза внешне могут никак не проявляться, поэтому по рекомендации врача следует обязательно сделать коагулограмму.
Тромбоэмболия (ТЭ) сосудов разной локализации является одной из ведущих причин инвалидизации, смертности и сокращения средней продолжительности жизни населения, которые определяют необходимость применения средств, снижающих свертываемость крови.
- 1. Антиагреганты (препараты, воздействующие на адгезию и агрегацию тромбоцитов (нестероидные противовоспалительные препараты (НПВП), ингибиторы рецепторов Hb/IIIa, тиенопиридины).
- 2. Прямые антикоагулянты (гепарин, низкомолекулярные гепарины).
- 3. Непрямые антикоагулянты (ингибиторы тромбина, антагонисты витамина К).
- 4. Тромболитические препараты (средства, активирующие фибринолитическую систему через преобразование плазминогена в плазмин).
Ацетилсалициловая кислота влияет на начальную фазу тромбообразования при приеме в небольших дозах (0,08−0,3 г) 1 раз в день или через день длительное время. В таких дозах препарат нарушает синтез тромбоксана А, путем ацетилирования циклооксигеназы тромбоцитов. Антиагрегантное действие сохраняется несколько дней, потому что ингибирующее влияние ацетилсалициловой кислоты на циклооксигеназу тромбоцитов необратимо. Восстанавливается циклооксигеназа только в процессе образования новых тромбоцитов. Восстановление уровня этого фермента в стенке сосудов осуществляется в течение нескольких часов, поэтому нормализация содержания тромбоксана А2 наступает через несколько суток, а простациклина — значительно быстрее. При увеличении дозы ацетилсалициловая кислота начинает угнетать образование в эндотелиальных клетках сосудов простациклина, который противодействует агрегации тромбоцитов, и антиагрегантный эффект препарата уменьшается.
Показания к применению: тромбофлебиты, тромбозы сосудов сетчатки, нарушения мозгового кровообращения, для предупреждения послеоперационных тромбов и профилактики тромбоэмболических осложнений при стенокардии и инфаркте миокарда.
Дипиридамол (Курантил®), как и ацетилсалициловая кислота, угнетает агрегацию тромбоцитов и противодействует образованию тромбов в сосудах, угнетая фосфодиэстеразу, что способствует накоплению в тромбоцитах цАМФ. Это приводит к уменьшению выхода из них активаторов агрегации тромбоксана серотонина, АДФ. Угнетает также аденозиндезаминазу. Способствует накоплению аденозина в эритроцитах и тромбоцитах, что сопровождается расширением сосудов и угнетением агрегации тромбоцитов. Дипиридамол переносится лучше, чем ацетилсалициловая кислота, не оказывает ульцерогенного действия. В отдельных случаях наблюдаются покраснение лица, тахикардия, аллергическое кожное высыпание. Препарат противопоказан при атеросклерозе венечных артерий.
Тиенопиридипы — антагонисты рецепторов к АДФ, блокируют АДФиндуцируемый путь активации тромбоцитов путем специфического блокирования P2Y12 рецептора. Первым таким используемым препаратом у больных с ОКС был тиклоиидин.
Тиклопидин (Тиклид) назначается при непереносимости и неэффективности аспирина. Основные фармакодинамические эффекты:
- • ингибирование АДФ (блокада адгезии и агрегации тромбоцитов, нарушение процессов высвобождения тромбоцитарных гранул);
- • улучшение реологических свойств крови (снижение концентрации фибриногена и вязкости крови, улучшение деформируемости эритроцитов).
Для профилактики тромбозов у больных после инсульта, при нестабильной стенокардии, атеросклерозе периферических артерий, после аортокоронарного шунтирования, ангиопластики тиклопидин назначают по 500 мг в сутки. Побочные эффекты: нейтропения, желудочно-кишечные кровотечения, тошнота, рвота, диарея, повышение уровня трансаминаз в печени и атерогенных липопротеидов в плазме крови.
При назначении тиклопидина общий анализ крови с лейкоцитарной формулой осуществляется каждые две недели. Противопоказания: гиперчувствительность к препарату, язвенная болезнь, тяжелые заболевания печени, нейтропения.
Тиклопидин заменен в настоящее время на клопидогрел (Плавике®) и прасугрел (Эффиент®), так как может вызывать серьезные осложнения, такие как нейтропения или тромбоцитопения.
Пентоксифиллин (Трентал®) угнетает фосфодиэстеразу, уменьшает агрегацию тромбоцитов и эритроцитов, повышает фибринолиз, понижает вязкость крови, улучшает микроциркуляцию. Назначается при атеросклерозе периферических артерий. Антиагрегантные свойства имеют также другие производные ксантина — теофиллин, теобромин, эуфиллин, которые угнетают фосфодиэстеразу.
Антагонисты гликопротеинов GP IIb/IIIаа. Абциксимаб (РеоПро®) неконкурентно блокирует и конформационно изменяет гликопротеиновые рецепторы, нарушая фиксацию фибриногена, фактора Виллебранда и других адгезивных молекул с активированным гликопротеиновым комплексом GP IIb/IIIа. Показания: тромбофилические состояния, в том числе острый инфаркт миокарда, нестабильная стенокардия, после ангиопластики коронарных артерий (внутривенно одномоментно или канельно). Побочные эффекты: внутренние кровотечения, брадикардия, гипотензия, тромбоцитопения, аллергические реакции, диспепсия и др.
Отечественный аналог абциксимаба — Монафрам. Монафрам отностится к антиагрегантам — ингибиторам агрегации тромбоцитов. По механизму действия он является антагонистом гликопротеинов GP IIb/IIIаа. Монафрам представляет собой фрагменты мышиных моноклональных антител FRaMon (фрамон) против рецептора фибриногена тромбоцитов GP IIb/IIIаа. Монофрам препятствует взаимодействию с фибриногеном и другими лигандами и, таким образом, ингибирует агрегацию тромбоцитов.
Применяется у больных острым коронарным синдромом (острым инфарктом миокарда) с подъемом сегмента ST при проведении коронарной ангиопластики.
Антикоагулянты прямого действия применяются для профилактики тромбозов.
Гепарин натрий (Лиотон® 1000, Гепариновая мазь, Кальципарин). Низкомолекулярные гепарииы: дальтенарин (Фрагмин), надропарин (Фраксипарин), эноксапарин (Клсксан), рсвипарин (Кливарин). Гепариноиды: сулодексид (Вессел Дуэ Ф). Прямые ингибиторы тромбина — гирудин, лепирудин (Рефлудан) используются при различных заболеваниях с повышенным тромбообразованием.
Антикоагулянты непрямого действия (антагонисты витамина К). Варфарин предупреждает возможность рецидива венозного тромбоза, снижает риск инсульта при неклапанном мерцании предсердий, уменьшает возникновение системных ТЭ после пересадки механических клапанов; у больных с заболеваниями периферических артерий и у лиц с наличием значительных факторов риска варфарин эффективен для предупреждения острого ИМ. Применение варфарина в адекватной дозе позволяет снизить не только частоту инсульта, но и тяжесть его клинических проявлений, а также смертность.
Исторический экскурс
Антикоагулянтные свойства кумаринов были обнаружены случайно. В начале XX в. в Северной Америке было отмечено новое заболевание крупного рогатого скота, которое проявлялось серьезными кровотечениями. В 1939 г. группа американских биохимиков выделила первое вещество кумаринового ряда — дикумарол, вызывавший так называемую болезнь сладкого клевера у коров. С 1950;х гг. непрямые антикоагулянты широко применяются для лечения и профилактики тромбозов.
Преимущества кумаринов перед производными индандиона — они реже вызывают аллергические реакции и дают более стабильный антикоагулянтный эффект. Основным методом контроля гипокоагуляционного эффекта АНД является протромбиновый тест. Использование стандартизированного тромбопластина в протромбиновом тесте сводит к минимуму разброс показаний при повторных исследованиях. Для пациентов, которые ранее не принимали варфарин, начальная доза составляет 5 мг в сутки (2 таблетки в день) в течение первых четырех дней. На 5-й день лечения определяется МНО и, в соответствии с этим показателем, назначается поддерживающая доза препарата. Обычно эта доза составляет 2,5−7,5 мг в сутки (1−3 таблетки в сутки). Частота геморрагий в первую очередь зависит от интенсивности гипокоагуляции, которую отражают показатели МНО. Результаты исследований, основанных на принципах доказательной медицины, свидетельствуют о том, что оптимальный диапазон значений МНО на фоне терапии варфарином должен быть в пределах от 2,0 до 3,0. При каждом увеличении значений МНО на 0,5 ед. выше данного терапевтического диапазона риск геморрагического инсульта возрастает в 1,37 раза. Риск геморрагических осложнений варфарина зависит от так называемых немодифицируемых факторов риска: возраста, пола больных, генетически детерминированной чувствительности к препарату. Усиливают антикоагулянтное действие варфарина за счет взаимодействия с системой цитохрома Р450 клюквенный и грейпфрутовый соки. На фоне совместного длительного приема некоторых растений, таких как корень имбиря, папайя, чеснок, женьшень, гинкго, ананас, куркума, красный стручковый перец, и варфарина возможно появление кровоточивости за счет их влияния на различные механизмы гемокоагуляции. Прямое кумариноподобное действие оказывают конский каштан, донник белый, клевер луговой. Напротив, продукты и растения, богатые витамином К, могут вызывать определенную резистентность к проводимой терапии варфарином. Значительные количества витамина К содержатся в листьях свеклы, листовой и кочанной капусте, капусте брюссельской, брокколи и китайской, в салате латук, в траве пастушьей сумки, люцерне, листьях петрушки, подорожника, шпината, водяном перце, жгучей крапиве, кукурузных рыльцах. Тормозит гинокоагулянтную активность варфарина и коэнзим Q10.
Фибринолитики. Используются для профилактики и лечения тромбозов. Схема фибринолиза представлена на рис. 5.10.
Фибринолизин (человека) — фибринолитическое средство, физиологический компонент естественной противосвертывающей системы. Стимулирует растворение тромба (тканевый фибринолиз) и разрушение фибриногена (системный фибринолиз). Показания к применению: тромбэмболия легочной артерии, сосудов мозга, инфаркт миокарда, острый тромбофлебит, обострение хронического тромбофлебита. Контроль за свертывающей системой крови осуществляется до введения, перед каждым последующим и через сутки после последнего введения фибринолицина путем определения протромбинового индекса (нс ниже 40%), времени общего свертывания крови, которое может увеличиваться нс более чем в 2,5 раза, и фибриногена плазмы (не менее 100 мг%).
Побочное действие: аллергические реакции, кровотечение.
Стрептокиназа и эберкиназа (рекомбинантная стрептокиназа) растворяют тромб (тромболизис). Это позволяет восстановить кровоток, ограничить размер инфаркта и снизить смертность. Тромболизис проводят как можно раньше и в пределах 12 ч от начала заболевания.
Алтеплаза (Актилизе®) — рекомбинантный человеческий активатор плазминогена. Представляет из себя гликопротеин. После связывания с фибрином активируется, вызывая превращение плазминогена в плазмин, что приводит к растворению фибринового сгустка. Применяется для тромболизиса.
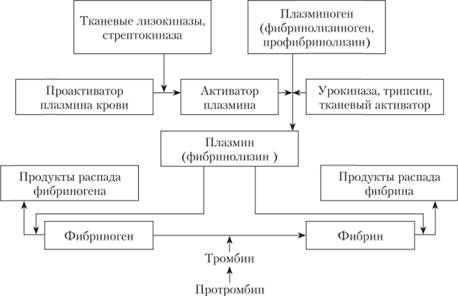
Рис. 5.10. Схема фибринолиза.
Противопоказаниями для всех средств, снижающих свертывание крови, являются гиперчувствительность, кровотечения, эрозии и язвы ЖКТ, недавние множественные ранения, артериальная гипертензия и другие состояния, грозящие кровотечениями.
Фазы гемостаза и точки приложения антитромботических средств представлены на рис. 5.11.
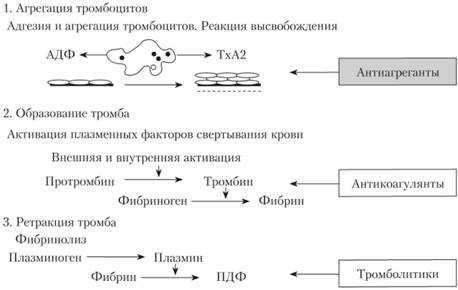
Рис. 5.11. Фазы гемостаза и точки приложения антитромботических средств.