Теплота и температура горения

Методика определения температуры горения других классов веществ аналогична. В случае горения индивидуальных химических соединений при определении Vn г удобнее пользоваться единицей измерения кмоль/кмоль, а при нахождении Qn г и Д#ср — единица измерения кДж/кмоль. В этом случае в расчете необходимо использовать данные табл. 113 приложения. Таким образом, температура горения находится в интервале… Читать ещё >
Теплота и температура горения (реферат, курсовая, диплом, контрольная)
Теплота горения
Пример 1. Рассчитать по закону Гесса низшую теплоту горения бензола в кДж/моль и кДж/м3.
Решение
1. Запишем уравнение реакции горения бензола в воздухе:

2. Уравнение закона Гесса для этого случая будет выглядеть гак:
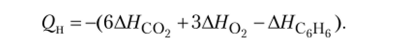
Значения величины АН0 для С02, Н20 и С6Нб возьмем из табл. ПЗ приложения:
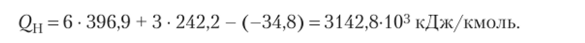
3. Низшую теплоту сгорания 1 кг бензола найдем исходя из закона Авогадро и определения киломоля. При сгорании 1 кмоля = 78 кг выделяется тепла 3142,8 • 103 кДж; при сгорании 1 кг выделяется тепла.
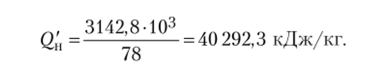
4. Теплоту сгорания 1 м3 паров бензола при нормальных условиях определим, используя следствие из закона Авогадро. При сгорании 1 м3 паров выделяется тепла.
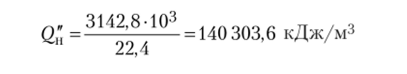
Пример 2. Определить по формуле Менделеева низшую теплоту горения 4-метил-5-р-оксиэтилтиазола (C6H9ONS).
Решение
Так как необходимо определить низшую теплоту горения, величину ДТ/О Q выбираем для газообразной воды.
1. Определим весовой состав вещества:

2. Определим низшую теплоту горения вещества:
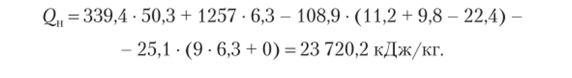
Пример 3. Определить низшую теплоту сгорания в кДж/м[1] и кДж/кмоль газовой смеси, имеющей следующий состав: СО=20%, Н2 = 10%, СН4 = 20%, С2Н6 = 20%, С02 = 10%, N2 = 10%, 02= 10%. Условия — нормальные.
Решение
1. Из справочника определяем теплоту сгорания компонентов:
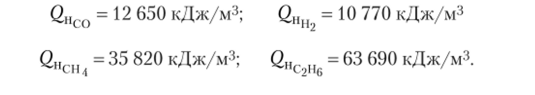
2. По формуле (2.21) находим теплоту сгорания 1 м3 смеси:
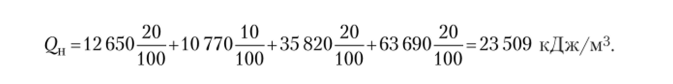


V" г = 0,84 + 0,68 + 3,28+1,66 = 6,46 м3
При нормальных условиях продукты горения 1 кг древесины будут состоять из: 0,84 м3 С02; 0,68 м3 паров Н20; 3,28 м3 N2 и 1,66 м3 воздуха. Общий объем продуктов горения составит 6,46 м3/кг.
3. Найдем температуру горения. Для этого определим среднее теплосодержание единицы объема продуктов горения:

Это значит, что в каждом 1 м3 продуктов горения при температуре горения будет содержаться 2129,3 кДж тепла. Учитывая, что 3,28 + 1,66−0,79 00/
на-100 =71,2% продукты горения состоят из азота,.
6,49.
по табл. П5 приложения находим, при какой температуре удельное теплосодержание азота соответствует найденной величине (2129,3 кДж/м3). Видим, что эта температура находится между [(1400 — 1500) + 273] К. Принимая во внимание, что в состав продуктов горения входят С02 и Н20, которые обладают таким теплосодержанием при более низких температурах, задаемся температурой (1300 + 273) К и определяем для нее суммарное теплосодержание продуктов горения:

где величины АН" г определены по табл. ПЗ приложения.
Так как теплосодержание продуктов горения при Т = 1573 К ниже <2п г = 13 819 кДж, то Тг > 1573 К.
Задаемся Т = (1400 + 273) К и вновь определяем теплосодержание продуктов горения при 1673 К:
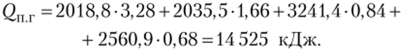
Так как теплосодержание продуктов горения при Т = 1673 К выше Qn Г' тг< 1673 К.
Таким образом, температура горения находится в интервале 1573—1673 К. Точное значение температуры горения найдем методом интерполяции, считая, что в этом интервале температур теплосодержание продуктов горения линейно зависит от температуры:
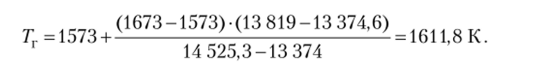
Методика определения температуры горения других классов веществ аналогична. В случае горения индивидуальных химических соединений при определении Vn г удобнее пользоваться единицей измерения кмоль/кмоль, а при нахождении Qn г и Д#ср — единица измерения кДж/кмоль. В этом случае в расчете необходимо использовать данные табл. 113 приложения.
- [1] Теплоту сгорания 1 кмоля газовой смеси найдем, используяследствие из закона Авогадро: 1 кмоль газа при нормальных условиях занимает объем 22,4 м1: