Энергия ионизации и сродство к электрону

Под электроотрицателыюстыо элемента (ЭО) подразумевают относительную способность его атомов притягивать электроны. Атомы элементов обладают различной электроотрицательностью: одни легче отдают электроны, другие легче их присоединяют. При образовании химической связи между двумя атомами связующие электроны обычно больше притягиваются тем атомом, у которого электроотрицательность больше… Читать ещё >
Энергия ионизации и сродство к электрону (реферат, курсовая, диплом, контрольная)
Поскольку электрон притягивается ядром, то для его отрыва нужно сообщить атому энергию, превышающую энергию этого взаимодействия. Количество энергии, затрачиваемое для превращения нейтрального атома в положительно заряженный ион, называется энергией ионизации, или ионизационным потенциалом. Для химических исследований наибольшее значение имеют первые потенциалы; первым потенциалом ионизации называется энергия, затрачиваемая на полное удаление наиболее слабо связанного электрона от атома в невозбужденном состоянии. Ионизируемым является тот электрон, для которого энергия минимальна.
Внутри каждого периода слева направо наблюдается повышение ионизационных потенциалов (рис. 3.9). В некоторых случаях это происходит не всегда равномерно и иногда потенциал ионизации элемента оказывается меньше, чем у предыдущего элемента того же периода.
Примером могут служить бор (Z = 5) и бериллий (Z = 4). У бора потенциал ионизации меньше, чем у бериллия. Это объясняется большим про;
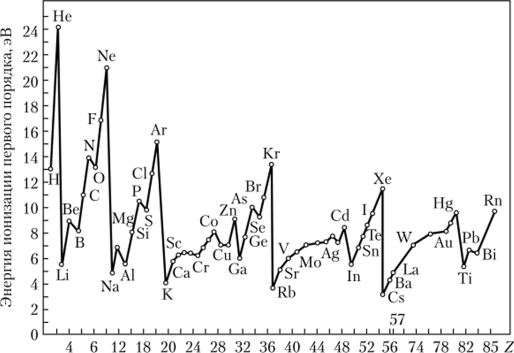
Рис. 3.9. Периодическая зависимость ионизационных потенциалов атомов от порядкового номера элемента.
никновением s-электронов к ядру по сравнению с р-электронами того же энергетического уровня. Ионизация бериллия сопровождается отрывом от атома s-электрона второго уровня, а ионизация бора — отрывом р-электрона того же уровня. Проникающий эффект электронов зависит от их природы: наибольшим эффектом обладают s-электроны, меньшим — р-электроны и еще меньшим d- и/-электроны. Эффект проникновения более характерен для тяжелых атомов с большим числом электронов во внутренних слоях. Проникающий эффект внешних электронов наиболее сильно выражен у ^-элементов.
Атомы (и молекулы простых веществ) могут не только отщеплять электрон, но и присоединять. Тепловой эффект, отнесенный к 1 молю нейтрального атома элемента при присоединении им электрона, называется энергией сродства к электрону.
Сродство к электрону возрастает с уменьшением радиуса. Следовательно, в пределах периода с увеличением заряда ядра от щелочного металла к галогену наблюдается увеличение сродства к электрону. В пределах групп сверху вниз наблюдается обратная зависимость, т. е. с увеличением заряда ядра сродство к электрону уменьшается.
Потенциал ионизации и сродство к электрону — важные характеристики реакционной способности атомов элемента. Если атомы двух элементов сильно отличаются между собой значениями потенциалов ионизации, то у одного из них будет низкий потенциал ионизации, а у другого — высокое сродство к электрону. Такие атомы будут легко реагировать друг с другом с образованием прочной связи. Практическое использование этих характеристик ограничено тем, что они относятся к изолированным атомам, т. е. к газообразным состояниям. Если же атомы находятся не в изолированном состоянии, то в этом случае принято пользоваться эмпирической величиной, называемой электроотрицательностью.
Под электроотрицателыюстыо элемента (ЭО) подразумевают относительную способность его атомов притягивать электроны. Атомы элементов обладают различной электроотрицательностью: одни легче отдают электроны, другие легче их присоединяют. При образовании химической связи между двумя атомами связующие электроны обычно больше притягиваются тем атомом, у которого электроотрицательность больше. Следовательно, зная значения электроотрицательностей взаимодействующих атомов, можно предсказать тип формирующейся связи между ними. Так, молекулы, образованные атомами, сильно отличающимися по электроотрицательности, должны быть более ионными, а если у взаимодействующих атомов близкие значения электроотрицательностей, то между ними образуется менее полярная связь.
Внутри периода слева направо электроотрицательность увеличивается. Для переходных элементов электроотрицательность несколько уменьшается в пределах периода. Внутри групп электроотрицательность преимущественно уменьшается сверху вниз (рис. 3.10).
Н1 2,1. |
| |||||
Li. | Be. | в. | C. | N. | F. | |
1,0. | 1,5. | 2,0. | 2,5. | 3,0. | 3,5. | 4,0. |
Na. | Mg. | Al. | Si. | P. | s. | Cl. |
0,9. | 1,2. | 1,5. | 1,8. | 2,1. | 2,5. | 3,0. |
К. | Ca. | Ga. | Ge. | As. | Se. | Br. |
0,8. | 1,0. | i, 6. | 1,8. | 2,0. | 2,4. | 2,8. |
Rb. | Sr. | In. | Sn. | Sb. | Tc. | I. |
0,8. | 1,0. | 1,7. | 1,8. | 1,9. | 2,1. | 2,5. |
Рис. 3.10. Значение относительной электроотрицательности некоторых «V- и /7-элементов по Полингу2
Степень окисления. Смещение связующих электронов в сторону более электроотрицательного атома создает у него избыток отрицательного заряда, а у менее электроотрицательного — дефицит электронов. В соединениях с ионной связью атом, отдавший электрон, превращается в катион, а принявший электрон — в анион. Для характеристики атомов в молекуле введено понятие степени окисления, или окислительного числа атомов. Степень окисления — численное значение электрического заряда атома при допущении, что молекула построена по ионному типу. Эта величина указывает на состояние окисления атома и представляет собой лишь удобный метод учета переноса электронов: она не является истинным зарядом атома в молекуле. Более подробно см. параграф 9.1.