Декарбоксилирование аминокислот.
БИОХИМИЯ Часть 2.

Другим примером образования биологически активных аминов в процессе декарбоксилирования аминокислот является образование гистамина (из гистидина), большие количества которого выделяются из тучных клеток соединительной ткани, вызывая аллергическую реакцию в ответ на действие аллергена: В животных тканях выявлено декарбоксилирование тирозина, триптофана, 5-окситриптофана, валина, серина, гистидина… Читать ещё >
Декарбоксилирование аминокислот. БИОХИМИЯ Часть 2. (реферат, курсовая, диплом, контрольная)
Отщепление карбоксильной группы аминокислот в виде СО, катализируется декарбоксилазами аминокислот, которые весьма широко распространены в природе. Примеры ферментативного декарбоксилирования аминокислот и их производных у различных видов живых организмов представлены в табл. 24.3.
В животных тканях выявлено декарбоксилирование тирозина, триптофана, 5-окситриптофана, валина, серина, гистидина, глутаминовой и у-оксиглутам и новой кислот, 3,4-диоксифенилаланина, цистеина и цистеинсульфи новой кислоты, аргинина, орнитина, S-адснозил метионина, а-аминомалоновой кислоты.
Среди различных типов декарбоксилирования аминокислот для организма человека и животных наибольшее значение имеет а-декарбоксилированис, т. е. отщепление карбоксильной группы при а-углеродном атоме и образование продуктов реакции аминов, обладающих, как правило, сильным фармакологическим действием и поэтому названных биогенными аминами.
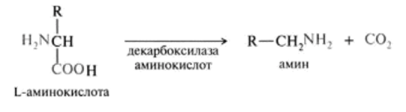
Таблица 24.3. Ферментативное дскарбоксилирование аминокислот и их производных (по Т. Т. Березову и Б. Ф. Коровкину, 1983).
Субстрат. | Продукт реакции. | Распространение. | ||
животные. | растения. | микроорганизмы. | ||
5-Аденозил метионин. | S- Аденозил гомоцистсамин. | |||
«-Аминобензойная кислота. | Анилин. | |||
а-Аминомалоновая кислота. | Глицин. | |||
а-Аминомасляная кислота. | Пропиламин. | |||
Антраниловая кислота. | Анилин. | |||
L-Аргинии. | Агматин. | |||
L-Аспарагиновая кислота. | р-Аланин. | +(?). | ||
L-Аспарагиновая кислота. | а-Аланин. | |||
L-Валин. | 2-Метил пропиламин. | |||
L-Гистидин. | Гистамин. | |||
Две молекулы глицина. | 2С02 + 2NH3 + СН, СООН. | |||
L-Глутаминовая кислота. | у-Аминомасляная кислота. | |||
Мезо-а; е-диаминопимелиновая. | L-Лизин. | |||
кислота. | ||||
3,4-Диоксифенилаланин. | 3.4-Диоксифенилэтиламин. | |||
L-Изолейцин. | 2 — М стил буг ил, а м и н. | |||
L-Лейцин. | 3 — Мстилбутил ами н. | |||
L-Лизин. | Кадаверин. | |||
у-МетиленL-глутаминовая. | у-Амино-а-метилеимасляная. | |||
кислота. | кислота. | |||
Норвалин. | «-Бутил амин. | |||
Алло-р-оксиглутаминовая кислота. | у-Амино-и-оксимасляная кислота. | |||
у-Оксиглутаминовая кислота. | а-Окси-у-аминомасляная кислота. | |||
5-Оксилизин. | 2-Оксикадавсрин. | |||
5-Окситриптофан. | Серотонин. | |||
«-Оксифенилсерин. | «-Оксифениламиноэтанол. | |||
L-Орнитин. | Путресцин. | |||
L-Ссрин. | Этаноламин. | |||
L-Тирозин. | Тирамин. | |||
L-Тригттофан. | Тритамин. | |||
L-Фенил аланин. | Фенил этиламин. | |||
L-Цистеиновая кислота. | Таурин. | |||
L-Цистсинсульфиновая кислота. | Гипотаурин. | |||
Реакции дскарбоксилирования, в отличие от других процессов промежуточного обмена аминокислот, являются необратимыми. Декарбоксилазы аминокислот являются сложными ферментами, коферментами которых, как и у трансаминаз, является пиридоксальфосфат (ПФ), специфичность их действия определяется апобелковым компонентом фермента. Механизм реакции дскарбоксилирования аминокислот в соответствии с теорией пиридоксалевого катализа связан с образованием шиффова основания между пиридоксальфосфатом и аминокислотой, лабилизацисй всех связей в субстрате (а, Ь, с), что обусловливает способность аминокислоты вступать в реакции трансаминирования (а), декарбоксилирования (b), альдольного расщепления ©.
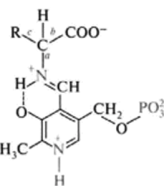
шиффово основание между аминокислотой и пирилоксальфосфатом Неспецифическая декарбоксилаза ароматических аминокислот катализирует декарбоксилирование триптофана, 5-гидрокситриптофана и 3,4-диоксифенилаланина (ДОФА). Продуктами реакций, помимо С02, являются соответственно триптамин, серотонин и диоксифенилэтиламин (дофамин):
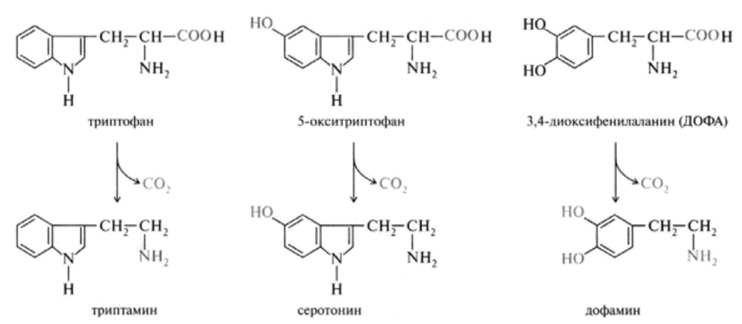
Образующиеся биогенные амины — триптамин, серотонин, дофамин обладают сильным фармакологическим действием на множество физиологических функций человека и животных. Так, триптамин и серотонин оказывают сосудосуживающее действие. Кроме этого, серотонин участвует в регуляции артериального давления, температуры тела, дыхания и почечной фильтрации, является нейромедиатором, который вызывает изменение поведения, например при шизофрении. Дофамин, возможно, сам является нейромедиатором, а также предшественником широко известного медиатора норэпинефрина и гормона адреналина. Источником ДОФА в организме является тирозин, который под действием специфической гидроксилазы превращается в 3,4-диоксифенилаланин. Тирозингидроксилаза открыта в надпочечниках, в тканях мозга и периферической нервной системы.
Другим примером образования биологически активных аминов в процессе декарбоксилирования аминокислот является образование гистамина (из гистидина), большие количества которого выделяются из тучных клеток соединительной ткани, вызывая аллергическую реакцию в ответ на действие аллергена:
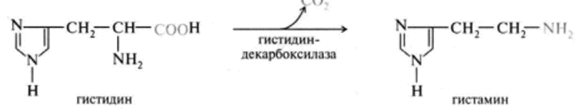
Количество гистамина увеличивается при различных патологических состояниях организма: травмах, стрессе, а также при введении в организм различных ядов и некоторых лекарственных веществ (антибиотиков, лечебных сывороток и др.).
Гистамин обладает широким спектром биологического действия. Много гистамина образуется в очаге воспаления, обладая сосудорасширяющим действием, он ускоряет приток лейкоцитов и тем самым активирует защитные силы в борьбе с инфекцией. Большое количество гистамина образуется в слизистой желудка, где он активирует секрецию пепсина и соляной кислоты.
Важную биологическую функцию выполняет у-аминомасляная кислота (ГАМК) — продукт а-декарбоксилирования глутаминовой кислоты. Фермент, катализирующий эту реакцию (глутаматдекарбоксилаза), является высокоспецифичным:

Оба эти соединения — глутамат и ГАМК — относятся к нейромедиаторам: ГАМК ингибирует, а глутамат активирует передачу нервных импульсов.
Введение
у-аминомасляной кислоты вызывает тормозной процесс в коре головного мозга (центральное торможение), а у животных приводит к утрате условных рефлексов. у-Аминомасляная кислота используется в клинике при лечении некоторых заболеваний ЦНС, связанных с резким возбуждением коры головного мозга.
К биогенным аминам относится также таурин, который образуется из цистеина и используется в печени при образовании парных желчных кислот:
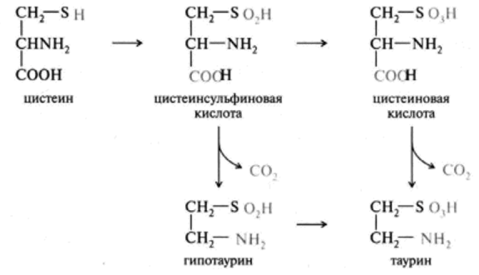
Таким образом, биогенные амины являются сильными, фармакологически активными веществами, оказывающими разностороннее действие на физиологические функции организма. Некоторые биогенные амины (гистамин.
серотонин, их производные) нашли широкое применение в качестве лекарственных средств.