Гидроксид алюминия.
Соли алюминия

Алюминий образует большое число различных солей. Они представляют собой твердые, как правило, белые вещества. Эти соли или растворимы (хлорид, нитрат, сульфат, квасцы и др.), или нерастворимы (фосфат, алюмосиликат, каолин и др.). Их химические свойства определяются особенностями аниона и катиона алюминия. Одним из важных свойств является их способность к гидролизу, так как они, как минимум, соли… Читать ещё >
Гидроксид алюминия. Соли алюминия (реферат, курсовая, диплом, контрольная)
Гидроксид алюминия получают действием щелочи на раствор соли:
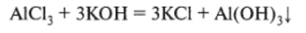
Гидроксид алюминия применяют для очистки воды на водоочистительных станциях, так как А1(ОН)3 способен поглощать различные загрязняющие вещества.
Соли алюминия
Алюминий образует большое число различных солей. Они представляют собой твердые, как правило, белые вещества. Эти соли или растворимы (хлорид, нитрат, сульфат, квасцы и др.), или нерастворимы (фосфат, алюмосиликат, каолин и др.). Их химические свойства определяются особенностями аниона и катиона алюминия. Одним из важных свойств является их способность к гидролизу, так как они, как минимум, соли слабого основания (гидроксид алюминия амфотерен и в данном случае выступает в роли слабого основания).
Соли алюминия в определенных количествах ядовиты для человека, в чем состоит их негативная экологическая роль.
Рассмотрим применение наиболее важных солей алюминия.
Алюмокалиевые квасцы KA1(S04)2* 12Н20 и аммонийно-алюминиевые квасцы NH4A1(S04)2 • 12Н20 используют для обработки кож (обладают коагулирующим воздействием); при водоочистке (подвергаются гидролизу, образуя гидроксид алюминия в коллоидном состоянии) и т. д.
Сульфат алюминия — применяют при водоочистке, как реактив в лаборатории и т. д.
Атюмосиликаты различного состава, например каолин А1203 • 2Si02 • ЗН20 — сырье для получения фаянса и фарфора.
Трехкальциевый алюминат ЗСаО • А1203 — компонент цемента.
? Задания для самостоятельной работы[1][2][3][4]
I. Общая характеристика.
Железо находится в четвертом ряду, в четвертом периоде в VIIIB-группе (в побочной подгруппе VIII группы), в семействе железа. О нем в периодической системе имеются сведения: Fe — химический знак (две буквы латинского названия, показывающие, что это железо, 1 его атом; 56 мае. ч); /lr(Fe) = 56 (относительная атомная масса, выраженная в а.е.м., показывающая, что масса атома железа в 56 раз больше массы 1 а.е.м. и в его ядре содержится 56 нуклонов); номер Fe равен 26, т. е. в ядре атома железа содержится 26 протонов, а в электронной оболочке — 26 электронов.
Составьте схему, электронную и графическую формулы атома; обоснуйте валентные возможности железа в этом состоянии.
Краткая электронная формула стационарного состояния: …3dHs. Краткая графическая формула возбужденного состояния:
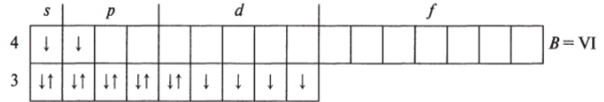
Краткая электронная формула возбужденного состояния: …3 d4s4p.
Железо проявляет валентность II и III, из них более характерна В = III. Его максимальная валентность равна VI. Возможные степени окисления: +2, +3, +6.
В последние годы были получены соединения, в которых железо проявляет С.О. = +8. M (Fe) = 56 г/моль.
II. Физические свойства.
В свободном состоянии железо является твердым кристаллическим веществом серо-белого цвета с металлическим блеском, р = = 7,87, = 1589 °C. Оно ковко и пластично. Существует несколько аллотропных видоизменений (а, Р, у), которые устойчивы при разных температурах.
III. Химические свойства.
1. Железо реагирует с неметаллами:
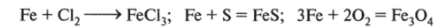
2. Взаимодействует с водой: 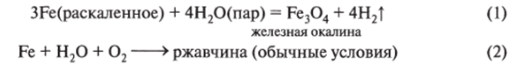
3. Реагирует с водными растворами солей (согласно ряду напряжений): 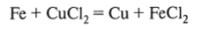
4. Взаимодействует с кислотами:
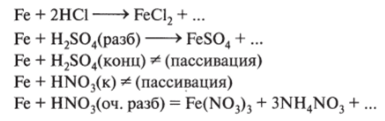
Завершите и уравняйте схемы реакций.
IV. Получение.
В лаборатории железо практически не получают, так как используют товарные образцы. Однако его можно получать восстановлением оксидов, например алюминотермией:
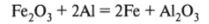
В промышленности получение железа осуществляют в два этапа на различных производствах.
1. Доменный процесс. Процесс получения чугуна в домнах называется варкой чугуна.
Сплав железа с углеродом, содержащий до 4,5% углерода, 0,5— 2% кремния, 1—3% марганца, 0,02—2,5% фосфора и 0,005—0,08% серы, называют чугуном. Он хрупок, не ковок и не пластичен. Различают серый (литейный) и белый (передельный) чугун. В белом чугуне углерод содержится в виде цементита Fe3C. Серый чугун применяют для получения различных деталей машин, посуды, белый — полностью переплавляется в сталь.
Сырьем доменного процесса являются железные руды, лом, кокс, флюсы. К железным рудам относят: FeC03 — сидерит; Fe304 — магнитный железняк, магнетит; Fe203 — гематит, красный железняк; Fe203 *хН20 — лимонит, бурый железняк. Источником железа в доменном процессе являются также продукты обжига сульфидов железа и железный лом.
Кокс в доменном процессе многофункционален: он является топливом, сырьем для получения восстановителя и восстановителем. Для интенсификации доменного процесса используют метан (топливо и сырье для получения восстановителей — водорода и угарного газа).
Для удаления примесей из получающегося чугуна используют флюсы. Для кислых руд флюсом является известняк СаС03, для основных руд — диоксид кремния Si02. Кислые руды в качестве примесей содержат диоксид кремния, основные руды — карбонаты кальция и магния.
Химизм доменного процесса. При протекании доменного процесса реализуется большое число химических процессов. Рассмотрим наиболее важные из них. Эти процессы условно подразделяют на группы.
1. Получение оксидов железа:
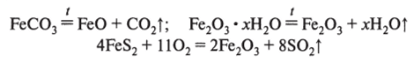
2. Получение восстановителя:
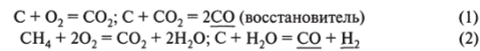
3. Восстановление оксидов железа:
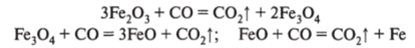
(сначала — губчатое, потом оно переходит в расплав).
При 1000 °C возможны процессы:
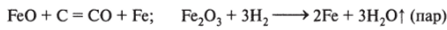
4. Образование шлака:
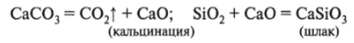
Шлак имеет более низкую температуру плавления, чем примеси, кроме того, шлак предотвращает окисление расплавленного железа кислородом воздуха, поступающего в домну.
Доменный процесс завершается образованием чугуна:

Варку чугуна осуществляют в доменных печах (домнах) (рис. 10.3) — вертикальных сооружениях, расширяющихся книзу (шахта) до самой широкой части — распара, после чего сужается и самая узкая часть домны — под доменной печи. В районе распара имеются фурмы, при помощи которых в домну подается воздух и небольшое количество метана для оптимизации процесса. В верхнюю часть домны через загрузочное устройство поступает шихта (смесь руды, кокса и флюсов в определенных количественных соотношениях), которая, постепенно нагреваясь, поступает в низ домны (поэтому домна книзу расширяется). После плавления железа объем смеси уменьшается, поэтому в районе пода доменная печь сужается. Над расплавленным чугуном находится слой шлака. Шлак, с одной стороны, Очищает чугун от примесей, а с другой, предохраняет расплавленный чугун от окисления. В доменном процессе используются следующие принципы научного химиче;
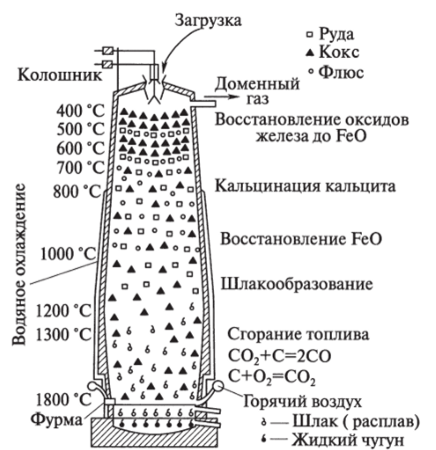
Рис. 10.3. Схема доменного процесса и строения домны.
ского производства: непрерывность процесса, противоток, использование оптимальных температур, утилизация теплоты, комплексное использование сырья и отходов (шлак используют для получения строительных материалов и т. д.).
Производство чугуна является экологически опасным процессом, поэтому требует усовершенствования.
2. Варка стали. Стали — сплавы железа, содержащие 1,7% углерода и менее (по массе). Различают твердые (1,7—0,3% углерода) и мягкие (менее 0,3% углерода) стали. Кроме углерода, в сталях содержатся и другие компоненты, придающие им особые свойства, которые позволяют применять их в различных областях хозяйства.
Сущность варки стали состоит в проведении процессов удаления из чугуна избыточного углерода и неметаллических примесей (серы, фосфора и др.). Применяют различные способы варки стали, среди которых наиболее распространены конверторные, мартеновские и электрометаллургические методы.
Конверторные способы подразделяют на бессемеровский, томасовский и конверторный с кислородным дутьем сверху. Последний метод является самым эффективным, так как при небольшом времени на реализацию процесса получают стали высокого качества.
Стали специального назначения, обладающие особыми свойствами, варят в электропечах.
Химизм варки стали. Процесс сталеварения сложен, но его условно можно охарактеризовать рядом химических процессов, в результате осуществления которых из сырья (передельного чугуна, железного лома и др.) удаляются неметаллические примеси и вводятся добавки, позволяющие получать стали с различными свойствами. Рассмотрим наиболее важные процессы, протекающие при варке стали. Их условно подразделяют на группы процессов.
1. Получение окислителя (примеси удаляют за счет их окисления и проведения реакций, позволяющих удалить продукты окисления из сплава, если это не газы):
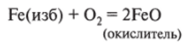
2. Окисление примесей (окисляются как металлические, так и неметаллические примеси):
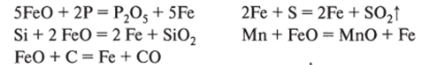
- 3. Шлакообразование: оксид фосфора (У) и диоксид кремния удаляются за счет реакции с оксидом кальция, который или содержится в футеровке аппарата, или добавляется в виде известняка; этот процесс называют шлакообразованием. Получающиеся шлаки можно использовать как удобрения (томасшлак) или в производстве строительных материалов.
- 4. Раскисление (удаление избытка окислителя): избыток оксида железа (Н) удаляют, вводя раскислители — металлы, восстанавливающие этот оксид. Наиболее часто применяют марганец или алюминий. Эти металлы одновременно являются и легирующими добавками, т. е. они придают сталям специфические, эксплуатационно полезные свойства. Такими добавками являются хром, титан, ванадий и т. д.
Производство сталей является экологически опасным процессом, поэтому требует усовершенствования.
V. Применение.
Железо и его сплавы (чугуны, стали) находят широкое применение в деятельности людей. Открытие железа и получение его из руд стало поворотным пунктом в развитии человечества. В чистом виде железо используют в качестве катализатора при синтезе аммиака. Основное применение находят чугун и стали, называемые черными метшлами. Из них изготавливают машины, агрегаты, различные сооружения и технику (транспортную, сельскохозяйственную, военную). Применяют черные металлы и в строительстве (строительные машины, железобетон, детали водопровода и канализации и т. д.). Обработкой металлов занимается металлообрабатывающая отрасль промышленности.
Необходимо отметить, что добыча руд, варка чугуна и стали являются процессами, нарушающими экологическое равновесие. В районах производств железа и его сплавов возникает неблагоприятная экологическая обстановка. Перед учеными и практиками стоит задача такой организации производства и обработки черных металлов, при которой отрицательное воздействие этих производств будет минимальным.
VI. Железо в природе. Экологическая роль соединений железа.
Земная кора содержит 4,65% железа (по массе). В свободном виде встречается только в составе метеоритов. Наиболее важные железосодержащие минералы: Fe304 — магнитный железняк, магнетит; Fe203 — гематит, красный железняк; 2Fe203 • ЗН20 — лимонит, бурый железняк; FeC03 — сидерит или шпатовый железняк; FeS2 — пирит или железный колчедан. Входит железо и в состав других горных пород, но они как руды для получения железа не используются. Железо является компонентом органических веществ, в частности гемоглобина, без которого невозможна жизнь аэробных животных, включая человека (гемоглобин является дыхательным пигментом). Железо является составной частью ядра Земли.
Без соединений железа невозможна жизнь различных организмов, так как оно входит в состав жизненно важных соединений, участвующих в обмене веществ. Из соединений железа формируются горные породы, образующие природные ландшафты, и т. д.
- ? Задания для самостоятельной работы
- 1. Поясните, почему валентность невозбужденного атома железа равна нулю.
- 2. Поясните, почему при обычных условиях железо относительно малоактивно.
- 3. Поясните, почему введение в железо углерода делает его более твердым, а при достаточно высоких концентрациях не ковким и не пластичным.
- 4. Поясните, чем (с позиций валентности) отличается взаимодействие железа с неокислительными и окислительными кислотами; приведите соответствующие уравнения реакций.
- 5. Поясните, в чем состоит сущность процесса: а) варки чугуна; б) варки стали.
- 6. Приведите три обоснованных примера использования железа человеком.
- 7. Приведите обоснованный пример экологического воздействия получения черных металлов.
- [1] Поясните, почему гидроксид алюминия амфотерен, используя равновесие в коллоидном растворе этого гидроксида в воде.
- [2] Напишите уравнения реакций взаимодействия гидроксида алюминияс едким натром: а) с позиций теории комплексных соединений (три уравнения в условно-молекулярной и краткой ионной формах); б) в традиционнойформе.
- [3] Напишите уравнения реакций взаимодействия сульфата алюминия сгидроксидом калия в зависимости от молярного соотношения соли и щелочи (три варианта).
- [4] Приведите три обоснованных примера использования солей алюминия.