Основы неорганической химии

Работа адгезии Wa, также отнесенная к единице поверхности, опреде-ляется как работа разрыва межфазного поверхностного слоя. В этом случае энергия затрачивается на образование двух поверхностей раздела, равных по величине, но разных по свойствам. Соответственно, изменения свободной энергии связаны с заменой свободной энергии исходной межфазовой границы на свободную энергию поверхностей фаз… Читать ещё >
Основы неорганической химии (реферат, курсовая, диплом, контрольная)
1. При каких условиях энтальпия является критерием самопроизвольного процесса? Каково ее изменение в этих условиях?
Если энтропия веществ в реакции не изменяется, и давление постоянно, то самопроизвольно могут протекать реакции с уменьшением энтальпии В изохорном процессе V = const, ДV = 0, следовательно, тепловой эффект реакции QV равен изменению внутренней энергии системы:
QV = U2 — U1 = ДU, т.к. работа W = 0.
В изобарном процессе p = const, следовательно, тепловой эффект реакции Q равен:
QP = ДU + p· ДV = (U2 — U1) + p· (V2 — V1) = (U2 + p· V1) — (U1 + p· V1).
Обозначим: U + p· ДV = H.
Величина H называется энтальпией или теплосодержанием системы. Поэтому тепловой эффект химической реакции при изобарном процессе равен изменению энтальпии системы:
QP = H2 — H1 = ДH.
или QP = ДU + p· ДV = ДH.
Энтальпия, также как и внутренняя энергия, является термодинамической функцией состояния системы. Для реакций, в которых участвуют только твердые и жидкие вещества, член p· ДV мал или равен нулю.
Одной из составляющих движущей силы самопроизвольно идущих процессов является тенденция к понижению энергии системы. Экзотермические реакции, при протекании которых выделяется теплота, сопровождаются уменьшением энтальпии. Экзотермические реакции, как правило, идут самопроизвольно. Однако тенденция к достижению минимальной энергии не является единственным фактором Однако тенденция к достижению минимальной энергии не является единственным фактором, определяющим направление самопроизвольного процесса. На это указывает возможность самопроизвольного протекания не только экзотермических, но и эндотермических реакций. Частицам (молекулам, атомам, ионам и др.) присуще стремление к беспорядочному движению, поэтому система стремится перейти из более упорядоченного состояния в менее упорядоченное. Количественной мерой неупорядоченности (беспорядка) системы является термодинамическая функция состояния системы — энтропия (S, Дж/(моль· K)). Чем в большей мере выражен беспорядок в системе, тем больше ее энтропия. Следовательно, еще одной составляющей движущей силы самопроизвольно протекающих процессов является тенденция к увеличению энтропии системы. Принято, что энтропия идеально правильно построенных кристаллов при T = 0 К равна нулю (в такой системе полностью устраняется всякая неупорядоченность, положение частиц в узлах кристаллической решетки характеризуется идеальным порядком).
Если энтропия веществ в реакции не изменяется, и давление постоянно, то самопроизвольно могут протекать только реакции с уменьшением энтальпии.
2. Каково соотношение между константами равновесия Кр и Кс химической реакции, А + В = С + D, если вещества находятся в идеальном газообразном состоянии?
Константа равновесия обратимой реакции A + B = C + D выражается соотношением: Kр = pС• pD / pA• pB или Kс = СС• СD / СA• СB
p — равновесные парциальные давления газообразных веществ, С — их концентрации.
Величина константы химического равновесия может быть выражена через концентрации реагирующих веществ. Kс = СС• СD / СA• СB
Для гомогенных реакций газов при небольших давлениях (когда газ подчиняется законам идеальных газов) вместо концентрации компонентов пользуются величинами соответствующих парциальных давлений. В этом случае выражение для константы химического равновесия выглядит следующим образом: Kр = pС• pD / pA• pB
Kр = Кс • (RT) •Дх Дх — алгебраическая сумма стехиометрических коэффициентов (разность коэффициентов в уравнении реакции) Здесь Дх = У х (продуктов) — У х (исх. веществ) = 2 -2 =0.
То есть константы Kр и Kс равны.
- 3. Вычислите Н°, U°, G0 (энергию Гиббса). Определите, в каком направлении пойдет реакция при стандартных условиях:
- 2HCI® = Н2+ Cl2
Мерой химического сродства является убыль G потенциала или G. Самопроизвольно протекающие процессы идут в сторону уменьшения любого потенциала и, в частности, в сторону уменьшения G.
Если G О — процесс самопроизвольно проходить не может Чем меньше G, тем сильнее стремление к протеканию данного процесса и тем дальше он от состояния равновесия; при котором G0 = 0 и H0 = ТS0
Энтальпии, внутрениии энергии и свободные энергии Гиббса образования для простых веществ в стандартных условиях равны нулю.
Следовательно, необходимые значения определяются только значениями этих величин для хлороводорода.
Для расчета ДН°, ДU°, ДG° реакции разложения хлороводорода при 298 К выпишем энтальпии и свободные энергии Гиббса образования хлороводорода (с учетом того, что в реакции участвует 2 моль):
Т/д свойства. | Н2+ Cl2= 2HCI® | 2HCI® = Н2+ Cl2 |
ДН0, кДж/моль. | 2 (-92,3) = -184,6. | 184,6. |
ДG 0, кДж/моль. | 2 (-95,27) = - 190,54. | 190,54. |
ДU° кДж/моль. | — 184,6. | 184,6. |
Величины для реакции разложения имеют обратный знак.
ДН° = ДU°
DU—+—p· DV—=—DH.
Так как в реакции не изменяется объем (число моль).
4. Вычислить число степеней свободы, которыми обладает система, состоящая из: раствора обеих солей (KN03 и NaN03) в присутствии льда и паров воды.
Число степеней свободы С определяется по основному уравнению фазового равновесия (правилу Гиббса):
С = К — Ф + n,.
где К — число независимых компонентов; Ф — число фаз; n — число внешних параметров.
Для данной системы число внешних параметров n = 1, так как давление постоянно (1,01 * 105Па).
Общее число компонентов 3 — вода и обе соли.
Число фаз Ф = 3 (пар, раствор и лед).
Рассчитываем число степеней свободы:
С = 3−3+1= 1.
Так как число степеней свободы (вариантность) определяет число параметров, которые можно изменять независимо друг от друга без изменения природы и числа фаз, то в данной системе при Р = const, можно изменять температуру или содержание солей.
5. Смесь камфоры и воды кипит при нормальном атмосферном давлении (101 325 Па) при 99 °C. Определить, в каком соотношении будут переходить вода и камфора в дистиллят. Молекулярный вес камфоры 152,2. Камфора практически не растворима в воде. Давление паров воды при 99 °C равно 97 740,9 Па
Решение:
Согласно закону Дальтона суммарное давление пара Р (общая упругость паров) определяется суммой парциальных давлений отдельных компонентов Давление, создаваемое парами камфоры, равно 101 325 — 97 740,9 = 3584,1 Па.
m (камф.)/ m (воды) = М (камф.)· Р (камф.)/ М (воды)· Р (воды).
m (камф.)/ m (воды) = 152,2· 3584,1/ 18· 97 740,9 = 0,3 (или 3: 10).
6. Вычислить при температуре 25 °C электродвижущую силу концентрационного серебряного элемента, в котором взяты 0,1 н и 0,01 н концентрации растворов нитрата серебра, если кажущиеся степени диссоциации растворов равны 81,4% и 93% соответственно
С учетом степени диссоциации концентрации ионов в растворах равны.
0,1· 0,814 = 0,0814 и 0,01· 0,93 = 0,093 моль Ag+ /дм3 соответственно.
Концентрационным называется элемент, электроды которого состоят из оного итого же материала (металла), помещенные в раствор его одной и той же соли разных концентраций. Электродный потенциал (Е) зависит от концентрации катионов металла в растворе. Эта зависимость выражается уравнением Нернста:
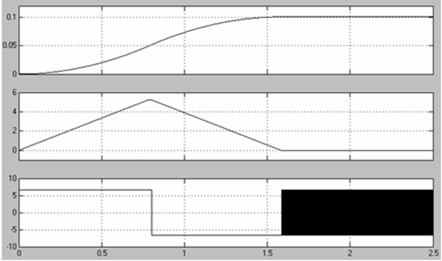
где Е° - стандартный электродный потенциал; n — число электронов, принимающих участие в процессе; С — молярная концентрация (при точных вычислениях — активность катионов металла в растворе. При использовании эквивалентной концентрации (нормальности) формула упрощается:
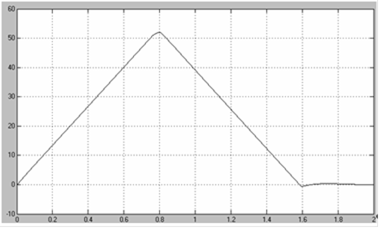
Для серебряного электрода:
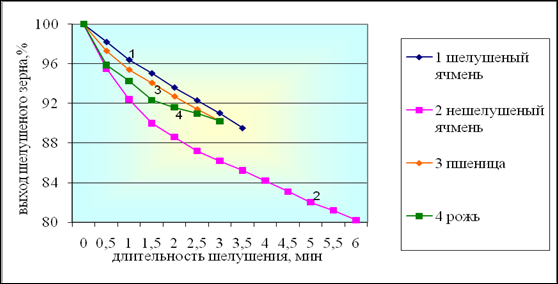

Электрод с более отрицательным потенциалом служит анодом, менее отрицательным — катодом Серебро Анод (-): Ag — e- = Ag+
Серебро Катод (+): Ag+ + e- = Ag.
Схема элемента:
Анод (-) Ag¦ Ag+ ¦ Ag+¦ Ag (+) Катод.
Электродвижущая сила Е= Еа — Ек = 0,739−0,735 = 0,04 В.
7. Разложение угольной кислоты при 310 К без катализатора характеризуется Еа = 86 кДж/моль, а в присутствии карбоангидразы Еа = 49 кДж/моль. Оцените, во сколько раз возрастает скорость реакции при использовании катализатора
Энергия активации и константа скорости связаны уравнением Аррениуса.
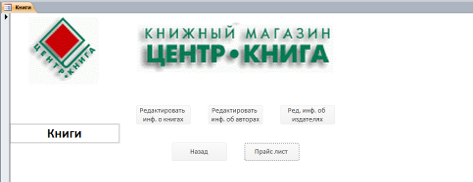
где lnВ — постоянная интегрирования.
ln K1 — ln K2 = ln K1 / ln K2 = (Е2 — Е1)/ R T.
ln K1 / ln K2 = (86 000−49 000)/ (8.314· 310) = 14.36.
K1 / K2 =1 716 650.
Во столько раз возрастет скорость реакции.
8. Что такое адгезия и когезия? Что такое краевой угол смачивания и как он определяется? Гидрофобные (лиофобные) и гидрофильные (лиофильные) поверхности?
энтальпия химический адгезия В коллоидной химии и других разделах физики и химии поверхностных явлений при анализе межфазовых взаимодействий часто используют понятия адгезии и когезии. Адгезия — связь между молекулами (атомами и ионами) разных фаз. Когезия — связь между молекулами (атомами и ионами) внутри тела в пределах одной фазы. Работу когезии Wk определяют как работу разрыва однородной гомогенной фазы с образованием двух новых поверхностей раздела этой фазы с ее собственным паром. В простейшем случае Wk равна обратимой работе разрыва столбика жидкости с единичной площадью сечения, т. е.:
Wk = 2жп
где множитель 2 указывает на образование двух новых одинаковых по вели-чине и свойствам поверхностей раздела ж/п. В итоге работу когезии можно рассматривать как меру межмолекулярного взаимодействия в объеме гомогенной конденсированной фазы.
Работа адгезии Wa, также отнесенная к единице поверхности, опреде-ляется как работа разрыва межфазного поверхностного слоя. В этом случае энергия затрачивается на образование двух поверхностей раздела, равных по величине, но разных по свойствам. Соответственно, изменения свободной энергии связаны с заменой свободной энергии исходной межфазовой границы на свободную энергию поверхностей фаз, граничащих с собственным паром. В системе ж/т работа адгезии Wa равна.
Wa = жп + тп — тж Работу адгезии можно рассматривать как меру интенсивности взаимодейст-вия двух разных контактирующих фаз, т. е. степени взаимного насыщения нескомпенсированных поверхностных сил, причем член тж определяет интенсивность остаточных нескомпенсированных связей (чем больше тж, тем меньше при прочих равных условиях величина Wa).
Wa /Wk = 0.5 (1 + Cos).
или.
Wa = жп (1+ Cos).
Уравнение удобно тем, что позволяет исключить трудно опреде-ляемые экспериментально величины тп и тж, в то время как значения жп и Cos измеряются довольно легко. Из уравнений следует, что величина Cos (краевой угол смачивания) характеризует степень родственности или, как говорят, фильности контактирующих фаз. Твердые тела, образующие с водой контактный угол < 90O, называют гидрофильными, и при < 90O — гидрофобными, а в более общем случае при контакте с произвольной жидкостью — соответственно, лиофильными или лиофобными (от греч. lyo-растворять, раствор, и phobos — бояться, страх или рhileo — любить). Например, полярные поверхности хорошо смачиваются водой и поэтому являются гидрофильными, а насыщенная неполярная поверхность углеводородов, особенно фторзамещенных, является гидрофобной.
Из уравнений) также следует:
при = 00 Cos = 1.0 Wa /Wk = 1.0 (полное смачивание),
900 > > 00 1> Cos > 0 0.5 < Wa /Wk < 1.0 (смачивание),
= 900 Cos = 0 Wa /Wk = 0.5 (равновесие).
1800> >900 0> Cos > -1 0 < Wa /Wk < 0.5 (несмачивание)
При равенстве работ когезии и адгезии контактный угол =00, а усло-вие Wa/Wk > 1.0 приводит к неограниченному растеканию (это же условие является необходимым условием последующего растворения). Движущую силу растекания определяют как разницу работ адгезии и когезии и назы-вают работой растекания.
Величина адгезии всегда больше нуля, т.к. между соприкасающимися фазами всегда имеется какое-либо, пусть очень небольшое межмолекулярное взаимодействие. Поэтому ситуация, когда Wa=0 и угол =1800, не возможна.