Количественное определение.
Растительные источники витаминов: стандартизация и медицинское применение

Определение содержания свободных органических кислот. Аналитическую пробу сырья измельчают до размера частиц, проходящих сквозь сито с отверстиями диаметром 2 мм. 25 г измельченных плодов шиповника помещают в колбу вместимостью 250 мл, заливают 200 мл воды и выдерживают в течение 2 ч на кипящей водяной бане, затем охлаждают, количественно переносят в мерную колбу вместимостью 250 мл, доводят… Читать ещё >
Количественное определение. Растительные источники витаминов: стандартизация и медицинское применение (реферат, курсовая, диплом, контрольная)
Методы количественного определения витаминов основаны на их физико-химических свойствах, таких как окислительно-восстановительные свойства, способность флуоресцировать в УФ-свете. Применяют различные методы определения: титрометрические, фотоколориметрические, спектрофотометрические, флуорометрические и др. [9].
Количественное определение витамина К.
Витамин К в листьях крапивы определяют методом СФМ (таблица 3).
Таблица 3. Количественное определение витамина K в листьях крапивы (авторский метод).
Этап определения. | Сущность. | Обоснование. |
Подготовительный. | Измельчение сырья и взятие точной навески. | Для лучшей экстракции. |
Экстракция. | Гексан. | Витамин K хорошо растворяется в органических растворителях. |
Очистка. | ТСХ (условия разделения в качественной хорматографии). | Для выделения витамина K. |
Количественное определение. | Обнаруженное пятно витамина K элюируют с хроматограммы и снимают оптическую плотность (СФМ). | Способность витамина K за счет системы двойных связей поглощать свет при определенной длине волны. |
Количественное определение БАВ в плодах шиповника.
Аскорбиновую кислоту можно определять титрометрическим методом, который основан на восстановлении 2,6-дихлорфенолиндофенола. С этим же реактивом можно провести фотоколориметрическое определение аскорбиновой кислоты. Для этого проводят экстракцию сырья 2% метафосфорной кислотой, добавляют раствор 2,6-дихлорфенолиндофенола. Через 35 сек. проводят фотоколориметрирование. Параллельно колориметрируют контрольный раствор 2% метафосфорная кислота с 2,6-дихлорфенолиндофенолом. Интенсивность окраски пропорциональна количеству аскорбиновой кислоты.
Количественное определение аскорбиновой кислоты можно провести фотоколориметрическим методом с помощью гексацианоферрита калия. В кислой среде аскорбиновая кислота восстанавливает гексацианоферрит калия до гексацианоферрата калия, который в присутствии ионов железа (Ш) образует берлинскую лазурь, с последующим ее фотоколориметрированием.
Метод количественного определения аскорбиновой кислоты (по ГФ XI, вып. 2, стр. 294) основан на ее способности окисляться до дегидроформы раствором 2,6-дихлорфенолиндофенолята и восстанавливать последний до лейкоформы. Точка эквивалентности устанавливается появлением розового окрашивания, которое свидетельствует об отсутствии восстановителя, т. е кислоты аскорбиновой (2,6-дихлорфенолиндофенол имеет в щелочной среде синее окрашивание, в кислой — красное, а при восстановлении обесцвечивается): [4].
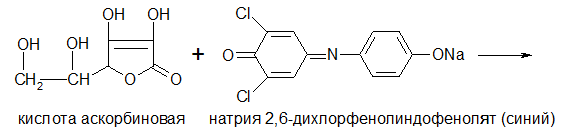

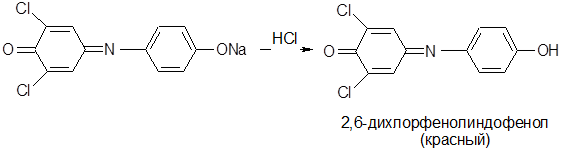
1. Определение содержания аскорбиновой кислоты. (таблица 4). Из грубо измельченной аналитической пробы плодов берут навеску массой 20 г, помещают в фарфоровую ступку, где тщательно растирают со стеклянным порошком (около 5 г), постепенно добавляя 300 мл воды, и настаивают 10 мин. Затем смесь размешивают и извлечение фильтруют. В коническую колбу вместимостью 100 мл вносят 1 мл полученного фильтрата, 1 мл 2%раствора хлористоводородной кислоты, 13 мл воды, перемешивают и титруют из микробюретки раствором 2,6-дихлорфенолиндофенолята натрия (0,001 моль/л) до появления розовой окраски, не исчезающей в течение 30−60 с. Титрование продолжают не более 2 мин. В случае интенсивного окрашивания фильтрата или высокого содержания в нем аскорбиновой кислоты [расход раствора 2,6-дихлорфенолиндофенолятанатрия (0,001 моль/л) более 2 мл], обнаруженного пробным титрованием, исходное извлечение разбавляют водой в 2 раза или более.
Содержание аскорбиновой кислоты в пересчете на абсолютно сухое сырье в процентах (X) вычисляют по формуле:

где 0,88 — количество аскорбиновой кислоты, соответствующее 1мл раствора 2,6-дихлорфенолиндофенолята натрия (0,001 моль/л), в граммах; V — объем раствора 2,6-дихлорфенолиндофенолята натрия (0,001 моль/л), пошедшего на титрование, в миллилитрах; m — масса сырья в граммах; W — потеря в массе при высушивании сырья в процентах.
Примечания. Приготовление раствора 2,6-дихлорфенолиндофенолята натрия (0,001 моль/л): 0,22 г 2,6-дихлорфенолиндофенолята натрия растворяют в 500 мл свежепрокипяченной и охлажденной воды при энергичном взбалтывании (для растворения навески раствор оставляют на ночь). Раствор фильтруют в мерную колбу вместимостью 1 л и доводят объем раствора водой до метки. Срок годности раствора не более 7 сут при условии хранения в холодном, темном месте.
Установка титра. Несколько кристаллов (3−5) аскорбиновой кислоты растворяют в 50 мл 2% раствора серной кислоты; 5 мл полученного раствора титруют из микробюретки раствором 2,6-дихлорфенолиндофенолята натрия до появления розового окрашивания, исчезающего в течение 1−2 нед. Другие 5 мл этого же раствора аскорбиновой кислоты титруют раствором калия йодата (0,001 моль/л) в присутствии нескольких кристаллов (около 2 мг) калия йодида и 2−3 капель раствора крахмала до появления голубого окрашивания. Поправочный коэффициент вычисляют по формуле:

где V — объем раствора калий йодата (0,001 моль/л), пошедшего на титрование, в миллилитрах; V1-объем раствора 2,6-дихлорфенолиндофенолята натрия, пошедшего на титрование, в миллилитрах.
2. Определение содержания свободных органических кислот. Аналитическую пробу сырья измельчают до размера частиц, проходящих сквозь сито с отверстиями диаметром 2 мм. 25 г измельченных плодов шиповника помещают в колбу вместимостью 250 мл, заливают 200 мл воды и выдерживают в течение 2 ч на кипящей водяной бане, затем охлаждают, количественно переносят в мерную колбу вместимостью 250 мл, доводят объем извлечения водой до метки перемешивают. Отбирают 10 мл извлечения, помещают в колбу вместимостью 500 мл, прибавляют 200−300 мл свеже-прокипяченной воды, 1 мл 1% спиртового раствора фенолфталеина, 2 мл 0,1% раствора метиленового синего и титруют раствором натра едкого (0,1 моль/л) до появления в пене лиловокрасной окраски.
Содержание свободных органических кислот в пересчете на яблочную кислоту в абсолютно сухом сырье в процентах (X) вычисляют по формуле:
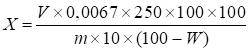
где 0,0067-количество яблочной кислоты, соответствующее 1 мл раствора натра едкого (0,1 моль/л), в граммах; V — объем раствора натра едкого (0,1 моль/л), пошедшего на титрование, в миллилитрах; m — масса сырья в граммах; W — потеря в массе при высушивании сырья в процентах. [1].
Таблица 4. Количественное определение аскорбиновой кислоты в плодах шиповника (фармакопейный метод).
Этап определения. | Сущность. | Обоснование. |
Подготовительный. | Измельчение сырья и взятие точной навески. | Для лучшей экстракции. |
Экстракция. | Водой. | Аскорбиновая кислота растворяется в воде. |
Очистка. | Не проводится. | Водорастворимые органические кислоты не обладают окислительно-восстановительными свойствами и не будут мешать определению аскорбиновой кислоты. |
Количественное определение. | Титрование 2,6-дихлорфенолиндофенолятом натрия до устойчивой розовой окраски. | Способность аскорбиновой кислоты к окислению. |
Количественное определение химических веществ в цветках календулы.
Каротиноиды определяют в лекарственном сырье фотоколориметрическим методом, основанном на измерении интенсивности их природной окраски. Разработан спектрофотометрический метод определения каротиноидов. Каротиноиды из сырья экстрагируют петролейным эфиром, затем хроматографируют на пластинке «Силуфол» в системе петролейный эфир-бензол-метанол (60:15:4), элюируют хлороформом и спектрофотометрируют при длине волны 464 нм (-каротин) при 456 нм (в-каротин). [19].
- 1. Около 1 г (точная навеска) измельченных цветков ноготков, просеянных сквозь сито с отверстиями размером 1 мм, помещают в коническую колбу вместимостью 250 мл, прибавляют 50 мл спирта 70%, колбу закрывают пробкой, взвешивают (с погрешностью ± 0,01 г) и оставляют на 1 ч. Затем колбу соединяют с обратным холодильником, нагревают, поддерживая слабое кипение в течение 2 ч. После охлаждения колбу с содержимым вновь закрывают той же пробкой, взвешивают и потерю в массе восполняют растворителем. Содержимое колбы тщательно взбалтывают и фильтруют через сухой бумажный фильтр, отбрасывая первые 20 мл, в сухую колбу вместимостью 200 мл (раствор А).
- 1 мл раствора, А помещают в мерную колбу вместимостью 25 мл, прибавляют 5 мл раствора алюминия хлорида, 0,1 мл кислоты уксусной и доводят объем раствора спиртом 96% до метки и оставляют на 40 минут (раствор Б).
Через 40 минут измеряют оптическую плотность испытуемого раствора Б и раствора стандартного образца Б 1 на спектрофотометре в максимуме поглощения при длине волны (408 + 2) нм в кювете с толщиной слоя 10 мм, используя растворы сравнения для испытуемого раствора и стандартного образцов.
Содержание суммы флавоноидов в процентах (Х) в пересчете на рутин вычисляется по формуле:
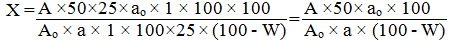
где: А — оптическая плотность испытуемого раствора;
Ао— оптическая плотность раствора стандартного образца рутина;
а — навеска сырья, г;
ао— навеска стандартного образца рутина, г;
W — влажность сырья, %;
Допускается проводить определение содержания суммы флавоноидов с использованием удельного показателя поглощения рутина.