Метод приготовления катализатора.
Метод активации катализатора

Прокаливание смешанных катализаторов приводит к образованию полимолибдатов, Мо03, СоМо04 или NiMo04, Со304, либо NiO, А12(Мо04)3, (х = 0.1 -1.0) и алюминатов Со или Ni. При низких температурах прокаливания кобальт находится преимущественно в октаэдрической координации. С содержанием кобальта именно в такой форме коррелирует активность катализатора после сульфидирования. С повышением температуры… Читать ещё >
Метод приготовления катализатора. Метод активации катализатора (реферат, курсовая, диплом, контрольная)
Приготовлению катализаторов гидроочистки, их формированию в условиях катализа и механизмам протекающих реакций посвящено огромное количество исследований (см., например, обзоры). Обычно применяют катализаторы, нанесенные на г-А12Оз или на углерод. Более высокую активность, чем катализаторы на основе г-А12Оз, проявляют катализаторы на з-А12Оз, что объясняется большей прочностью связи МоОз с этим оксидом алюминия и большей легкостью последующего сульфидирования.
Предшественником МоОэ является молибдат аммония (NH4)2Mo04. В кислой среде образуются полимолибдаты.
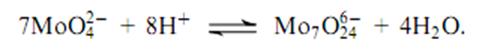
При высокой концентрации молибдата аммония происходит дальнейшая конденсация.
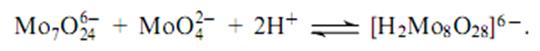
При рН > 7 полимолибдаты деконденсируются вновь образуя Мо042-. В этих кислотно-основных процессах участвует амфотерная по своей природе поверхность А1203.
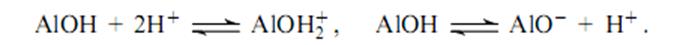
При получении катализаторов методом пропитки для образования полимолибдатных частиц необходимо поддерживать рН ниже изоэлектрической точки данного носителя (3−6 для А12Оз и ниже 2 для Si02). После пропитки катализатор сушат при 250−300°С и прокаливают на воздухе при 500−550°С. Дисперсность частиц МоО3 при этом мало изменяется. Исследования различными физическими методами (раман-спектроскопия, ИКС, EXAFS и др.) показали, что при типичных концентрациях МоО3 (10−12%) исходные молибдаты образуют с А1203 связи Al-O-Mo и имеют вид островков толщиной в два монослоя, состоящих из семи атомов молибдена.
Носитель можно пропитывать растворами гетерополисолей, например гетерополимолибдатов никеля или кобальта. Однако при этом из-за сильного взаимодействия ГПС с ОН-группами А12Оз предшественник не проникает в поры, и вместо равномерного имеет место «корочковое» распределение активного компонента на носителе. Для приготовления катализаторов используют и тиогетеро-анионы.
Другим методом приготовления Mo-Al-O-катализаторов является механическое смешение оксидов МоОз и А12Оз в присутствии воды при 400−500°С. Образующаяся система обладает практически такими же каталитическими свойствами, как контакт Мо03/А12O3, полученный пропиткой.
Второй компонент («промотор») наносят пропиткой носителя нитратами кобальта или никеля, причем последовательность пропитки может быть разной. Полагают, что повышению активности катализатора способствует пропитка носителя сначала солями молибдена, а потом кобальта. Но существует и противоположная точка зрения, согласно которой выгоднее сначала пропитывать носитель солями кобальта или одновременно осуществлять пропитку Сои Mo-содержащими соединениями. Ионообменное введение Со2+ или Ni2+ после нанесения молибдена лучше проводить при низких рН.
Двухстадийный метод приготовления катализатора предусматривает пропитку г-А12Оз в псевдоожиженном слое раствором (NH4)2Mo7024 при постоянном рН 7, прокаливание на воздухе при 500 °C, а затем пропитку нитратами никеля или кобальта до заполнения пор и новое прокаливание при 500 °C.
Активные катализаторы гидрирования получают с использованием тиосолей, например, пропиткой носителя смесью (NH4)2MoS4 и Ni (N03)2 или Co (N03)2 и последующим нагревом в смеси H2S + Н2 при 400 °C.
Ненанесенные Co-Mo-S-катализаторы получают, обрабатывая порошки МоОз и Со304 горячим раствором (NH4)2S или смешивая растворы Co (N03)2 и (NH4)2Mo7024, затем добавляют (NH4)2S, сушат и прокаливают. Во втором случае катализатор содержит больше лабильной серы, характеризуется более высокой дисперсностью фазы Co9S8 и активностью, но быстрее дезактивируется.
Имеются данные о том, что активность катализатора зависит от кислотности носителя. Это объясняют наличием поверхностных ОН-групп, способных взаимодействовать с солями молибдена и кобальта.
Прокаливание катализатора проводят при 400−600°С, когда соли полностью разлагаются, но еще не происходят нежелательные твердофазные реакции. Согласно данным, полученным различными физическими методами, после прокаливания Мо-Аl-катализаторов на поверхности А1203 появляется аморфная фаза Мо03 и возникают анионы типа (Мо7024)6-. Объемная фаза Мо03 при этом не образуется.
Прокаливание смешанных катализаторов приводит к образованию полимолибдатов, Мо03, СоМо04 или NiMo04, Со304, либо NiO, А12(Мо04)3, (х = 0.1 -1.0) и алюминатов Со или Ni. При низких температурах прокаливания кобальт находится преимущественно в октаэдрической координации. С содержанием кобальта именно в такой форме коррелирует активность катализатора после сульфидирования. С повышением температуры в результате внедрения в решетку А1203 образуется также тетраэдрический кобальт, который сульфидируется труднее. Поэтому прокаливание при температурах выше 600 °C нецелесообразно.
Никель при прокаливании приобретает октаэдрическую координацию и сильнее взаимодействует с решеткой А1203, чем кобальт. Существует мнение, что образование молибдатов никеля или кобальта или изополимолибдатов, удаляемых экстракцией водой, полезно для дальнейшего сульфидирования и образования смешанной NiMoили СоМо-фазы.
Введение
заранее приготовленного NiMo04 в Ni —Мо —Аl-матрицу позволяет увеличить активность катализатора.
Содержание активного компонента зависит от удельной поверхности носителя. Обычно на А1203 удается нанести от 8 до 15 мас.% молибдена, что соответствует удельной поверхности А1203, равной 250 м2*г-1. Отношение Со: Мо изменяется в пределах от 0.1 до 1.0. Соотношение между молибденом и кобальтом или молибденом и никелем зависит от последовательности пропитки. В наилучших катализаторах оно равно 2.
Активные катализаторы могут быть получены при разложении карбонилов кобальта и молибдена на носителе.
Максимальный эффект промотирования катализаторов СоМо/г-А1203 добавкой W03 достигается при отношении W: (W + Мо) = 0.25. Пропиткой носителя сначала раствором соли вольфрама, а потом раствором соли кобальта получают более активные катализаторы, чем при обратной последовательности пропитки. По данным ЭПР и РФЭС вольфрам способствует изменению координации молибдена от октаэдрической к тетраэдрической и облегчает его восстановление.
Сульфидирование катализаторов Мо/А1203 при низких температурах приводит к замещению атомов кислорода на серу.

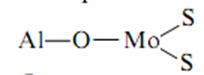
и образованию мостиковых связей Al-O-Mo-SH или Формирующиеся при этом частицы содержат по семь атомов Мо. Продолжительное сульфидирование при температуре выше 300 °C приводит к восстановлению Мо6+ в Мо4+ и к образованию, по данным электронной микроскопии плоских гексагональных частиц MoS2 размером менее 3 нм, удерживаемых на поверхности связями Мо — О — А1 и расположенных преимущественно перпендикулярно поверхности А1203. Имеются данные об образовании при неполном сульфидировании серосодержащих Со — Мо-гетерополисоединений.
При оптимальной температуре сульфидирования (400° С) связи Мо —О —Аl разрываются, а частицы MoS2 располагаются параллельно поверхности носителя и укрупняются, причем соотношение между базальными и боковыми гранями частицы остается постоянным. Однако ориентированного роста (эпитаксии) MoS2 на А1203 не происходит: частицы связаны между собой физическими силами. Чем меньше средние размеры частиц MoS2 и WS2, тем выше активность катализатора в процессах гидрообессеривания. Более высокая активность, по-видимому, достигается при неполном сульфидировании Мо03. Полное превращение кислородсодержащей поверхностной фазы в MoS2 происходит только при 970 °C, но при такой высокой температуре фаза MoS2 спекается.
По-видимому, природа носителя не очень влияет на конечные формы оксидов и сульфидов молибдена и вольфрама. Чаще оказывается, что Мо/С активнее, чем Мо/А1203. В молибденовом катализаторе, нанесенном на активный уголь, были обнаружены изолированные ионы молибдена или очень дисперсные частицы Мо03, которые на угле сульфидируются быстрее, чем на А1203: уже при 400 °C сульфидирование заканчивается. После сульфидирования MoS2 образует на А1203 пластинки, а на угле — трехмерные частицы. Это объясняется более сильным взаимодействием оксидного предшественника с поверхностью Аl2O3, чем с углеродом. Каталитическая активность MoS2 на угле выше, чем на оксиде алюминия.
Авторы работы наблюдали несколько иную ориентацию частиц MoS2 на носителе: на А1203 и Si02 ими были обнаружены пластинки, ориентированные перпендикулярно поверхности, а на ТЮ2 и Zr02 — плоские частицы. Каталитическая активность последних была выше.
Обработка системы Mo03/Si02 смесью H2S + Н2 при комнатной температуре приводит к образованию MoOxSj5 при 150 °C появляются частички MoS3, а при 250−270°С — фаза MoS2. В системе Co-Mo-S/Al203, по данным электронной микроскопии, образуются частицы MoS2, размер которых с ростом температуры сульфидирования увеличивается от 1 до 1.5 нм. Эти частицы связываются между собой в цепочки. При большом содержании кобальта образуется фаза Co9S8. В Ni-Mo-Sи Ni-W-S-катализаторах наряду со смешанными фазами наблюдалась также фаза NiS.
По данным ЯМР и EXAFS, основной активной фазой молибденсульфидного катализатора являются пластинки MoS2 с координацией Мо 4 или 5, по ребрам которых располагаются атомы Со. Образование сплошной фазы MoS2, происходящее, например, после длительной работы катализатора, приводит к дезактивации последнего. Такие же фазы, образующиеся на SiO2 и угле, менее прочно связаны с этими носителями, чем с А1203.
Для моделирования сульфидных катализаторов гидроочистки на грань Мо (110) наносили несколько слоев серы и затем напыляли Zn или Со. Оказалось, что цинк и кобальт ускоряют сульфидирование молибдена. Была отмечена корреляция между гидродесульфирующей активностью катализаторов и легкостью сульфидирования молибдена. В присутствии цинка или кобальта атомы Мо становятся координационно-ненасыщенными.