Гастрит.
Болезни желудка

Лимфоцитарный (вариолоформный, или хронический эрозивный) гастрит. Характерна инфильтрация лимфоцитами исключительно покровно-ямочного эпителия: примерно 30 лимфоцитов на 100 эпителиоцитов (при хеликобактерном гастрите 7−10 на 100 эпителиоцитов), тогда как в собственной пластинке слизистой оболочки лимфоциты немногочисленны. Эндоскопически при этом на высоте складок видны узелки с изъязвлённой… Читать ещё >
Гастрит. Болезни желудка (реферат, курсовая, диплом, контрольная)
Гастрит — воспаление слизистой оболочки желудка. По характеру течения выделяют острый и хронический гастрит.
Острый гастрит Это кратковременное заболевание обычно протекает бессимптомно, реже сопровождается болями в эпигастрии, тошнотой, рвотой, иногда признаками желудочного кровотечения.
Причины острого гастрита разнообразны: недоброкачественная пища, употребление суррогатов алкоголя, противоопухолевых химиопрепаратов, ожог кислотами и щелочами, а также уремия, системные инфекции (например, сальмонеллёз), шок, тяжёлый стресс.
Механизм повреждения слизистой оболочки желудка может быть общим или различным для нескольких этиологических факторов. Ацетилсалициловая кислота, например, не диссоциирует на ионы, а всасывается путём пассивной неионной диффузии. При нейтральном значении pH внутри клеток покровного эпителия желудка ацетилсалициловая кислота переходит в ионную форму, разрушает клетки и создаёт условия для повреждающего действия кислотно-пептического фактора. Ацетилсалициловая кислота и другие нестероидные противовоспалительные препараты препятствуют синтезу простагландинов, что снижает сопротивляемость слизистой оболочки желудка. Нарушения кровотока при шоке приводят к развитию микроинфарктов, чувствительных к действию кислотно-пептического фактора. Многие перечисленные выше причины способствуют нарушению секреторной функции эпителиоцитов, повреждению слизистого барьера и последующей обратной диффузии водородных ионов.
Различают несколько видов гастрита.
- ? По распространённости: диффузный или очаговый.
- ? По топографии: антральный, фундальный, пилороантральный, пилородуоденальный.
- ? По морфологии выделяют следующие формы острого гастрита: катаральный, фибринозный, гнойный (флегмонозный), некротический (коррозивный).
- ? Катаральный гастрит. Макроскопически слизистая оболочка желудка утолщена, с высокими гиперемированными складками, покрытыми густой вязкой слизью. Иногда на высоте складок видны точечные кровоизлияния и мелкие дефекты конической формы, их дно и края окрашены в чёрный цвет (эрозии). При гистологическом исследовании слизистая оболочка покрыта серозно-слизистым экссудатом с примесью нейтрофилов и слущенного покровного эпителия. В собственной пластинке слизистой оболочки — отёк, полнокровие сосудов, диапедезные кровоизлияния и незначительная нейтрофильная инфильтрация.
- ? Фибринозный гастрит. На поверхности слизистой оболочки желудка желтовато-серая или жёлто-коричневая плёнка. Эта плёнка либо рыхло фиксирована и легко отторгается (крупозный гастрит), либо прочно прикреплена, при попытке её отделить обнажаются язвенные дефекты (дифтеритический гастрит).
- ? Гнойный (флегмонозный) гастрит крайне редок и осложняет травмы, опухоли (перитуморозный) или язвы (периульцерозный). Макроскопически стенка желудка утолщена, складки сглажены, покрыты гноевидной зеленовато-жёлтой пленкой. Микроскопически выражена диффузная инфильтрация всех слоёв стенки нейтрофилами, иногда с колониями микроорганизмов. Выражен лейкопедез эпителия (проникновение лейкоцитов в эпителиоциты). Процесс может переходить на брюшину с развитием перигастрита и перитонита.
- ? Некротический (коррозивный) гастрит обычно развивается при попадании в желудок кислот, щелочей и других препаратов, разрушающих слизистую оболочку. Некроз захватывает поверхностные отделы слизистой оболочки или всю стенку желудка и по характеру может быть коагуляционным и колликвационным. При отторжении некроза обнажаются эрозии и/или язвы. При острых язвах нередко возникает перфорация стенки желудка.
Исходы и осложнения острого гастрита. При катаральном гастрите обычно наступает полное выздоровление и восстановление слизистой оболочки. Крайне редко процесс затягивается, и гастрит переходит в хронический. При остальных формах сохраняется значительная атрофия слизистой оболочки и деформация стенки желудка. Эрозивный и некротический гастриты могут дать профузное кровотечение, перфорацию стенки желудка. При флегмонозном гастрите возникает перигастрит, медиастинит, гнойный плеврит, поддиафрагмальный абсцесс, тромбофлебит крупных вен, пилефлебитические абсцессы печени.
Хронический гастрит Это широко распространённое заболевание. Полагают, что половина населения земного шара страдает хроническим гастритом.
Этиология. В развитии гастрита основную роль играют экзогенные и эндогенные факторы. Экзогенные факторы: хроническое нарушение режима и ритма питания, воздействие химических, термических, механических агентов, радиации, длительного приёма нестероидных противовоспалительных препаратов, алкоголя. Последний в больших концентрациях подавляет секрецию соляной кислоты, пепсиногена и нарушает защитный барьер слизистой оболочки желудка, что приводит к повышенной обратной диффузии водородных ионов и увеличению потери белка.
Эндогенные факторы: аутоинтоксикация (например, при уремии и хронической сердечно-сосудистой недостаточности), механические причины, включающие обструкцию привратника (например, рубцовую), безоары (пищевые камни) и атонию желудка. Хронический гастрит развивается при амилоидозе, гранулематозных болезнях, после резекции желудка или наложения гастроэнтероанастомоза, когда происходит рефлюкс (заброс) дуоденального содержимого в желудок. Иногда причиной хронического гастрита становится аутоиммунизация, когда у больных обнаруживают аутоантитела к париетальным клеткам и к внутреннему фактору Кастла.
Однако в возникновении большинства случаев хронического гастрита главную роль играет Helicobacter pylori (H. pylori). Открытие H. pylori австралийскими гастроэнтерологами B.J. Mаrshall и R. Warren (1983 г.) совершило переворот в гастроэнтерологии. Сейчас этиологическая роль H. pylori в развитии гастрита признана и зафиксирована в Международной классификации хронического гастрита (Сидней, 1990 г.; Хьюстон, 1994 г.). B.J. Mаrshall и R. Wаrren в 2005 г. были удостоены Нобелевской премии.
Helicobacter pylori — грамотрицательная неспорообразующая S-образная бактерия с пятью подвижными жгутиками на одном конце. Обычно H. pylori располагается в пилорическом отделе желудка под слоем слизи, где pH нейтрально, может с помощью уреазы расщеплять мочевину до аммиака и углекислого газа и нейтрализовывать соляную кислоту. H. pylori вырабатывает супероксиддисмутазу и каталазу, предохраняющие от фагоцитоза, и, кроме того, фосфолипазы, А и С. Благодаря спиралевидной форме, жгутикам и фосфолипазам, бактерия преодолевает слой слизи на поверхности эпителия, повреждая то и другое. С помощью лептинов и фактора колонизации происходит адгезия бактерии к эпителиоциту желудка.
Распространение инфекции H. pylori носит глобальный характер. Масштабы колонизации возбудителя впечатляют: в настоящее время заражено H. pylori около трёх миллиардов человек. В странах Западной Европы H. pylori обнаруживают у половины населения старше сорока лет, в Латинской Америке — у 70−90% взрослых, в Азии — 40−80%, в Санкт-Петербурге — 46%, у пострадавших от аварии на Чернобыльской атомной электростанции инфицированность лиц старше 35 лет составляет 95−100%, детей до 7 лет — 50%. Доказано, что в развитых странах инфицирование происходит в детском возрасте (до 7−10 лет) и достигает 20−25%, такой уровень сохраняется и у взрослых. Напротив, в развивающихся странах в популяциях с низким доходом инфицирование H. pylori происходит и в детском, и в подростковом возрасте, достигая у взрослых 50−70%.
Однако большинство инфицированных лиц не болеют гастритом и никогда не заболеют ЯБ. Речь идет о типичном представителе желудочно-кишечной флоры, попадающим в организм фекально-оральным или орально-оральным путем во время эндоскопического исследования, при тесном контакте с домашними животными (кошки, собаки, свиньи) или через нестерильные приборы при стоматологическом обследовании.
Существуют особые патогенные типы возбудителя. Выделены штаммы H. pylori, способные вырабатывать вакуолизирующий цитотоксин и цитотоксин-ассоциированный белок VacА и CagA (I тип), и штаммы, не вырабатывающие ни то, ни другое (II тип). Бактерии I типа имеют гены vacA и cagA и продуцируют вакуолизирующий токсин; бактерии II типа имеют только ген vacA (гена cagA нет), однако соответствующий белок не вырабатывают. Адгезивные свойства микроорганизма неодинаково выражены у различных штаммов H. pylori. Наиболее сильно этот феномен выражен у штаммов I типа. Белок CagA через экспрессию гена и синтез матричной РНК стимулирует секрецию ИЛ-8, по уровню последнего и определяют адгезивные свойства бактерии.
Согласно современным представлениям, H. pylori нарушает нормальные процессы регенерации желудочного эпителия, таким образом, микроорганизм прямо или косвенно отвечает за дисрегенераторные процессы, являющиеся важной составляющей в патогенезе гастрита. H. pylori оказывает влияние и на пролиферацию, и на апоптоз эпителиоцитов слизистой оболочки желудка. Нарушение процессов клеточного обновления в слизистой оболочке желудка лежит в основе морфогенеза атрофии при гастрите.
Существует множество методов выявления H. pylori. «Золотой стандарт» диагностики H. pylori — морфологическое исследование с окраской препаратов по Гимзе. Обычно бактерии располагаются в слизи, покрывающей эпителий, на высоте и по краям валиков, иногда непосредственно около эпителиоцитов. Однако внутрь эпителия они не проникают. В участках тесной близости эпителиальная клетка своей апикальной частью образует своеобразное выпячивание, хорошо видимое на электронной микрофотографии, названное Tytgat C.N.J. «адгезивным пьедесталом». Обычно видны спиралевидные структуры бактерии, хотя она может иметь и кокковую форму.
В гастробиоптатах H. pylori выявляют иммуногистохимически с использованием моноклональных антител против H. pylori. Особое значение придают молекулярной диагностике, особенно ПЦР, позволяющей идентифицировать фрагмент ДНК H. pylori, проводить типирование бактерий по уже известным генам сagA, vacA и недавно открытым новым генам iceA, babА.
Патогенез хронического гастрита. С учётом механизма развития выделено несколько основных форм: гастрит типа А, В и С.
Аутоиммунный гастрит, или гастрит типа, А — крайне редкое заболевание, в популяции его находят менее чем у 1%, в структуре хронических гастритов — около 10%. У больных аутоиммунным гастритом в крови и в желудочном соке обнаруживают два типа аутоантител: антитела к липопротеину микроворсинок секреторных канальцев париетальной клетки и антитела к внутреннему фактору, блокирующие его связывание с витамином В12. Антитела к париетальным клеткам направлены против Н+, К+-зависимой АТФазы, катализирующей образование соляной кислоты. Разрушение желёз и атрофия слизистой оболочки приводят к прекращению выработки соляной кислоты (гипоили ахлоргидрия). При этом также прекращается продукция внутреннего фактора, снижение его продукции нарушает всасывания витамина В12 и ведёт к развитию пернициозной анемии. Гастрит типа, А — генетическое заболевание. Оно наследуется по аутосомно-доминантному типу и нередко сочетается с такими аутоиммунными заболеваниями, как тиреоидит Хашимото, сахарный диабет I типа, болезнь Аддисона. Учитывая локализацию париетальных клеток, аутоиммунный гастрит всегда поражает тело желудка (фундальный гастрит). Здесь развиваются диффузные атрофические изменения с элементами воспаления, тогда как антральный отдел остается непоражённым. Снижение секреции соляной кислоты нарушает отрицательную обратную связь париетальных клеток и G-клеток, возникает гиперплазия последних, что ведёт к развитию гастринемии.
Бактериальный гастрит, или гастрит типа В — антральный поверхностный гастрит. Однако со временем процесс поднимается выше, гастрит становится не только антральным, но и фундальным. Причина его развития — инфекция, вызванная H. pylori, основную роль играет штамм возбудителя и наличие вакуолизирующего токсина.
Механизм действия vacA расшифрован. Его мишень —АТФаза v-типа эпителиальных клеток, она присутствует в поздних эндосомах, сливающихся друг с другом после контакта с цитотоксином. АТФаза — протонный насос, создающий после стимуляции цитотоксином кислую среду внутри вакуолей. Вещества, поступающие извне в вакуоли (например, аммиак), теряют способность выхода через мембраны и накапливаются внутри вакуолей. После протонирования они осмотически притягивают воду, вакуоли, увеличиваясь в размерах и количестве, «разбухают», сливаются друг с другом, разрывают клеточную мембрану, и клетка погибает. Вакуолизирующий цитотоксин, помимо повреждения клетки, тормозит клеточную пролиферацию и стимулирует высвобождение пепсиногена. Адгезия H. pylori, как и в случае любой бактериальной инфекции, немедленно вызывает сигнальную трансдукцию и реорганизацию цитоскелета эпителиоцитов, отвечающих на это продукцией цитокинов: ИЛ-8 и некоторых других хемокинов. Эти цитокины вызывают миграцию лейкоцитов из кровеносного русла, в результате развивается активная стадия воспаления. Активированные макрофаги секретируют ИФ-б и ФНО-г, активирующие рецепторы лимфоидных, эпителиальных и эндотелиальных клеток, что, в свою очередь, привлекает в слизистую оболочку новые клетки, участвующие в иммунных и воспалительных реакциях. Метаболиты активного кислорода нейтрофилов оказывают дополнительное повреждающее действие на эпителиоциты желудка. При этом сам H. pylori, благодаря каталазе и супероксиддисмутазе, недоступен для фагоцитоза, а полиморфно-ядерные лейкоциты, наоборот, часто гибнут. Хронический гастрит — диффузная лимфоплазмоцитарная инфильтрация. При наличии лейкоцитов гастрит становится активным.
Рефлюкс-гастрит, или гастрит типа C развивается при забросе (рефлюксе) дуоденального содержимого в желудок. В двенадцатиперстной кишке, где идет процесс переваривания и всасывания жиров, лецитин под действием поступающих из поджелудочной железы трипсина и фосфолипазы, А превращается в лизолецитин. Основной механизм развития гастрита типа С — цитотоксическое действие на слизистую оболочку желудка лизолецитина. При рефлюкс-гастрите H. pylori выявляют редко, не более чем в 15%. случаев, секреция соляной кислоты обычно не нарушена, количество гастрина в пределах нормы. Доля рефлюкс-гастрита в структуре заболеваемости хроническими гастритами незначительна.
Помимо названных выше, в модифицированной Сиднейской Системе выделены особые формы хронического гастрита: лимфоцитарный, радиационный, гранулематозный, эозинофильный, коллагеновый, гипертрофический и др. Патогенез в каждом случае свой, причем не всегда ясный. Терминология не очень удачна, так как часть гастритов названа по морфологическому принципу, часть — по этиологическому.
- ? Лимфоцитарный (вариолоформный, или хронический эрозивный) гастрит. Характерна инфильтрация лимфоцитами исключительно покровно-ямочного эпителия: примерно 30 лимфоцитов на 100 эпителиоцитов (при хеликобактерном гастрите 7−10 на 100 эпителиоцитов), тогда как в собственной пластинке слизистой оболочки лимфоциты немногочисленны. Эндоскопически при этом на высоте складок видны узелки с изъязвлённой поверхностью. Лимфоцитарный гастрит составляет около 4,5% всех гастритов. Локализация его также отличается от остальных форм: в 76% — пангастрит, 18% — фундальный и только в 6% — антральный (неспецифический гастрит в 91% случаев — антральный). Этиология и патогенез неизвестны. H. pylori выявляют гораздо реже, чем при гастрите типа В, однако антитела к H. pylori обнаруживают почти всегда, в половине случаев в сочетании с целиакией. Скорее всего, лимфоцитарный гастрит — следствие глубоких нарушений иммунной системы слизистых оболочек, а H. pylori — фактор, провоцирующий развитие заболевания.
- ? Эозинофильный гастрит. Ярко выражена эозинофильная инфильтрация иногда только слизистой оболочки, иногда всех слоёв стенки желудка. Подобные изменения обнаруживают при болезни Крона, паразитарных поражениях желудка, иногда при язве и раке. У 25% больных в анамнезе аллергия, бронхиальная астма, экзема. По течению гастрит может быть острым или хроническим рецидивирующим. Кроме того, эозинофильный гастрит бывает проявлением эозинофильного гастроэнтерита. У больных склеродермией, дерматомиозитом эозинофилии крови нет, эозинофильный инфильтрат сочетается с тучными клетками, особенно выражен в глубоких слоях стенки желудка и завершается массивным фиброзом мышечной пластинки.
- ? Гранулематозный гастрит. Характерно наличие в слизистой оболочке желудка эпителиоидноклеточных гранулём, нередко с гигантскими многоядерными клетками. Подобные гранулёмы находят при саркоидозе, болезни Крона, туберкулёзе, микозах, отравлении бериллием, инородных телах и др. При саркоидозе антральный гранулематозный гастрит встречается в 10% случаев, при болезни Крона — в 7%. Однако в гастробиоптатах гранулёмы выявляют гораздо реже. Вблизи инородных тел значительно чаще, в 10−29% возникают другие, гигантоклеточные гранулёмы.
- ? Коллагеновый гастрит отличается отложением коллагена под покровным эпителием желудка в виде тяжей толщиной до 20−30 мкм. В эпителии находят очаговые повреждения и повышенное количество интерэпителиальных лимфоцитов. В кишечнике подобные изменения обозначают как коллагеновая спру и коллагеновый колит. Этиология и патогенез заболевания неизвестны. Предполагают участие иммунных механизмов, нарушающих функцию перикриптальных фибробластов и их обновление.
- ? Гипертрофическая гастропатия (гипертрофический гастрит) наиболее интересна. Характерна гипертрофия слизистой оболочки желудка и образование гигантских складок, напоминающих клубок змей. В основе подобных изменений лежит не воспаление, как ошибочно полагали раньше, а гиперплазия покровно-ямочного и/или железистого эпителия. Выделено три типа гипертрофической гастропатии: мукозный, гландулярный и смешанный.
Клинически для гипертрофической гастропатии характерны следующие синдромы:
болезнь Менетрие;
синдром Золлингера-Эллисона;
гипертрофическая гиперсекреторная гастропатия с потерей и без потери белка.
Структура заболеваемости хроническим гастритом неоднородна, 90% составляет бактериальный гастрит типа В.
Морфогенез хронического гастрита. Постоянное раздражающее действие на слизистую оболочку желудка различных экзогенных и эндогенных факторов, уреазы H. pylori, лизолецитина жёлчи или аутоантител неизбежно активизирует кислотно-пептические факторы агрессии желудочного сока. Это нарушает, в первую очередь, регенерацию эпителия и проявляется различными вариантами.
Темпы регенерации эпителия возрастают. Прежде всего, укорачивается фаза дифференцировки эпителия: не достигнув степени зрелости, молодые недифференцированные эпителиоциты подвергаются инволюции. Наибольшие изменения происходят в специализированных клетках желёз, что выявляется на электронограммах. Главные клетки содержат единичные зимогенные гранулы с незрелым мукоидом. Цитоплазма их загустевает за счёт слияния мелких гранул, содержащих секрет, близкий по структуре к секрету слизистых клеток. В париетальных клетках видны признаки преждевременной инволюции: редукция крист и просветление матрикса митохондрий, отложение липидов и миелиноподобных структур, обилие крупных вторичных лизосом; тубуловезикулы отсутствуют, хорошо развит лишь аппарат Гольджи и эндоплазматическая сеть.
Незрелые клетки из ямочно-шеечной области (естественной их локализации) устремляются вверх и вниз. Гистоавторадиографический метод позволяет увидеть незрелые ДНК-синтезирующие клетки на вершине валиков и даже в теле желёз. Преобладают добавочные (слизистые) клетки, они начинают занимать в железах отделы, предназначенные для париетальных и главных клеток. Таким образом, транслокация слизистых клеток завершается уменьшением количества специализированных гландулоцитов, вырабатывающих основные ингредиенты желудочного сока — соляную кислоту и пепсиноген. В то же время покровный эпителий с явными признаками недоразвития гораздо дольше остается на валиках, не подвергаясь апоптозу в установленные сроки.
Процесс апоптоза извращён, что особенно характерно для инфекции H. pylori: если в норме около 2−3% клеток желудка находятся в состоянии апоптоза, то при инфекции H. pylori их количество возрастает до 8%, при этом апоптозные тельца выявляют не только на поверхности валиков, но и по всей длине железы.
При хроническом гастрите, наряду с характерным для каждого отдела желудка эпителием, нередко появляется эпителий, не свойственный этому отделу, т. е. происходит структурная перестройка эпителия или метаплазия. Возможны два варианта метаплазии.
- ? Пилорическая метаплазия в области фундальных желёз, при ней в теле желудка появляются железы, напоминающие слизистые, или пилорические (псевдопилорические железы Штерка).
- ? Кишечная метаплазия, когда слизистая оболочка желудка внешне напоминает слизистую оболочку кишки с характерными ворсинками вместо валиков, выстланными каёмчатыми энтероцитами, бокаловидными клетками с наличием клеток Панета (полная, или тонкокишечная метаплазия). Иногда эпителиальные клетки напоминают колоноциты, бокаловидных клеток много, а клетки Панета отсутствуют (неполная, или толстокишечная метаплазия). Именно этот эпителий может при определённых условиях малигнизироваться: желудочный эпителий, в норме всасывающий лишь алкоголь, в очагах кишечной метаплазии всасывает липиды. Однако система дренирования отсутствует, и растворимые в липидах канцерогены депонируются в стенке желудка, вызывая переход метаплазии и дисплазии в рак. Выражением крайнего извращения регенерации при хроническом гастрите являются «клетки-химеры», или «клетки-миксты», их характерная особенность — наличие в одной клетке ультраструктурных признаков сразу нескольких высокоспециализированных зрелых клеток. Например, бывают клетки, сочетающие элементы париетальной (внутриклеточные канальцы) и главной (зимогенные гранулы) клеток или главной клетки и покровного эпителия (мукоид).
Основные процессы морфогенеза хронического гастрита — нарушение и извращение регенерации. Они неизбежно заканчиваются атрофией железистого аппарата желудка. Хронический гастрит — прежде всего, дисрегенераторный процесс. Наряду с нарушенной регенерацией, видны воспалительные (инфильтрация собственной пластинки лимфоцитами, плазмоцитами), склеротические (разрастание соединительной ткани) и атрофические изменения (вытеснение участками склероза железистого аппарата желудка).
Классификация хронического гастрита, помимо этиологии и патогенеза заболевания, учитывает топографию процесса, морфологические типы гастрита, активность процесса, наличие и выраженность метаплазии эпителия.
- ? По топографии различают три варианта хронического гастрита: антральный, фундальный и пангастрит.
- ? По морфологии выделяют поверхностный (неатрофический) и атрофический гастрит.
- ? Хронический поверхностный гастрит. Слизистая оболочка желудка обычной толщины. Покровный эпителий с дистрофическими изменениями. Собственная пластинка слизистой оболочки инфильтрирована лимфоцитами и плазматическими клетками. Инфильтрат обычно располагается в поверхностных отделах на уровне валиков. В период обострения в инфильтрате и эпителии появляются полиморфно-ядерные лейкоциты (рис. 13−3а).
Д Прогноз поверхностного гастрита благоприятный. Заболевание длится много лет, возможно обратное развитие.
Д При H. pylori-ассоциированном антральном поверхностном гастрите в биоптатах и мазках-отпечатках при окраске по Гимзе выявляется H. pylori. После лечения антибактериальными препаратами и уничтожения бактерии H. pylori (эрадикация) в слизистой оболочке желудка происходит восстановление ультраструктуры клеток, из инфильтрата исчезают полиморфноядерные лейкоциты.
? Хронический атрофический гастрит отличается от поверхностного появлением атрофии. Слизистая оболочка истончена, её рельеф сглажен. Валики укорочены, плоские, но могут быть и в виде микропапиллярных разрастаний. Ямки углублены, штопорообразные. Покровно-ямочный эпителий уплощён. Главная клинико-морфологическая черта — не истончение слизистой оболочки, а уменьшение числа специализированных гландулоцитов, обеспечивающих секреторную функцию желудка, и замена их на более примитивные мукоциты. Последние при выраженной атрофии полностью вытесняют париетальные и главные клетки. Железы укорочены, количество их уменьшено. В собственной пластинке — поля склероза и полиморфноклеточный инфильтрат на месте бывших желёз. Помимо типичного покровно-ямочного и железистого эпителия нередко возникают очаги полной или неполной кишечной метаплазии, а также дисплазии эпителия (рис. 13−3б).
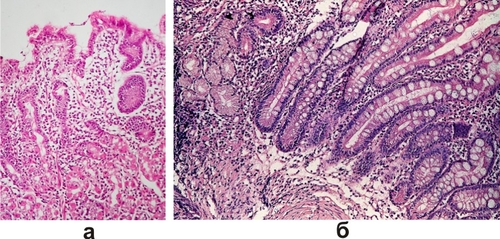
Рис. 13−3. Хронический гастрит: а — хронический поверхностный гастрит; б — хронический атрофический гастрит с перестройкой эпителия по кишечному типу. Окраска гематоксилином и эозином (x200).
Хронический атрофический гастрит — заболевание, длительно текущее без регресса атрофических изменений и сопутствующей кишечной метаплазии, т.к. механизмы, препятствующие обратному развитию атрофии, обусловлены изменением фенотипа эпителиоцитов в сторону уменьшения способности к апоптозу.
Прогноз. Хронический атрофический гастрит — предраковое заболевание желудка, поскольку на фоне тяжёлой дисплазии эпителия может развиться рак.