Технологии получения липосом

Установлено, что в ходе сушки с использованием соответствующих концентраций сахаров, до определенной степени снижается уровень слияния и агрегации липосом при образовании аморфной стеклоподобной массы (Crowe et al., Arch. Biochem. Biophys., 242 (1985) 240−247), а также взаимодействие сахаров с основной группой фосфолипидов (Crowe et al., Cryobiology, 31 (1994) 355−366). В ранних исследованиях… Читать ещё >
Технологии получения липосом (реферат, курсовая, диплом, контрольная)
Для получения липосом известны различные способы. Так, например, они могут быть получены способом дегидратации/регидратации, в соответствии с которым липид растворяют в органическом растворителе, таком как хлороформ, дихлорметан или спирт, такой как метанол или этанол. Затем раствор высушивают с использованием, например, роторного испарителя, после чего на стенке испарительной колбы образуется пленка липида. Добавление к сухой пленке воды или водного раствора, такого как буфер, приводит к образованию многослойных липосом. Образованием именно этого продукта завершается первая стадия образования везикул с использованием различных методик. Последующая обработка может приводить к дегидратации/регидратации везикул, или ДРВ (DRV) (Kirby and Gregoriadis, Biotechnology (1984) 2, 979−984). Альтернативно, при последующей обработке ультразвуком липидной суспензии получают однослойные липосомы (A.D.Bangham et al., J. Mol. Biol. 13, 238 (1965)).
Другие известные в технике способы включают детергентную обработку (Y. Kagawa et al., J. Biol. Chem. (1971) 246, 5477), выпаривание с обращением фаз (F. Szoka and D. Рараhadjopoulos, Proc. Natl. Acad. Sci, USA (1978) 75, 4194) и введение эфира (D.Deamer et al., Biochim. Biophys. Acta, (1976) 433, 629), а также лиофилизацию (см., например, работу Ohsawa et al., Chem. Pharm. Bull, (1984) 32, 2442−5 and Kirby and Gregoriadis (1984) supra.) и методы замораживания — оттаивания (D.D.Lasic «Liposomes: From Physics to Application, Elsevier, 1993, p. 98).
В зависимости от применяемого для образования липосом способа получают липосомы разного размера и с различающимися характеристиками. Липосомы могут использоваться для инкапсулирования материалов, таких как биологически активные продукты, в частности фармацевтические средства, включая вакцины, а также нефармацевтические средства, такие как продукты, воздействующие на кожу, в частности препараты для искусственного загара и другие средства макияжа. Методики инкапсулирования варьируют в зависимости от природы инкапсулируемого реагента и размера и свойств образованных липосом.
Размер липосом важен с точки зрения их применения. В некоторых случаях нужны крупные липосомы, в тех случаях, например, когда инкапсулируются частицы, включающие микроорганизмы, такие как бактерии, для получения, например, вакцин, как описано в документе WO 95/9 619.
Однако во многих случаях предпочтительны мелкие липосомы. Это связано с тем, что мелкие липосомы не так быстро удаляются ретикуло-эндотелильной системой (РЭС), и в меньшей степени, чем крупные липосомы (с размерами свыше 200 нм). Захват везикул в РЭС возрастает с увеличением их размера. Кроме того, крупные липосомы при их внутримышечной инъекции не способны эффективно достичь регионарных лимфатических узлов и доставить в них вакцины и другие средства (Gregoriadis G., Liposomes as Drug Carriers: Recent Trends and Progress, Wiley Chichester, 1988).
Липосомные препараты, содержащие различные лекарственные средства, могут быть оптимизированы с точки зрения содержания лекарственного ингредиента, стабильности, картины биологического распределения и уровня поступления в клетку путем изменения физико-химических параметров липосом, таких как температура фазового перехода, размер липосом, характер распределения препарата по размеру, величина поверхностного заряда, гидратация поверхности соединениями, несущими гидрофильные группы, и характер распределения по размеру частиц.
Размер липосом представляет собой параметр, который определяет фракцию, захватываемую РЭС (Senior et al., Biochem., Biophys., Acta (1985) 839. 1−8: Nagayasu et al., Biol. Pharm. Bull. (1995) 18 (7), 1020−1023). Мелкие липосомы могут быть получены при использовании гомогенизаторов под высоким давлением (Talsma et al., Drug Development and Industrial Pharmacy (1989) 15 (2) 197−207, Vemuri S. et al., Drug Development and Industrial Pharmacy (1990) 16 (15), 2243−2256), но при этом используют большие количества липидов, для того чтобы добиться приемлемой величины коэффициента отношения включенного лекарственного средства к липидной массе. При использовании другого подхода (Gresoriadis et al., Int. J. Pharm. 65 (1990) 235−242) в псевдоожиженном слое многослойных дегидратированных-регидратированных везикул (ДРВ) в присутствии неинкапсулированного лекарственного средства получают везикулы с размером менее 200 нм, сохраняющие количество первоначально включенных растворенных веществ.
Показан стабилизирующий эффект на везикулы, возникающий при добавлении сахара после получения липосом (Crowe L.M. et al., Arch. Biochem. Biophys. 242 (1985) 240−247, Hauser et al., Biochem. Biophys. Acta (1987) 897, 331−334), в том случае, например, когда липосомы, содержащие лекарственное средство, лиофильно высушивают для хранения и затем подвергают повторной гидратации.
Предлагается способ получения липосомного препарата, содержащего реагент, который включает следующие стадии:
- (1) образование пустых липосом;
- (2) смешивание липосом, полученных на стадии (1), с раствором сахара и указанного реагента и
- (3) высушивание смеси, полученной на стадии (2).
При повторной гидратации высушенного материала, полученного на стадии (3), образуются липосомы, содержащие включенный в них реагент. При получении таким способом липосом увеличение их размера относительно липосом, образуемых на стадии (1), происходит в значительно меньшей степени, чем в случае липосомных препаратов, которые не содержат сахара. И в этом случае указанные выше процессы экструзии, обработки в псевдоожиженном слое или гомогенизации могут быть исключены.
Установлено, что в ходе сушки с использованием соответствующих концентраций сахаров, до определенной степени снижается уровень слияния и агрегации липосом при образовании аморфной стеклоподобной массы (Crowe et al., Arch. Biochem. Biophys., 242 (1985) 240−247), а также взаимодействие сахаров с основной группой фосфолипидов (Crowe et al., Cryobiology, 31 (1994) 355−366). В ранних исследованиях дегидратированные/регидратированные везикулы (ДРВ) получали без использования cахаров в качестве стабилизаторов, при этом процедура основывалась на индукции слияния/агрегации образующихся мелких однослойных везикул при контролируемой регидратации (Kirby, Gregoriadis, 1984). В этой связи, можно было предположить, что общая стабилизация мелких однослойных везикул за счет добавления соответствующих количеств cахаров будет сопровождаться при восстановлении исходных MOB (SUV) очень низкой величиной включения.
Однако оказалось, что это не так. Хотя, как и в случае всех липосом, степень включения реагента зависит в некоторой мере от характеризующего систему коэффициента отношения липид: реагент, тем не менее ожидается, что уровень инкапсулирования реагента в липосомы, достигаемый при использовании способа по настоящему изобретению, будет вполне приемлемым.
Кроме того, применение липосом в качестве системы доставки лекарств налагает определенные требования к их физической и химической стабильности. Липосомы в виде водной дисперсии подвергаются гидролизу и физическим изменениям в процессе хранения, включая подтекание инкапсулированных лекарственных средств, а также изменение размеров в результате агрегации или слияния. Однако ожидается, что физическая и химическая стабильность липосом, получаемых по способу настоящего изобретения, будет хорошей.
Таким образом, настоящий способ дает возможность получать мелкие липосомы с высокой загрузкой, которые, как отмечалось выше, будут особенно полезны при создании фармацевтических композиций. Кроме того, заявленный способ может использоваться для приготовления инкапсулированных материалов разных типов.
Однако способ согласно настоящему изобретению будет особенно полезен при изготовлении липосом для применения в фармацевтической области. В этом случае используемые в рамках данного способа реагенты будут включать биологически активный материал, такой как фармацевтический ингредиент или лекарственное средство. Для этой цели получаемые на стадии (i) липосомы должны представлять собой мелкие однослойные везикулы со средним размером, например, в диапазоне от 25 нм до 90 нм, предпочтительно в диапазоне от 50 нм до 90 нм и наиболее предпочтительно от 70 нм до 90 нм. В конечном итоге, получаемые в рамках этого способа липосомы будут иметь все еще небольшой размер, в среднем менее 500 нм и обычно от 100 до 200 нм.
Имеющиеся на стадии (1) липосомы представляют собой пустые липосомы, получаемые посредством любого традиционного способа, например с помощью описанного выше классического способа. При этом любые образованные липосомы, в случае если их средний размер слишком велик для целевого использования, могут быть уменьшены с помощью известных в технике способов, например ультразвука, гомогенизации, экструзии или техники псевдоожиженного слоя.
Для получения липосом используют известные в технике липиды. Они включают, например, лецитины, такие как, например, фосфатидилхолин (ФХ), дипальмитоилфосфатидилхолин (ДПФХ), дистеароилфосфатидилхолин (ДСФХ), или заряженные липиды, в частности анионные липиды, такие как фосфатидиновая кислота, или катионные липиды, такие как стеариламин, необязательно в присутствии холестерина. Предпочтительным липидом является ДСФХ. Выбор липида зависит, в определенной мере, от природы активного средства и от цели использования липосом.
Приемлемые для использования на стадии (2) растворы сахаров включают водные растворы моносахаридов, таких как глюкоза и фруктоза, дисахаридов, таких как лактоза или сахароза, а также полисахаридов. Особенно предпочтительным для использования в способе настоящего изобретения сахаром является дисахарид, такой как сахароза или лактоза, или моносахарид, такой как глюкоза. В особенности, в качестве сахара предпочтительна сахароза.
В предпочтительном варианте на стадии (2) используют такое количество сахара, чтобы отношение массы сахара к массе липида составляло от 1:1 до 6:1 (вес/вес) и более предпочтительно — в диапазоне от 1:1 до 5:1 (вес/вес). Было обнаружено, что чем большее количество сахара используют, тем меньше увеличение размера липосом, получаемых после регидратации, в сравнении с имевшимися на стадии (1). Однако при этом уровень включения реагента может быть ниже. Таким образом, правильный выбор используемых в данном способе коэффициентов указанных соотношений будет зависеть от их целевого использования, при этом необходимо определять нужный баланс между степенью включения реагента при данном содержании липтида и размером липосомы. Разница между этими параметрами находит отражение в определенной вариабельности воздействия конкретного реагента на образование липосом, что будет пояснено ниже. В приемлемом варианте количество имеющегося сахара менее 10% (вес/объем) от всей композиции.
Кроме того, было показано, что увеличение объема используемого в рамках данного способа сахарного раствора при снижении его концентрации может способствовать повышению уровня включения. Приемлемые концентрации растворов сахаров находятся в диапазоне от 20 до 200 мМ, предпочтительно от 30 до 150 мМ.
Далее, было также обнаружено, что если последующую регидратацию проводить при повышенных температурах, например от 30 до 80oС, в частности от 40 до 65oС, и в особенности примерно при 60oС, то уровень включения может быть повышен. Показана эффективность такой процедуры в случае липосом, включающих ФХ и холестерин (ХОЛ), которые обычно образуются при комнатной температуре. Однако при использовании в рамках такого способа повышенных температур может наблюдаться некоторое увеличение размера липосом в сравнении с их исходными значениями, что нужно принимать во внимание при выборе условий, практикуемых для получения липосом в каждом конкретном случае.
К числу других факторов, которые, как было показано, также влияют на уровень включения, относятся индивидуальная природа реагента, такого как инкапсулируемое лекарственное средство, и, в частности, растворимость и количество такого реагента. При этом в некоторых случаях растворимость реагента может лимитировать то его количество, которое может быть растворено на стадии (2) и далее включено в липосому. К числу других факторов, влияющих на количество включаемых реагентов, относятся взаимодействия реагента с липидами липосомы, а также проницаемость липосомы для реагента.
В случае наличия в растворе, используемом на стадии (2) реакции, высоких концентраций реагента процент его включения может быть снижен. В этой связи, по экономическим причинам может быть выгодно снижать количество применяемого реагента.
Условия, выбираемые для целей получения липосом желательных размеров и нагрузки, включают коэффициент отношения массы сахара к массе липида, природу липида, концентрацию используемого раствора сахара, количество включенного в раствор реагента и температуру регидратации, которые могут быть определены для каждого конкретного реагента с помощью обычных процедур.
Указанная выше стадия (3) может проводиться с использованием традиционных способов, например с помощью лиофильной сушки, распылительной сушки, флэш-кристаллизации, высушивания в воздушном потоке (например, в псевдоожиженном слое), вакуумной сушки, сушки в печи или посредством любого другого известного в технике способа. И хотя механические свойства продуктов, получаемых описанными способами, могут различаться, при том что продукт распылительной сушки будет представлять собой дискретный и зачастую текучий порошок, тогда как лиофильная сушка дает твердую лепешку, свойства липосом при регидратации с точки зрения их стабильности и способности к нагрузке реагентом будут в целом сходными.
Распылительная сушка может оказаться предпочтительной для ряда приложений, включая приготовление фармацевтических композиций, поскольку она позволяет получать продукт с приемлемыми для дальнейшей обработки механическими свойствами.
Продукт, получаемый при лиофильной сушке, включает блочную пористую массу, обладающую относительно слабыми механическими характеристиками. С помощью размалывания этой массы ей могут быть приданы лучшие механические свойства, однако имеется риск возникновения повреждений на такой дополнительной стадии.
Распылительная сушка может дать продукт с хорошими механическими характеристиками, который может быть доставлен ингаляцией или введен парентерально после разбавления водой.
Последующая стадия регидратации может быть осуществлена в ходе процесса производства или альтернативно композиция может поставляться в сухом виде и дальше подвергаться регидратации уже в сайте предполагаемого введения, например, в больнице или в фармацевтическом отделении, когда инкапсулированное лекарственное средство должно быть доставлено пациентам.
Образуемые липосомы отличаются хорошей стабильностью, что определяет длительный срок годности продукта. Это свойство важно, например, для косметических продуктов, гигиенических принадлежностей и фармацевтических средств.
Как отмечалось выше, указанный способ особенно хорошо подходит для получения относительно мелких липосом с высокой степенью нагрузки реагентом. Это особенно желательно для применения в фармацевтической области, в частности для доставки материалов, таких как полимерные или белковые лекарственные средства, ДНК-содержащие вакцины, векторы для генной терапии или химические лекарственные средства. Приемлемые химические средства включают антибиотики, такие как окситетрациклины, b-лактамные антибиотики, такие как пенициллины, в частности пенициллин G, ампициллин или амоксициллин, или цефалоспорины, а также противораковые средства, гормоны, иммунотерапевтические препараты, противовирусные средства, противовоспалительные соединения и др.
На основе получаемых с помощью вышеописанного способа липосомных продуктов могут быть приготовлены фармацевтические композиции, например, при объединении их с фармацевтически приемлемыми носителями или наполнителями. Такие композиции могут быть пригодны для целей перорального, парентерального, и, в частности, внутривенного, или местного введения, например, на поверхность кожи или слизистой. Особенно полезной в рамках настоящего изобретения является композиция, пригодная для введения с помощью аэрозольного распылителя или ингалятора. Было обнаружено, что для этой цели приемлемы нейтральные липосомы липидной природы с высоким фазовым переходом, такие как липосомы, образуемые из смесей ДСФХ и холестерина. При осуществлении процесса в соответствии со способом настоящего изобретения, проведение экструзии перед сушкой может стать необязательной процедурой.
Ниже изобретение пояснено с помощью прилагаемых чертежей, при этом:
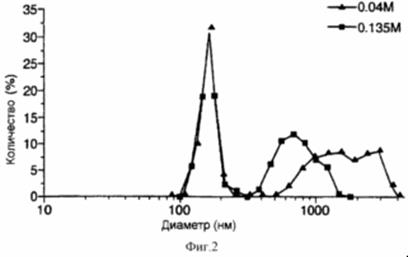
Рис 8. представляет собой график, демонстрирующий изменение размера дипальмитоилфосфатидилхолиновых (ДПФХ) и холестериновых (ХОЛ) липосом при их обработке ультразвуком и при лиофильной сушке с 0,0357 М сахарозы и затем регидратации;
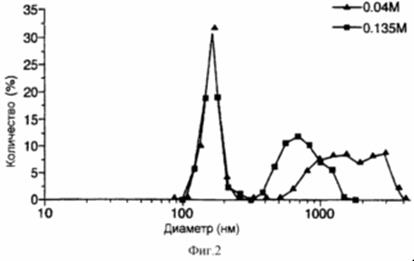
Рис. 9 представляет собой график, иллюстрирующий влияние молярности раствора сахарозы на распределение размеров ФХ: ХОЛ липосом, включающих FITC-альбумин (% распределения: интенсивность), получаемых после лиофильной сушки и регидратации
Рис. 10 представляет собой график, демонстрирующий влияние молярности раствора сахарозы на распределение размеров, получаемых после регидратации ФХ: ХОЛ липосом, включающих эпидермальный ростовой фактор (EGF)
Рис. 11 представляет собой график, иллюстрирующий в сравнительном аспекте данные по распределению размеров экструдированных и регидратированных ФХ: ХОЛ липосом, содержащих FITC-альбумин
Рис. 12 представляет собой график, иллюстрирующий распределение размеров экструдированных и лиофильно высушенных липосом, полученных по способу настоящего изобретения, которые содержат в инкапсулированном виде карбоксифлуоресцеин (КФ);
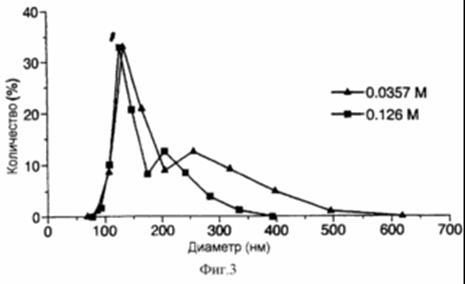
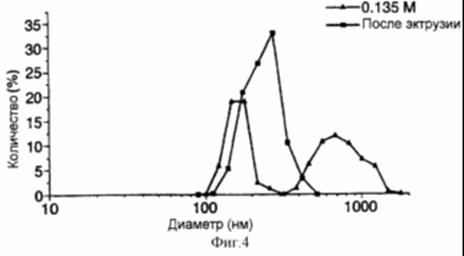
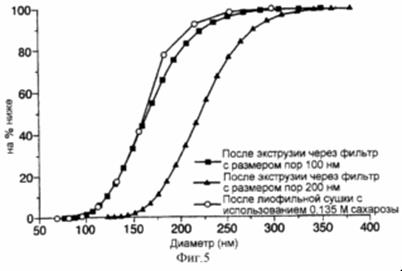
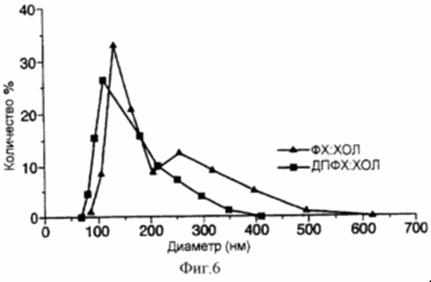
Рис. 13 представляет собой график, иллюстрирующий распределение размеров различных липосомных композиций
В приведенных ниже примерах фосфатидилхолин яйца (ФХ), дипальмитоилфосфатидилхолин (ДПФХ) и дистеарилфосфатидилхолин (ДСФХ) получают от Липоид ГмбХ (Lipoid GmbH, Ludwigshafen, Germany), холестерин, карбоксифлуоресцеин (КФ), альбумин, меченный флуоресцеинизотиоцианатом (FITC-альбумин), рибофлавин, даунорубицин, доксорубицин, Тритон Х-100, сахарозу, глюкозу и додецилсульфат натрия (ДСН, SDS) получают от компании Сигма (Sigma, Лондон). Эпидермальный фактор роста (ЭФР, EGF) был любезно предоставлен Центром Биологических Исследований, Гавана, Куба (Centre of Biological Sciences). Na125I, С14-меченый гидроксипропил-b-циклодекстрин и С14-меченый пенициллин были приобретены у компании Амершам Интернешнл, Великобритания (Amersham International, Amersham, UK). Мечение ЭФР с помощью 125I выполняют по хлораминатному методу. Все другие реагенты имеют аналитическую степень чистоты.