Разложение нитроэфиров, нитроаминов и других нитросоединений

Развитие термического распада циклотриметилентринитроамина на начальных стадиях выглядит следующим образом. Реакция возникает на дефектных местах кристалла — либо исходных, либо вызванных температурными напряжениями. Вследствие несоответствия объемов молекул продуктов реакции и исходного вещества происходит деформация кристаллической решетки, приводящая к возникновению в кристалле дополнительных… Читать ещё >
Разложение нитроэфиров, нитроаминов и других нитросоединений (реферат, курсовая, диплом, контрольная)
Многие исследователи считают, что первоначальной стадией реакции термического разложения нитроэфиров является разрыв связи RO-NO2, в результате чего образуются молекула диоксида азота и алкоксильный радикал. Последний превращается в продукты, содержащие альдегидные и гидроксильные группы, которые при взаимодействии с диоксидом азота приводят к образованию конечных продуктов разложения — оксида и диоксида углерода, оксидов азота и диазота, азота, водорода и воды (табл. 1.12).
Разложение метилнитрата при температурах 210−240°С происходит по следующей схеме:
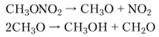
Экспериментальные данные о разложении этилнитрата хорошо объясняются уравнениями.
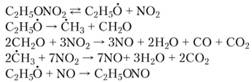
Таблица 1.12.
Состав продуктов, образующихся при медленном разложении нитроэфиров[1]
Нитроэфир | t,°С | Газы, % (об.). | Жидкие продукты. | ||||||
NO2. | NO. | N2O. | N2. | H2. | CO. | CO2. | |||
Этилнитрат. | 60,0. | 3,2. | 1,2. | 8,9. | 23,4. | CH3CHO, H2O. | |||
Нитроглицерин. | 22,0. | 30,0. | H2O. | ||||||
Нитроцеллюлоза. | 10,1. | 37,2. | 5,4. | 9.9. | 3,9. | 13,8. | 19,7. | CH2O, H2O. | |
Пентрит (ТЭН). | 11,8. | 47,7. | 9.5. | 1.6. | 2,0. | 21,1. | 6,3. | CH2O, H2O. | |
Причем этилнитрит образуется почти с количественным выходом. Образование свободных радикалов при разложении этилнитрата установил Ф. Райс в 1935 г. Медленное термическое разложение большого числа органических нитратов (нитроэфиров) происходит по реакциям первого порядка, если принимаются меры против автокатализа и саморазогревания.
Результаты исследования распада полинитратов гликоля и глицерина, а также алкилмононитратов позволили выявить закономерности в отношении распада полинитратов. Схему распада полинитратов применительно к простейшему динитрату можно представить совокупностью следующих реакций:
Скорость распада оксирадикала больше скорости распада этилнитрата, а соотношение констант образования нитритнитрата и оксиальдегида меняется в пользу последнего.
Схема термического разложения нитритов в большой мере сходна со схемой распада нитратов, особенно в начальной стадии, которая качественно тождественна (отрыв NOи NO2-групп). Различия обусловлены возможностью образования воды и кислоты как участника и катализатора гидролиза.
Медленное термическое разложение нитроаминов (табл. 1.13) напоминает разложение нитроэфиров[2]. Установлено, что многие реакции разложения нитроаминов имеют первый порядок. Разложения описанных соединений характеризуются большой энергией активации и высокими значениями предэкспоненциального множителя. Автокаталитическое действие и тепловой эффект в ряде случаев усложняют простую мономолекулярную схему разложения. Однако исследование продуктов разложения показало заметное отличие механизма разложения нитроаминов от механизма разложения нитроэфиров. В то время как начальная стадия разложения нитроэфиров сопровождается выделением NO2 с последующим восстановлением до NO, при разложении нитроаминов большая часть азота выделяется в виде N2O. Разрыв связи RN-NO2 с выделением NO2 не является основным процессом при разложении нитроаминов. Поскольку конечная стадия процесса горения сопровождается восстановлением оксидов азота, образующихся на начальных стадиях реакции, оксидом углерода и водородом, можно ожидать, что сгорание нитроаминов и нитроэфиров происходит неодинаково, так как при реакции в газовой фазе в одном случае преобладает N2O, а в другом — NO.
Сравнение данных табл. 1.12 и 1.13 показывает, что нитроамины более стойки при низких температурах, чем нитроэфиры.
Таблица 1.13
Состав продуктов медленного разложения нитроаминов
Нитроамин. | t,. °с. | Газы, % (об.). | Жидкие продукты. | |||||
NO. | N2O. | N2. | H2. | СО. | СO2. | |||
Этилендинитроамин. | 0,10. | 1,40. | 0.39. | 0,028. | 0,065. | СН3СНО, НО. | ||
Циклотриметилен тринитроамин. (гексоген). | 0,54. | 0,98. | 1,16. | 0,09. | 0.40. | 0,48. | СН2О, Н2О. | |
5%-ный раствор гексогена в тринитротолуоле. | 0,70. | 0,63. | 1.65. | 0.57. | 0,83. | CH2Q Н2О. | ||
Циклотетраметилен тетранитроамин. (октоген). | 0,95. | 1,51. | 1,16. | 0,20. | 0,57. | 0,64. | СН2O, H2? | |
Исследования термического разложения твердого нитроамина — циклотриметилентринитроамина — проводили с монокристаллами, выращенными из ацетона методом медленного охлаждения. Эксперименты показали, что это соединение при температурах ниже 165 °C, по крайней мере на начальных стадиях, разлагается без образования жидкой фазы и в процессе термического распада практически полностью переходит в газообразное состояние.
Развитие термического распада циклотриметилентринитроамина на начальных стадиях выглядит следующим образом. Реакция возникает на дефектных местах кристалла — либо исходных, либо вызванных температурными напряжениями. Вследствие несоответствия объемов молекул продуктов реакции и исходного вещества происходит деформация кристаллической решетки, приводящая к возникновению в кристалле дополнительных напряжений. Это, в свою очередь, способствует термической реакции в объеме, так как увеличивается дефектность кристалла. При развитии процесса продукты реакции не успевают диффундировать, их накопление приводит к образованию дефектных зон и столь большому росту напряжений, что кристалл растрескивается и начинается видимое газовыделение.
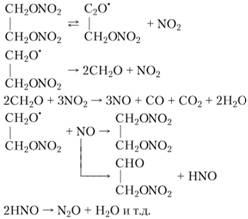
Разложение нитрометана рассмотрено в работе [1]. При низких давлениях 27−53 кПа в интервале температур 280- 300 °C продукты разложения нитрометана содержат оксиды азота и диазота, воду, оксид углерода, метан, диоксид углерода, малые количества этилена и этана и следы диоксида азота. Главным азотсодержащим соединением является NO; его содержание по ходу распада уменьшается. Отношение [СО]: [СН4]: [СO2] = 10: 6,2: 1,4 после разложения нитрометана на 5% остается постоянным. Для начальных стадий при низких давлениях принимается следующая схема реакций [38]:
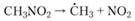
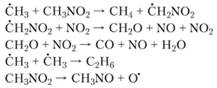
При повышенных давлениях и температуре 355 °C основными продуктами разложения нитрометана являются диоксид и оксид углерода, метан, синильная кислота, оксид азота, азот, вода и в меньших количествах метилцианид, этилцианид, формальдегид и оксид диазота. При 5% разложения отношение [СО]: [СН4]: [СO2] равно 10:5: 10.
Большое количество HCN, обнаруженное в продуктах разложения нитрометана при повышенных давлениях, может быть объяснено реакцией распада нитрозометана.
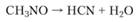
Разложение нитроэтана и нитропропанов изучено меньше, чем разложение нитрометана. Установлено образование свободных радикалов при распаде нитроэтана, а также значительное ускорение его разложения при введении метальных радикалов. При 477 °C распад может быть описан уравнением.
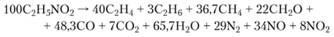
Это говорит о том, что первичным этапом является распад нитропарафина на радикал и NO2, с помощью которого можно объяснить последующее образование всех остальных экспериментально обнаруженных продуктов — С2Н4, NO, СО, СН2O и СН4.
Продукты первичного распада взаимодействуют также с самим нитроэтаном, вследствие чего наблюдаемая скорость распада оказывается больше, чем скорость разрыва связи C-N. Энергия активации составляет 142 кДж/моль, что значительно меньше энергии разрыва указанной связи.
Данные о кинетике термического разложения нитросоединений приведены в табл. 1.14.
Таблица 1.14
Кинетические характеристики термического разложения нитроэфиров, нитроаминов и других нитросоединений
Соединение. | t, °С | Eакт, кДж/моль. |
Метилнитрат. | 210−240. | 165,4. |
Этилнитрат. | 180−215. | |
161−181. | 172,5. | |
75−105. | 168,7. | |
Нитроглицерин. | 90−125. | 178,4. |
125−150. | 188,4. | |
150−190. | 209,3. | |
90−135. | 205,2. | |
Нитроцеллюлоза (13% N). |
|
|
130−155. | 195,5. | |
н-Пропилнитрат. | н/д. | 162,9. |
100−120. | 156,2. | |
Этилендинитроамин. | 120−135. | 173,8. |
135−145. | 215,6. | |
184−254. | 127,7. | |
Нитрометан. | 380−430. | 224,4. |
414−442. | 173,3. | |
Нитроэтан. | >442. | 195,9. |
355−405. | 191,8. | |
1-Нитропропан. | 414−442. |
|
2-Нитропропан. | 415−460. |
|
Тринитротолуол. |
|
|
Пикриновая кислота. | н/д. | 245,3. |
2,4,6-Тринитрофенил метилнитроамин (тетрил). | 211−260. | 160,8. |
140−150. | 232,4. | |
Гексоген. | н/д. | 198,9. |
В некоторых случаях наблюдаются значительные колебания в значениях кинетических параметров. Например, для тетрила предэкспоненциальный множитель A изменяется примерно на девять порядков, а энергия активации — на 71 кДж.
Следует иметь в виду, что экспериментальные значения зависят от условий проведения опыта, чистоты образца, его физического состояния, а также точности метода. На значения кинетических характеристик могут оказать влияние также саморазогрев системы, каталитическое действие примесей и промежуточных и конечных продуктов разложения.
Известно, что температурная зависимость константы скорости описывается уравнением Аррениуса.
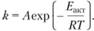 (1.75).
(1.75).
Значение предэкспоненциального множителя A согласно теории должно быть порядка частоты валентных колебаний связей в молекуле, т. е. 1013−1014 с-1. Однако экспериментальные исследования термического разложения многих взрывчатых веществ (ВВ) показали, что для одного и того же вещества наблюдаются иногда не одно, а несколько значений Eакт и, соответственно, несколько значений Л, на много порядков превосходящих теоретические. В виде исключения наблюдались и близкие к теоретическим значения A. Согласно А. И. Сербинову такой разброс в значениях предэкспоненциального множителя объясняется неточностью далекой экстраполяции, так как Л равно значению k при Т > ¥.
Энергия Еакт разложения кристаллического тетрила равна 159 кДж/моль (при lgA = 13,6), т. е. больше, чем для жидкого или растворенного, примерно па половину теплоты плавления. Данные по тепловому взрыву и, но изотермическому разложению тротила имеют значительный разброс; энергию активации его разложения, согласно Сербинову, можно оценить в 192,6 ± 8,4 кДж/моль.
Имеющиеся в литературе эмпирические зависимости (1.75) описывают кинетику разложения для исследованного диапазона температур и принятых условий эксперимента. Однако полученные данные, особенно при экстраполяции результатов на другой диапазон температур, следует проверять по методу Сербинова (вычисление теоретического значения А и использование его при обработке экспериментальных данных).