Изменение энергии Гиббса в химических реакциях

Во втором способе расчета? G химических реакций используют то, что эту величину можно рассчитать по известным величинам? G других реакций, комбинация уравнений которых дает интересующее нас уравнение реакции (аналогично расчету тепловых эффектов реакции). При этом мы исходим из свойств этой функции как функции состояния: считаем? G независимым от пути проведения процесса. Если термодинамика дает… Читать ещё >
Изменение энергии Гиббса в химических реакциях (реферат, курсовая, диплом, контрольная)
Расчет ?G для химических процессов можно осуществить двумя способами. В первом способе используется соотношение (4.3).
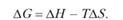
Рассмотрим в качестве примера расчет ?G0 для реакции.
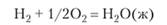
Символ «°», как и прежде, указывает на стандартное состояние всех участников реакции.
Известно, что стандартная энтальпия образования воды равна.
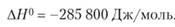
Используя табличные значения стандартных энтропий участников реакции, выраженных в энтропийных единицах, э.е. (Дж/моль • К): =126 э.е.;
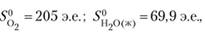 вычислим AS0, используя уравнение (3.6):
вычислим AS0, используя уравнение (3.6):
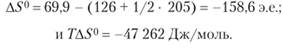
Таким образом, найдем, что.
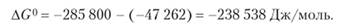
Полученная отрицательная величина говорит о том, что в стандартных условиях эта реакция должна идти слева направо.
Во втором способе расчета ?G химических реакций используют то, что эту величину можно рассчитать по известным величинам ?G других реакций, комбинация уравнений которых дает интересующее нас уравнение реакции (аналогично расчету тепловых эффектов реакции). При этом мы исходим из свойств этой функции как функции состояния: считаем ?G независимым от пути проведения процесса.
Наиболее удобно использовать для этих целей AG реакций образования (?Go6p). С реакциями образования мы знакомились, когда изучали первое следствие из закона Гесса. Напоминаем, что реакциями образования в термодинамике считаются такие реакции, в которых 1 моль вещества в стандартном состоянии при данной температуре образуются из простых веществ, взятых в их стандартном состоянии при той же температуре. Реакции образования часто бывают гипотетическими, т. е. не идущими реально, а лишь соответствующими приведенному выше определению. В термодинамических таблицах приводятся изменения энергии Гиббса для реакций образования при стандартных условиях (?G^) — Понятно, что ?G°6p простых веществ равно нулю.
Используя ?Gр, можно рассчитать стандартное изменение энергии Гиббса (?G0) любой химической реакции. Эта величина равна разности стандартных энергий Гиббса для реакций образования продуктов реакции и исходных веществ с учетом стехиометрических коэффициентов:
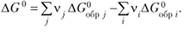
(4.4)
В качестве примера рассчитаем (? G°) важного биохимического процесса — реакции окисления глюкозы:
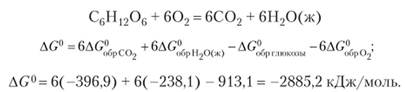
В биологических системах такое большое количество энергии освобождается нe сразу, а небольшими порциями в сложном ряду химических превращений.
Для расчета изменения энергий Гиббса реакций при температурах, отличающихся от стандартных (?GT), надо знать величины теплоемкостей участников реакции в интервале температур от 298 К до Т. Расчетные соотношения получают следующим образом:
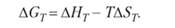 (4.5).
(4.5).
Так как в соответствии с уравнениями (2.18а) и (3.7).

и.
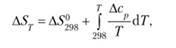
то.
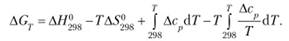 (4.5а) Аналогичным образом можно получить выражение зависимости ?F от температуры:
(4.5а) Аналогичным образом можно получить выражение зависимости ?F от температуры:
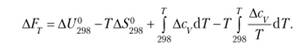 (4.6).
(4.6).
Для практического использования функций ?F и ?G полезно знать ответы на следующие вопросы.
1. Каковы различия между ?F и ?G химических реакций при Т = const?
Из определений ?F и ?G следует, что.
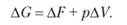
В реакциях в конденсированных средах (твердых и жидких) обычно изменением объема можно пренебречь (?V = 0). Тогда.
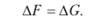
Если в реакциях участвуют газы и можно их считать идеальными, то 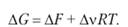
При ?V = 0, т. е. когда реакция идет без изменения числа молей,.
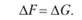
2. Какие выводы можно сделать, получив значения термодинамических критериев возможности самопроизвольного протекания процессов?
Если термодинамика дает отрицательный ответ на вопрос о возможности самопроизвольного протекания процесса (?F > 0 или ?G > 0), это означает, что без внешнего подвода энергии процесс невозможен. Процесс может самопроизвольно протекать только в обратном направлении.
Если термодинамика дает положительный ответ (?F< 0 или ?G < 0), это говорит только о возможности протекания процесса. Но часто в реальных условиях такой процесс не идет. Например, для реакции образования С02 ?G0 = -395,9 кДж/моль. Но графит с кислородом при 298 К и р = 1 атм не реагирует. Чтобы процесс шел, необходимо создать условия для увеличения скорости (запал, катализаторы и т. д.).
3. Может ли идти процесс, если ?F > 0 или ?G > 0?
Может, но не самопроизвольно. Для его проведения надо затратить энергию. Пример — процесс фотосинтеза, идущий в растениях под воздействием солнечной энергии. Другой пример — протекание реакций, характеризующихся ?G > 0, при сопряжении их с реакциями, для которых AG < 0. При этом сумма величин ?G для всех стадий процесса, включая сопряженные реакции, отрицательна. Например, для синтеза сахарозы из глюкозы и фруктозы:
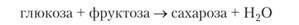
?G0 = 21 кДж/моль и, следовательно, прямая реакция самопроизвольно протекать не может. Вместе с тем, известно, что в организмах этот процесс происходит. Сопряженной реакцией в этом случае является гидролиз адепозинтрифосфата (АТФ) с образованием АДФ и фосфорной кислоты (Ф):
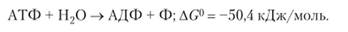
Сопряжение осуществляется путем образования в качестве промежуточного соединения глюкозо-1-фосфата. Реакция идет в две стадии:
1- я стадия: АТФ + глюкоза -> глюкозо-1-фосфат + АДФ;
?G0 = -29,4 кДж/моль.
2- я стадия: глюкозо-1 -фосфат + фруктоза —> сахароза + Ф; AG0 = 0.
Так как? G является величиной аддитивной, суммарный процесс можно записать в виде суммы двух стадий:
АТФ + глюкоза + фруктоза = сахароза + АДФ + Ф; ?G0 =.
= -29,4 кДж/моль.
Такое сопряжение типично для многих биологических реакций.
В живых организмах освобожденная при окислении глюкозы энергия не сразу расходуется в различных процессах жизнедеятельности, а запасаeтся впрок в различных соединениях, богатых энергией, таких, как эфиры фосфорной кислоты (АТФ, ЛДФ, креатини аргининфосфаты и др.).
4. В каких случаях АН (или ?U) является критерием самопроизвольности процесса?
В общем случае критерием самопроизвольности является величина ?G (или ?F) процесса.
Так как ?G = ?Н — T? S (или ?F = ?U — T? S), то при ?S = 0 (в изоэнтронийных условиях) ?G = ?Н (или ?F= ?U). В этом случае ?Н (или ?U) является критерием самопроизвольности процесса. При этом самопроизвольно идут экзотермические реакции (?Н < 0, ?U < 0).
5. В каких случаях ?S является критерием самопроизвольности процесса?
Рассуждения аналогичны приведенным в п. 4.
Так как ?G = ?Н — T? S (или ?F = ?U — T? S), то при отсутствии тепловых эффектов реакций (АН = 0, ?U = 0) ?G = -T?S(или ?F= -T?S). В этом случае ?S является критерием самопроизвольности процесса. При этом самопроизвольно идут процессы с ростом энтропии (?S > 0), т. е. процессы, связанные с разложением веществ, их деструкцией, дезагрегацией.
6. Каковы условия самопроизвольного протекания экзотермических реакций (?Н < 0, ?U < 0)?
Выберем для определенности изобарные условия протекания экзотермических реакций: ?Н < 0. При этом возможность самопроизвольного протекания реакции определяется знаком ?G = АН — T?S.
Рассмотрим, как меняется знак ?G при варьировании величины ?S:
- а) если ?S > 0, то ?G = ?Н — T?S < 0. Процесс идет самопроизвольно;
- б) если ?S = 0, то ?G = ?Н — T? S < 0. Процесс идет самопроизвольно;
- в) если ?S < 0, то ?G = ??Н — T? S может иметь различные знаки в зависимости от абсолютной величины T?S:
- • |?H|>|T?S|. При этом ?G < 0. Процесс идет самопроизвольно,
- • | ?H | = |T?S|. При этом? G = 0. Состояние равновесия,
- • | ?H |<|T?S|. При этом ?G > 0. Процесс не идет слева направо.
Таким образом, экзотермические реакции термодинамически запрещены только при значительном уменьшении энтропии, например, в некоторых процессах структурирования, образования дополнительных связей и т. д.
Еще один важный вывод из этих рассуждений: в изолированных системах самопроизвольно могут идти процессы с уменьшением энтропии, если они сопровождаются значительным тепловым эффектом. Это особенно важно для понимания возможности самопроизвольного усложнения систем, например, в процессе роста живых организмов. В этом случае источником энергии могут являться все те же богатые энергией эфиры фосфорной кислоты (АТФ, АДФ, креатини аргининфосфаты и др.). Кроме того, при рассмотрении реальных систем следует иметь в виду, что они практически не бывают изолированными и имеется возможность подачи энергии извне.
7. Каковы условия самопроизвольного протекания эндотермических реакций (?Н > 0)?
Выберем для определенности изобарные условия протекания эндотермических реакций: ?H> 0. При этом возможность самопроизвольного протекания реакции определяется знаком ?G = ?Н — T? S.
Как и в предыдущем случае, рассмотрим, как меняется знак ?G при варьировании величины ?S:
- а) если ?S > 0, то ?С = ?Н — T? S может иметь различные знаки в зависимости от абсолютной величины T?S:
- • ?Н < T? S. При этом ?С < 0. Процесс идет самопроизвольно,
- • ?Н = T? S. При этом ?G = 0. Состояние равновесия,
- • ?Н > T? S. При этом ?С > 0. Процесс не идет самопроизвольно слева направо;
- б) если ?S = 0, то АС = ?Н — T? S > 0. Процесс не идет самопроизвольно слева направо;
- в) если ?S < 0, то ?С = ?Н — T? S > 0. Процесс не идет самопроизвольно слева направо.
Таким образом, эндотермические реакции идут самопроизвольно только при значительном увеличении энтропии в реакции, например, в процессах разложения, деструкции, дезагрегации.
- 8. Как влияет повышение температуры на ?U, ?Н, ?S, ?G и aлхимических реакций:
- а) зависимость ?U от температуры выражается уравнением Кирхгоффа (2.21а):
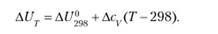
С ростом температуры величина ?Uрастет при ?cv> 0 и падает при ?cv< 0. При ?Су= 0 величина ?U не зависит от температуры;
б) зависимость ?Н от температуры выражается уравнением Кирхгоффа (2.20а):
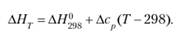
С ростом температуры величина ?Н растет при? ср> 0 и надает при ?ср < 0. При ?ср = 0 величина ?Н не зависит от температуры;
в) зависимость ?S от температуры выражается уравнением (3.8а):
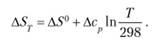
С ростом температуры ?S растет при ?ср> 0 и падает при? с/;< 0. При ?ср=0 величина? S не зависит от температуры;
г) зависимость? F от температуры выражается уравнением (4.6).
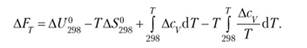
Часто можно пренебречь двумя последними слагаемыми из-за их незначительной величины по сравнению с первыми двумя слагаемыми:
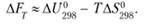
Приближенно можно заключить, что с ростом температуры? F растет при ?S < 0 и надает при ?S > 0. При ?S = 0 величина ?F нe зависит от температуры;
д) зависимость ?G от температуры выражается уравнением (4.5а):
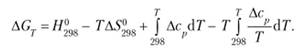
Часто можно пренебречь двумя последними слагаемыми из-за их меньшей величины по сравнению с первыми двумя слагаемыми:
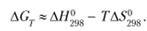
Приближенно можно заключить, что с ростом температуры ?G растет при ?S < 0 и падает при ?S > 0. При ?S = 0 величина ?G не зависит от температуры.