Химическая коррозия.
Физическая и коллоидная химия

Образующиеся на металле оксидные пленки часто препятствуют дальнейшему окислению (образуется так называемая «защитная» пленка, которая препятствует проникновению к металлу как газов, так и жидкостей). Защитными свойствами обладает только та пленка, которая может покрывать сплошь весь металл. Расчеты показывают, что это возможно, если объем оксида металла больше объема самого металла, пошедшего… Читать ещё >
Химическая коррозия. Физическая и коллоидная химия (реферат, курсовая, диплом, контрольная)
Химическая коррозия обусловлена взаимодействием металла с сухими газами или жидкостями, не проводящими электрического тока. Химической коррозии подвергаются детали и узлы машин, работающих в атмосфере кислорода, галогенов, при высоких температурах (турбинные, ракетные двигатели, оборудование химических производств).
Механизм реакции сравнительно прост. Продукты реакции образуются на тех участках металлической поверхности, которые вступили в реакцию. Так, на железе при 250—300°С появляется видимая пленка оксидов, при 600 °C и выше поверхность металла покрывается слоем окалины, состоящей из оксидов железа различной степени окисления (FeO, Fe304, Fe203). Окалина не может защитить металл от дальнейшего окисления, так как содержит трещины и поры, которые позволяют проникать кислороду к металлу. При повышении температуры свыше 800 °C скорость окисления железа резко увеличивается.
Образующиеся на металле оксидные пленки часто препятствуют дальнейшему окислению (образуется так называемая «защитная» пленка, которая препятствует проникновению к металлу как газов, так и жидкостей). Защитными свойствами обладает только та пленка, которая может покрывать сплошь весь металл. Расчеты показывают, что это возможно, если объем оксида металла больше объема самого металла, пошедшего на образование этого оксида.
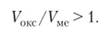
Для щелочных и щелочно-земельных металлов это условие не соблюдается (Vovx/Vm. < 1) — Такие пленки защитными свойствами не обладают и эти металлы ввиду своей химической активности принадлежат к числу коррозионно нестойких. На алюминии и хроме образуются хорошие защитные пленки, благодаря чему металлы в атмосферных условиях коррозийностойки (хотя химически активны). Толщина таких пленок крайне мала, например, на алюминии она достигает только 100 А. Такие пленки состоят всего из нескольких слоев молекул и могут быть обнаружены только специальными оптическими методами.
Если металл, покрытый пленкой, продолжает корродировать, то это означает, что имеет место диффузия атомов кислорода сквозь пленку к металлу, а атомов металла — в обратном направлении. Диффузия металла и кислорода в слое твердого защитного оксида может происходить по одному из двух возможных механизмов:
- а) движение ионов в междоузельном пространстве кристаллической решетки;
- б) движение ионов по пустым узлам решетки.
Первый механизм имеет место при образовании пленок ZnO, CdO, BeO, А1203; второй — Cu20, FeO, NiO, CoO, Zr02, Ti02.
Диффузия катионов в защитной пленке сопровождается одновременным перемещением в том же направлении эквивалентного числа электронов в междоузлиях при первом механизме и по «электронным дефектам» (катионом с более высокой валентностью) при втором механизме. При повышении температуры окисление металлов на воздухе происходит более интенсивно (увеличивается скорость диффузии).
Злектрохимическая коррозия. Подземная коррозия
Разрушение металла при соприкосновении с электролитом с возникновением в системе электрического тока называется электрохимической коррозией.
В атмосферных условиях роль электролита играет водная пленка на металлической поверхности, в которых часто растворены электропроводящие примеси. Электродами обычно являются сам металл и примеси в нем содержащиеся. В качестве примера рассмотрим действие серной кислоты на железо, содержащего примесь меди. При таком контакте возникает множество микроскопических гальванических элементов.
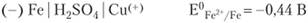

Более активный металл-железо — окисляется, посылая электроны атомам меди и переходит в раствор в виде ионов Fe2+, а ионы водорода разряжаются (восстанавливаются) на меди.
Помимо этого железо может растворяться и при непосредственном взаимодействии с кислотой (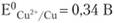 ), но опыт показывает, что скорость этой реакции мала по сравнению со скоростью растворения железа как анода гальванопары. Механизм коррозии в кислой и нейтральной среде различен.
), но опыт показывает, что скорость этой реакции мала по сравнению со скоростью растворения железа как анода гальванопары. Механизм коррозии в кислой и нейтральной среде различен.
Рассмотрим коррозию технического железа на воздухе, когда оно покрыто влажной пленкой или находится в растворе электролитов с небольшой концентрацией гидроксид ионов. В качестве анода здесь служит основной металл — железо, катодом являются примеси, содержащиеся в металле, например, зерна графита:
Анод: 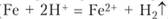
Катод: 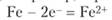
Ионы ОН- соединяются с перешедшими в раствор ионами Fe2+
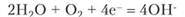
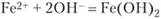
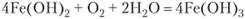
Согласно теории электрохимической коррозии при соприкосновении металла с электролитом на его поверхности возникает множество микрогальванических элементов. При этом анодами являются частицы металлов, катодами — загрязнения, примеси и участки металла, имеющие более положительный потенциал. Механическая обработка изменяет электродный потенциал, поэтому соприкосновение двух участков металла деформированного и недеформированного достаточно для появления разности потенциалов. Корродировать будет деформированный участок. Разность потенциалов возникает и там где соприкасаются обнаженный и покрытый пленкой участки.
Поскольку ионы и молекулы, связывающие электроны в катодном процессе, называют деполяризаторами, то часто говорят о водородной деполяризации в кислой и кислородной деполяризации в нейтральной и слабощелочной средах.
Так как электрохимическая коррозия обусловлена деятельностью гальванических элементов, можно сделать вывод, что факторы способствующие деятельности гальванических элементов усиливают коррозию. Скорость коррозии тем больше, чем дальше в ряду напряжений отстоят металлы, из которых образовалась гальваническая пара. Скорость коррозии возрастает с ростом температуры и с увеличением концентрации окислителя в растворе.
Нередко продукты коррозии оказываются малорастворимыми в данной среде и своим присутствием защищают металл от дальнейшего разрушения. Например, железо в щелочных растворах, свинец в разбавленной серной кислоте коррозионно стойки вследствие образования пленок Fe (OH)2, PbS04.
Большое значение в процессах коррозии имеют поляризация электродов, образование пленок на металлах, перенапряжение водорода. Если бы в коррозионных процессах не происходило поляризации электродов (см. поляризация), то процессы коррозии протекали бы с такой скоростью, что железо и ряд других металлов потеряли бы свое значение в технике.
Под влиянием веществ, растворимых в почве или под действием блуждающих токов, происходит разрушение газои нефтепроводов, оболочек кабелей, металлических конструкций, свай (почвенная коррозия). Интенсивность почвенной коррозии зависит от агрессивно действующих кислот, органических соединений и от деятельности бактерий. Наиболее активными считаются торфянистые и болотистые почвы. Под действием блуждающих токов, исходящих от электроустановок, работающих на постоянном токе, трамваев, метро, электрических железных дорог. Блуждающие токи вызывают появление на металлических предметах (трубопроводах, кабелях, рельсах участков входа и выхода постоянного тока, т. е. образование катодных и анодных зон на металле) анодные зоны — места выхода тока подвергаются коррозии. Блуждающие токи от источников переменного тока вызывают слабую коррозию изделий из стали и сильную — у изделий из цветных металлов. Резко увеличивают коррозию ионы хлора, брома, йода.