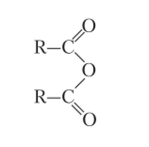
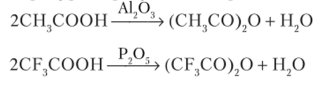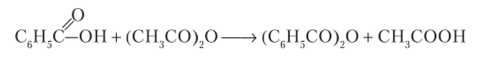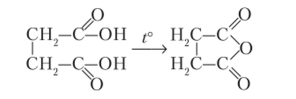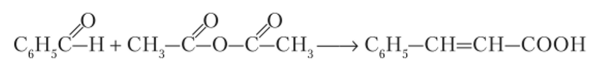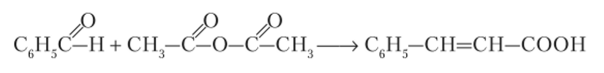Ангидриды можно рассматривать как продукты дегидратации карбоновых кислот:
Получение ангидридов
Взаимодействие галогенангидридов с солями кислот
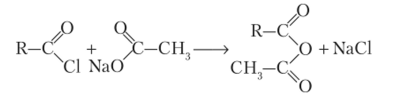
Взаимодействие галогенангидридов с солями кислот является общим способом получения ангидридов карбоновых кислот:
Действие водоотнимающих средств
Некоторые кислоты при действии сильных водоотнимающих средств (Р205) или в присутствии катализаторов при высокой температуре образуют ангидриды:
Перегонка смеси ароматической кислоты с уксусным ангидридом в присутствии фосфорной кислоты
Этим способом получают ангидриды ароматических кислот:
Нагревание 1,4- и 1,5-дикарбоновых кислот
Нагревание 1,4- и 1,5-дикарбоновых кислот дает внутренние циклические ангидриды: 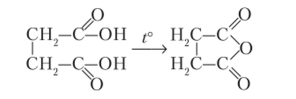
Физические свойства ангидридов
Ангидриды жирных кислот — жидкости с острым запахом, нерастворимы в воде. Ангидриды высших кислот — кристаллические вещества без запаха.
Химические свойства ангидридов
По химическим свойствам ангидриды напоминают хлорапгидриды. Они также являются ацилирующими средствами, но реакции с ними протекают более мягко, чем с хлорангидридами.
Ангидриды гидролизируются водой до кислот:
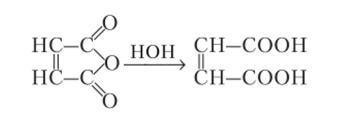
Со спиртами ангидриды образуют сложные эфиры: 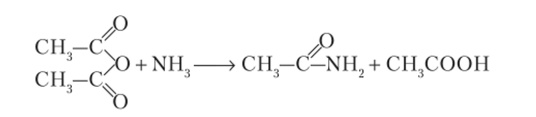 С аминами ангидриды образуют амиды:
С аминами ангидриды образуют амиды:
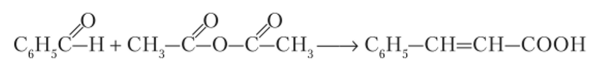
Реакция Перкина. Уксусный ангидрид может вступать в качестве метиленового компонента в реакции конденсации с карбонильными соединениями (реакция Перкина):
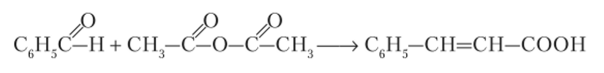
Малеиновый ангидрид-диенофил. Малеиновый ангидрид взаимодействует с сопряженными диенами в качестве диенофила в реакциях диенового синтеза:
Применение ангидридов
Ангидриды дикарбоновых кислот находят применение в реакциях поликонденсации для получения высокомолекулярных соединений, например, фталевый ангидрид служит для получения глифталевых алкидных смол.