История открытия законов термодинамики

Вернемся, однако, к Гельмгольцу. Мир, по его мнению, представляет собой совокупность материальных точек, взаимодействующих друг с другом так называемыми центральными силами. Во главу утла при этом Гельмгольц ставит принцип сохранения живой силы, требующий, чтобы количество работы при переходе из одного состояния в другое было тем же, что при обратном переходе, независимо от его способа, пути… Читать ещё >
История открытия законов термодинамики (реферат, курсовая, диплом, контрольная)
В результате изучения данной главы студент должен:
знать
- • исторические этапы развития термодинамики, историю открытия закона сохранения и превращения энергии;
- • физическую сущность законы термодинамики, уравнения Майера, механического эквивалента теплоты, энтропии;
уметь
- • оценивать значение работ Б. Румфорда и Г. Дэви в развитии теории теплоты, исторические опыты Дж. Джоуля, вклад Р. Майера, Дж. Джоуля, Г. Гельмгольца, Р. Клаузиуса, У. Томсона, В. Нернста в открытие законов термодинамики;
- • обсуждать вечные двигатели первого и второго рода, идею тепловой смерти Вселенной, парадокс — «демон Максвелла», биографии творцов термодинамики;
владеть
• навыками оперирования основными понятиями термодинамики.
Ключевые термины: закон сохранения и превращения энергии, второе начало (закон) термодинамики, энтропия, тепловая смерть Вселенной, третье начало (закон) термодинамики, «демон Максвелла».
О том, что при трении выделяется тепло, было известно еще нашим далеким предкам, жившим в каменном веке. Однако только исследования ученых XIX в. дали возможность количественно объяснить этот эффект. Первопроходцем был Бенджамин Томпсон, впоследствии лорд Румфорд (1753—1814). Он родился в США, которые тогда еще были английскими колониями. Во время борьбы колоний за независимость Б. Томпсон был агентом английской разведки. После разоблачения он уехал в метрополию, а затем в Мюнхен, где наладил производство пушек.
Румфорд обратил внимание на то, что при сверлении стволов артиллерийских орудий выделяется тепло. Для выяснения того, почему такой эффект имеет место, он выполнил ряд опытов, которые в сущности сводились к тому же сверлению цилиндров из пушечного металла и измерению прироста температуры, который при этом происходит. На основании этих опытов Румфорд пришел к выводу о том, что теплота — это особый вид движения.
Опыты Румфорда повторил Г. Дэви. Ученик аптекаря, затем химик в английском городе Бристоне, в конце жизни профессор химии Лондонского королевского института. Его опыты несколько отличались от экспериментов Румфорда. Дэви исследовал процессы, происходящие при трении двух кусков льда. Он пришел к тем же выводам, что и его предшественник: гипотеза теплорода не объясняет результатов опытов, а теплота должна быть какой-то формой движения. Был еще Фридрих Мор (1806—1879), профессор фармакологии, который высказал такие же мысли, но не смог их опубликовать в наиболее солидном в то время журнале «Annalen der Physik».
Одним из парадоксов истории явилось то, что идея сохранения энергии вызрела не у специалистов-физиков, а у людей, которые по характеру мышления отличались от них. В утверждении великого закона решающую роль сыграли врач Юлиус Роберт Майер (1814—1878), пивовар Джеймс Прескотт Джоуль (1818—1889), физиолог и врач Герман Людвиг Фердинанд Гельмгольц (1821—1894), за которыми закрепилась слава открывателей закона сохранения и превращения энергии (первого начала, или закона термодинамики). Естественно, что история открытия «закона сохранения энергии» тесно связана с биографиями этих ученых, что и определяет дальнейший характер изложения.
Роберт Майер (рис. 13.1) получил высшее медицинское образование в Тюбингенском университете. Решающее значение в научной карьере сыграла его поездка в качестве судового врача на голландском судне, плавающем на Яву. Именно там начались его научные исследования, приведшие его к открытию закона сохранения энергии. Как это ни странно, на это его натолкнул вид крови при обычных в то время медицинских процедурах — кровопусканиях. Цвет венозной крови зависит от потребления кислорода или от интенсивности процессов окисления, происходящих в организме.

Рис. 13.1. Портрет Роберта Майера.
Во времена Майера в умах естествоиспытателей господствовали представления витализма. Считалось, что живые организмы благодаря наличию в них некой «жизненной силы» не подчиняются законам физики и химии. Майер своими наблюдениями показал, что это совсем не так, что указанные законы действуют и в живых организмах.
По возвращении домой Майер написал статью «О количественном и качественном определении сил». В 1841 г. он отправил ее в журнал «Annalen der Physik». Главный редактор журнала И. К. Поггендорф получил ее, но печатать не стал и автору не вернул. Статья пролежала в письменном столе Поггендорфа 36 лет до самой его смерти. Конечно, редактор имел определенные основания отвергнуть статью: она была не очень хорошо написана, содержала ряд туманных и даже ошибочных идей. Но в ней содержались гениальные откровения, которые Поггендорф не смог заметить.
То, о чем не слишком внятно говорили Декарт и Ломоносов, здесь указывается с полной ясностью: «образовавшаяся теплота пропорциональна исчезнувшему движению» (речь в данном случае идет о неупругом ударе).
Не дождавшись ответа от Поггендорфа, Майер посылает вторую статью «Замечания о силах в неживой природе». Она опубликована в малочитаемом химико-фармацевтическом журнале, но сама по себе весьма примечательна. Статья содержит не только четкую формулировку закона сохранения энергии, но и глубокий анализ экспериментальных данных, полученных предшественниками Майера Румфордом и Дэви, а также им самим. Анализируя результаты опытов, Майер отвергает теплород как теоретическую основу их объяснения. Вместе с тем, увлекшись феноменологическим (термодинамическим) подходом, Майер не пытается найти объяснение природы теплоты. Поэтому он вынужден обосновывать свое открытие с помощью аналогий (например, известным из химии законом сохранения массы). В той же статье выдвинута идея эксперимента по определению механического эквивалента теплоты. Такой эксперимент осуществил в 1847 г. Дж. Джоуль, который работы Майера не знал. Здесь же, а также в письмах друзьям Майер обосновывает знаменитое уравнение, названное позднее уравнением Майера:
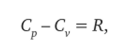
где Ср — молярная теплоемкость при постоянном давлении; Cv — молярная теплоемкость при постоянном объеме; R — универсальная газовая постоянная.
Статья Майера не привлекла внимания ученых. Интерес к закону сохранения энергии возник только после работ Джоуля и Гельмгольца. Майеру же пришлось отстаивать свой приоритет, в то время как немецкое научное сообщество не поддержало его. Майер подвергается травле и насмешкам, даже родные считали его маньяком. В 1850 г. в состоянии сильного нервного расстройства он пытается покончить с собой, выбросившись из окна. Через год родственники помещают Майера в больницу для душевнобольных. Выходит он оттуда морально и физически сломленным и вплоть до 1862 г. остается в полной неизвестности, его даже считают умершим. Впрочем, постепенно работы Майера начинают получать признание. В 1874 г. даже вышло собрание его трудов под названием «Механика тепла». Впрочем, Майеру это уже было безразлично, он умирает 20 марта 1878 г.
Интересно, что Роберт Майер с термодинамических позиций раскрыл космическую роль растений, выдвинув перед наукой проблему фотосинтеза. Поэтому Климент Аркадьевич Тимирязев (1843—1920) предпослал своей известной книге «Солнце, жизнь и хлорофилл» эпиграф из Р. Майера. Широкие философские обобщения, выдвинутые Майером, попытки распространить предложенные им законы на Космос и живую природу долгое время смущали ученых, считавших, что все это — чистая метафизика. Однако проведенные примерно в то же время опыты Дж. П. Джоуля подвели под теорию экспериментальную основу.
Джеймс Прескотт Джоуль (рис. 13.2) родился в 1818 г. Он был владельцем большого пивоваренного завода в Манчестере.

Рис. 13.2. Портрет Джеймса Прескотта Джоуля.
Уже в молодости Джоуль увлекся электрическими опытами и в 1841 г. опубликовал статью о тепловом эффекте электрического тока. Русский ученый Э. X. Ленц сделал это несколько позже, однако более тщательно. Закон выделения тепла при прохождении электрического тока носит название закона Джоуля — Ленца.
Работы по исследованию «джоулева тепла» поставили перед исследователем задачу о его природе. И вот в 1843 г. в докладе Лондонскому королевскому обществу Джоуль сообщает о том, что, согласно его представлениям, теплоту можно создавать с помощью механической работы, используя при этом «магнитоэлектричество» (электромагнитную индукцию). Эта теплота является пропорциональной квадрату силы индукционного тока. Сделав электромотор как бы посредником между тепловой энергией и механической работой, Джоуль впервые определил механический эквивалент теплоты J. Он писал: «Количество тепла, которое в состоянии нагреть 1 фунт воды на ГФ, может быть превращено в механическую силу, которая в состоянии поднять 838 фунтов на вертикальную высоту в 1 фут». Общим выводом из этих экспериментов явилось представление о сохранении энергии, в том числе и при химических превращениях в живых организмах.
Джоуль продолжал свои опыты. Он был искусным экспериментатором, его опыты становились все точнее, по мере устранения возможных источников ошибок.
В 1843 г. Джоуль выполнил эксперимент, который по праву считается фундаментальным (рис. 13.3).
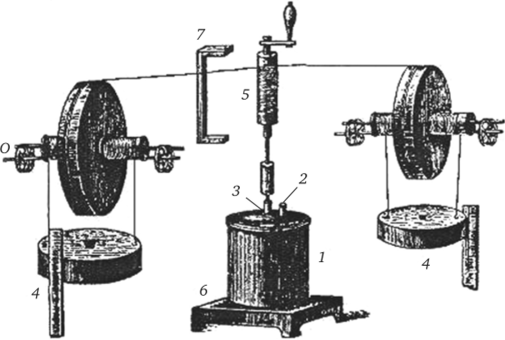
Рис. 13.3. Экспериментальная установка Дж. Джоуля.
Установка для опыта состояла из медного сосуда (калориметра) (I), закрывающегося медной герметичной крышкой, в которой имелись две трубки. В первую (2) вставлялся термометр. Во вторую трубку помещался деревянный стержень (3), на который были насажены лопатки. Сосуд заполнялся водой, и лопатки приводились во вращение с помощью двух грузов (4), подвешенных через блоки к тонкому шпагату, соединяющему грузы с центральным валом (5). Для того чтобы снизить потери энергии, сосуд ставили на деревянную подставку (6).
Сначала центральный вал был прикреплен к стержню, грузы удерживались в подвешенном состоянии с помощью рамы (7), определялось их положение над поверхностью земли и измерялась начальная температура воды. Затем вал освобождался и вращался до тех пор, пока грузы не достигали пола лаборатории. Общая высота составляла 63 дюйма (1,6 м). Опыт повторяли 20 раз, измеряя температуру воды в начале, середине и в конце каждого эксперимента. За час работы температура повышалась примерно на 0,5 °С.
Джоуль вычислил работу, которая была совершена при перемещении грузов, и количество теплоты, полученное сосудом, водой в сосуде, лопатками и др. Отношение совершенной работы А к количеству теплоты Q, т. е. механический эквивалент теплоты A/Q, получился равным (в современных единицах) 4,5 Дж/кал.
«Из этих опытов, — пишет Джоуль, — вытекал совершенно ясный вывод, что теплота и механическая сила обратимы одна в другую, и, следовательно, столь очевидно, что теплота является либо живой силой, либо некоторым состоянием притяжения или отталкивания, способным порождать живую силу».
В дальнейшем Джоуль много работал, в частности вместе с У. Томсоном (будущим лордом Кельвином) он выполнил эксперименты, которые привели к открытию эффекта Джоуля — Томсона. В 1870 г. вместе с Томсоном, Максвеллом и другими учеными он входит в состав комиссии по определению механического эквивалента теплоты. В своих воззрениях на природу теплоты Джоуль решительно поддерживал кинетическую теорию тепла, он был одним из основоположников кинетической теории газов. Умер Дж. П. Джоуль в 1889 г.
Теперь о третьем члене триады. Герман Людвиг Фердинанд Гельмгольц (рис. 13.4) родился в 1821 г. в Потсдаме в семье учителя гимназии. С 1843 г. он начал работу врачом. Затем — учеба в Берлине одновременно на двух факультетах. Физику он слушает у Г. Магнуса, физиологию — у Г. Мюллера. Научное развитие Гельмгольца происходило в условиях растущего в Германии интереса к естествознанию. В 1847 г. выходит его работа «О сохранении живой силы». Она напечатана отдельной брошюрой, так как Поггендорф отказался публиковать ее, как и статью Майера, в своем журнале.

Рис. 13.4. Портрет Германа Гельмгольца.
В деятельности Гельмгольца довольно прихотливо сочетаются физиология и физика. Он занимается физиологической оптикой и акустикой, на его счету исследования скорости передачи нервных импульсов, резонансная теория слуха, теория аккомодации глаза. Врачи-окулисты обязаны Гельмгольцу изобретением офтальмоскопа — прибора для обследования глазного дна. Недаром главный российский глазной институт носит имя Гельмгольца.
В физике Гельмгольца занимали проблемы электричества, теория колебаний, гидродинамика, метеорология, физиологическая оптика. К тому же он живо интересовался философией. С 1870 г. он — президент только что образовавшегося Физико-технического института в Берлине. Под руководством Гельмгольца институт стал крупнейшим научным центром и школой, где обучались молодые физики из разных стран. Разносторонняя деятельность принесла Гельмгольцу широкую популярность и авторитет в научном мире.
Для истории физики важны все достижения Гельмгольца, но мы подробно рассмотрим только его работу «О сохранении силы», где автор связывает закон сохранения энергии с невозможностью создания вечного двигателя.
Вопрос о вечном двигателе — отдельная область истории физики. Первый известный истории проект механического вечного двигателя принадлежит Виллару де Оннекуру (ок. 1195—.
1266) и относится к 1245 г. Свыше 500 лет подобные проекты продолжали будоражить воображение публики, пока в 1775 г. Парижская академия не отказалась рассматривать проекты вечного двигателя. Однако и сейчас время от времени такие проекты всплывают. Сегодня, когда модно отвергать общеизвестные истины, это случается и с идеей вечного двигателя.
Вернемся, однако, к Гельмгольцу. Мир, по его мнению, представляет собой совокупность материальных точек, взаимодействующих друг с другом так называемыми центральными силами. Во главу утла при этом Гельмгольц ставит принцип сохранения живой силы, требующий, чтобы количество работы при переходе из одного состояния в другое было тем же, что при обратном переходе, независимо от его способа, пути и скорости. Здесь Гельмгольц фактически вводит понятия кинетической и потенциальной энергий, называя их, правда, «живой силой» и «суммой напряженных сил». Тем самым закон сохранения живых сил приобретает вид обобщенного «закона сохранения», который может быть применен как к механическим, так и к немеханическим явлениям. В отличие от Майера, Гельмгольц уделял главное внимание физике и лишь бегло говорил о биологических явлениях. Тем не менее именно благодаря этой работе Гельмгольц получил кафедру физиологии в университете Кенигсберга. Умер Гельмгольц в 1894 г. будучи признанным лидером немецкой науки, причем не только физики, но также химии и физиологии.
Итак, Майер, Джоуль и Гельмгольц разными путями пришли к закону сохранения энергии. Наука же, благодаря их трудам и настойчивости, получила в свой арсенал фундаментальный закон.
Обратимся теперь к истории утверждения второго начала (закона) термодинамики. В XIX в. наблюдался бурный прогресс теплотехники, который стимулировал проведение научных исследований. Уточнялись основные понятия, создавалась аксиоматика, разрабатывались математические методы. Ведущую роль здесь сыграли Уильям Томсон и Рудольф Юлиус Эммануэль Клаузиус.
Уильям Томсон (лорд Кельвин) (1824—1907) — выдающийся английский физик, родился в 1824 г. в Белфасте в семье преподавателя математики. Затем семья переехала в Шотландию, в Глазго, где Томсон прожил всю жизнь. В возрасте 22 лет он становится профессором университета в Глазго и занимает кафедру в течение 53 лет до 1899 г.
Заняв кафедру, Томсон стал налаживать научную работу, которой в университете совсем не было. Для этого он, как это всегда бывает, искал пустующие помещения и занимал их все, включая винный подвал профессорского дома. У него появились добровольные помощники. Все студенты, в том числе юристы, теологи и т. д., — должны были пройти курс натурфилософии. Однако при этом от них не требовалась экспериментальная работа. Тем не менее они с энтузиазмом работали в практикуме, часто так много и усердно, что профессор начинал беспокоиться об их здоровье.
Вскоре в университете образовалась фирма по производству научных приборов. В 1870 г. университет переехал в новое великолепное здание, где было много места для научных лабораторий. Кафедра и дом Томсона первыми в Британии получили электрическое освещение. Между кафедрами и мастерскими действовала первая в стране телефонная линия. Мастерские разрослись в фабрику, ставшую как бы филиалом кафедры. Вообще Томсон был очень привязан к своему университету и, несмотря на лестные предложения занять высокие должности (директора Кавендишской лаборатории в Кембридже, ректора Эдинбургского университета и т. д.), его не покидал.
Томсон был выдающимся педагогом. Пять дней в неделю он читал ежедневно по две лекции: одну по физике, другую по математической физике. Ряд учеников Томсона стали выдающимися учеными, в том числе и те, кто сначала не помышлял о физике. Так, Джон Керр (182А—1907) — первооткрыватель электрооптического эффекта, сначала даже принял сан священника, однако в конце концов сменил карьеру священника на карьеру ученого-педагога. В 1892 г. Томсон стал лордом Кельвином (по имени реки Кельвин, протекающей вблизи университета в Глазго).
Научная деятельность Томсона связана в основном с термодинамикой, он известен, прежде всего, как создатель абсолютной шкалы температур, автор второго начала термодинамики и «отец» теории тепловой смерти Вселенной. Однако, кроме этого, им открыт также ряд важных термодинамических эффектов (например, эффект Джоуля — Томсона). Томсон известен также как исследователь в области магнетизма и физики колебаний. Скончался Томсон в 1907 г.
За свою долгую научную жизнь английский физик Уильям Томсон был автором огромного числа научных работ. Мы остановимся в основном на его вкладе в разработку второго начала термодинамики. Работа С. Карно подсказала Томсону важную мысль о возможности введения температурной шкалы, не зависящей от выбора термометрического тела. Это шкала, которая носит название шкалы Кельвина, основана на цикле Карно.
В 1851—1853 гг. Томсон в нескольких работах дал, как он выражался, «теорию движущей силы теплоты». Она зиждется на двух положениях, первое из которых восходит к Джоулю и является первым началом термодинамики. Второе положение, связанное с работами Карно и Клаузиуса, — это второе начало термодинамики, сформулированное автором следующим образом: «Невозможно при помощи неодушевленного материального деятеля получить от какой-нибудь массы вещества механическую работу путем охлаждения ее ниже температуры самого холодного из окружающих предметов». Эта так называемая томсоновская формулировка в современной интерпретации звучит так: «Невозможно построить вечный двигатель второго рода».
В 1852 г. в небольшой статье «О проявляющейся в природе общей тенденции к рассеянию механической энергии» Томсон формулирует знаменитую концепцию «тепловой смерти Вселенной». Она заключается в том, что все виды энергии во Вселенной в конце концов должны перейти в энергию теплового движения, которая равномерно распределится по веществу Вселенной, после чего в ней прекратятся все макроскопические процессы. Отметим, что в заметке фигурирует уже не «движущая сила», а энергия, т. е. термин, который ввел профессор университета в Глазго Уильям Джон Макуори Ранкин (1820—1872). Он же предложил современную формулировку закона сохранения энергии. С этого времени сам термин «энергия» и закон ее сохранения вошли во всеобщее употребление.
История открытия и утверждения в физике второго начала термодинамики связана с научной деятельностью Р. Клаузиуса.
Рудольф Юлиус Эммануэль Клаузиус (1822—1888) — выдающийся немецкий физик, родился в 1822 г. в г. Кеслине (ныне Кошалин, Польша) в семье пастора. Высшее образование он получил в Берлине, где долго выбирал, кем ему стать: физиком или историком. На наше счастье он выбрал физику. В 1850 г. вышла его первая статья по термодинамике. В ней, в частности, было дано обобщение уравнения, описывающего фазовые переходы «пар — жидкость» и «жидкость — твердое тело» (уравнение Клапейрона — Клаузиуса). В том же году появилась самая известная работа Клаузиуса, где он сформулировал второе начало термодинамики. Развивая это направление, он в 1865 г. предложил новое термодинамическое понятие — энтропию. Изучение ее свойств привело Клаузиуса к выводу о грядущей тепловой смерти Вселенной, который был опровергнут Больцманом много позже.
С 1869 г. Клаузиус работает в Боннском университете, ректором которого он потом стал. Здесь он занимается исследованиями поляризации диэлектриков (уравнение Клаузиуса — Мосотти). После франко-прусской войны (1870—1871), участвуя в которой Клаузиус получил ранение (1870), его научная активность постепенно спадает. Умер Клаузиус в 1888 г.
Итогом его термодинамических работ стал двухтомник «Сочинение о механической теории тепла». В ней приводится аналитическое выражение для первого начала термодинамики и вводится фундаментальное понятие «внутренней энергии». Первое начало Клаузиус формулирует в виде:
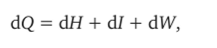
где dQ — бесконечно малое количество теплоты, сообщенное телу; dН — бесконечно малое приращение количества теплоты, заключенного в теле; d/ — внутренняя работа; dW — внешняя работа. Принимаем, что:
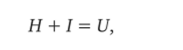
где U — внутренняя энергия. С учетом этого:
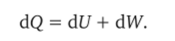
В книге приведены также данные, которые свидетельствуют о значительном вкладе Клаузиуса в кинетическую теорию газов. Ему принадлежит приоритет введения в нее статистических методов и понятий, в том числе таких, как средняя длина пробега частиц и др.
В статье 1850 г. Клаузиус, опираясь на работу Карно, формулирует второе начало термодинамики: «Теплота не может переходить сама собой от более холодного тела к более теплому». Устав объяснять, что же такое «сама собой», он впоследствии дал новую формулировку: «Переход теплоты от более холодного тела к более теплому не может иметь места без компенсации».
В 1854 г. Клаузиус в статье «Об измененной форме второго начала механической теории тепла» доказывает теорему Карно, исходя из своего постулата, и, обобщая ее, дает математическое выражение второго начала в виде неравенства. Для круговых процессов:
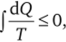
где знак «<�» относится к необратимым процессам; знак «=» — к обратимым.
В 1865 г. Клаузиус ввел новую величину, которая сыграла фундаментальную роль в последующем развитии термодинамики. Эта новая величина — энтропия S (от греч. «тропэ» — превращение) — математически строго определена, но физически мало наглядна. Клаузиус показал, что абсолютное значение энтропии остается неопределенным, определены лишь ее изменения в термически изолированных системах. В идеальном случае обратимых процессов энтропия остается постоянной. Энтропия как функции температуры т:
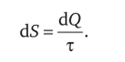
При этом для обратимых процессов:
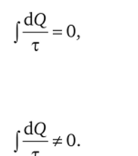
а для необратимых:
Тем самым Клаузиус показал, что изменение энтропии определяет направление протекания процессов. Последнее выражение, по Клаузиусу, является математической формулировкой второго начала термодинамики. Было установлено важнейшее свойство энтропии: в замкнутой системе она не может убывать. Второе начало термодинамики теперь формулируется так: «Энтропия Вселенной стремится к максимуму». Таким образом, через 20 лет после Томсона Клаузиус также приходит к «тепловой смерти Вселенной».
Идея тепловой смерти Вселенной вызвала значительные возражения в среде ученых. Одно из таких возражений — мысленный эксперимент, который носит название «демон Максвелла» и относится к 1870 г. Максвелл считал, что второе начало термодинамики имеет ограниченную область применения. По его мнению, в микромире могут осуществляться процессы, которые идут в направлении, противоположном указываемому вторым началом термодинамики. В частности, можно было представить себе микроскопическое существо («демона»), которое в рамках молекулярно-кинетической теории разделяет быстрые и медленные молекулы. Демон без затраты энергии понижает температуру в одной части сосуда и повышает в другой.
Демон Максвелла — шаг на пути к статистическому пониманию второго начала термодинамики (см. гл. 14). Он породил широкую дискуссию, результатом которой стало понимание того факта, что законы микромира не дают возможности осуществить эксперимент Максвелла.
В XX столетии теория энтропии обогатилась еще одним фундаментальным физическим принципом. В 1906 г. немецкий физик Вальтер Нернст сформулировал новый, независимый от первого и второго начал принцип термодинамики. Его иногда называют третьим началом (законом) термодинамики. Он вводит в термодинамику некоторые абсолютные значения, в частности абсолютное значение энтропии. Второе начало термодинамики указывает на существование и изменение энтропии S, определяемой через дифференциал dS, поэтому энтропия определена с точностью до постоянной интегрирования. Этого достаточно, чтобы решать задачи, в которые входят изменения энтропии. Но существуют задачи, требующие знания ее абсолютного значения.
Вальтер Фридрих Герман Нернст (1864—1941) — немецкий физик и химик, один из основоположников физической химии, родился в 1864 г. Он окончил Вюрцбургский университет (1887), в 1891— 1902 гг. был профессором Геттингенского университета. Там Нернст создал Институт физической химии и электрохимии. Вместе с присоединившейся к нему группой ученых из разных стран он занимался изучением таких проблем, как поляризация, диэлектрические константы и химическое равновесие. В 1905 г. Нернст покинул Геттинген, чтобы стать профессором химии в Берлинском университете.
В 1912 г., исходя из выведенного им теплового закона, ученый обосновал недостижимость абсолютного нуля. «Невозможно создать тепловую машину, в которой температура вещества снижалась бы до абсолютного нуля». Нернст предположил, что по мере того, как температура приближается к абсолютному нулю, возникает тенденция к исчезновению физической активности веществ. Третье начало термодинамики имеет важнейшей значение для физики низких температур и физики твердого тела.
Вплоть до конца своей профессиональной деятельности Нернст занимался изучением космологических проблем, возникших в результате открытия им третьего начала термодинамики, особенно так называемой тепловой смертью Вселенной, против которой он выступал, а также фотохимией и химической кинетикой.
В 1920 г. ему была вручена Нобелевская премия по химии «в признание его работ по термодинамике». В 1934 г. Нернст вышел в отставку и поселился в своем доме. В 1941 г. он скончался от сердечного приступа.
Путь, которым шел Нернст, можно представить следующим образом. Энтропия системы может быть представлена в виде интеграла: 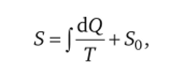
где Q — количество теплоты, которое система получила или потеряла в течение времени действия рассматриваемого процесса; Т — абсолютная температура; a S0 — постоянная интегрирования, не зависящая от температуры.
В результате изучения низкотемпературных процессов Нернст обнаружил, что при температурах, близких к абсолютному нулю, изменения энтропии становятся очень малыми. Он предположил, что энтропия стремится к постоянному значению S^ когда температура стремится к абсолютному нулю. Это значение не зависит от параметров и состояния системы. Константу S0 можно рассматривать как нулевое значение энтропии.
Из третьего начала термодинамики были сделаны такие важные выводы, как стремление теплоемкости к нулю, когда температура стремится к абсолютному нулю, недостижимость температуры абсолютного нуля (при принципиальной возможности получить любое приближение к нему).
Контрольные вопросы.
- 1. Какой важный вывод был сделан в результате опытов Румфорда и Дэви?
- 2. За какими учеными закрепилась слава открывателей первого начала термодинамики?
- 3. На основе каких наблюдений Майер пришел к открытию закона сохранения и превращения энергии?
- 4. Как записывается уравнение Майера? В чем состоит его физический смысл?
- 5. Какими открытиями известен Джоуль в истории физики?
- 6. В чем заключался фундаментальный опыт Джоуля по измерению механического эквивалента теплоты?
- 7. Что в современной физике понимают под «живой силой» и «суммой напряженных сил»?
- 8. Как записал первое начало термодинамики Клаузиус?
- 9. Как звучит второе начало термодинамики в формулировках Томсона и Клаузиуса?
- 10. В чем состоит физический смысл энтропии?
- 11. Что представляет собой: а) идея тепловой смерти Вселенной; б) парадокс «демон Максвелла»?
- 12. Как формулируется третье начало термодинамики?
Задания для самостоятельной работы
- 1. Роберт Майер. Биография и научная деятельность.
- 2. Научные достижения Джеймса Джоуля.
- 3. Многосторонний ученый Герман Гельмгольц: между физикой и физиологией.
- 4. История утверждения второго начала термодинамики.
- 5. Уильям Томсон. Биография. Успехи. Заблуждения.
- 6. История открытия эффекта Джоуля — Томсона.
- 7. Научная биография Рудольфа Клаузиуса.
- 8. Вечные двигатели первого и второго рода. Исторический аспект.
- 9. История «тепловой смерти Вселенной».
- 10. Вальтер Нернст и третье начало термодинамики.
Рекомендуемая литература
- 1. Кудрявцев, П. С. Курс истории физики. — 2-е изд. — М.: Просвещение, 1982.
- 2. Кудрявцев, П. С. История физики: в 3 т. — М.: Просвещение, 1956—1971.
- 3. Спасский, Б. И. История физики: в 2 т. — М.: Высшая школа, 1977.
- 4. Дорфман, Я. Г. Всемирная история физики: в 2 т. — М.: Наука, 1974—1979.
- 5. Голин, Г. М. Классики физической науки (с древнейших времен до начала XX в.) / Г. М. Голин, С. Р. Филонович. — М.: Высшая школа, 1989.
- 6. Храмов, Ю. А. Физики. Биографический справочник. — М.: Наука, 1983.
- 7. Лауреаты Нобелевской премии: энциклопедия: пер. с англ. — М.: Прогресс, 1992.
- 8. Томсон, У. Второе начало термодинамики. — 2-е изд. / У. Томсон, С. Карно, Р. Клаузиус, Л. Больцман, М. Смолуховский. — М.: ЛКИ, 2007.
- 9. Невзоров, Б. П. История фундаментальных понятий физики. Часть III: Молекулярная физика и строение вещества. Механика сплошных сред / Б. П. Невзоров, А. С. Поплавной, В. Е. Тупицын. — Кемерово: Кемеровский госуниверситет, 2001.
- 10. Орлов, В. А. Равновесная и неравновесная термодинамика. Элективный курс: учеб, пособие / В. А. Орлов, Г. Г. Никифоров. — М.: Бином, Лаборатория знаний, 2005.
- 11. Тельфер, Я. М. История и методология термодинамики и статистической физики. — М.: Высшая школа, 1981.
- 12. Майер, Р. Закон сохранения и превращения энергии. Четыре исследования 1841—1851. — М.; Л.: Гостехиздат, 1933.
- 13. Бродянский, В. М. Сади Карно. — М.: Наука, 1993.
- 14. Физика XIX — XX вв. в общенаучном и социокультурном контекстах. Физика XIX в. / отв. ред. В. П. Визгин, Л. С. Полак. — М.: Наука, 1995.
- 15. Книжные серии «ЖЗЛ»: «Люди науки», «Творцы науки и техники».