Очистка от соединений марганца

Удаление марганца аэрацией с подщелачиванием воды применяют при одновременном присутствии в ней марганца и железа. При аэрации воды удаляется часть диоксида углерода и происходит ее насыщение кислородом воздуха. При удалении С02 возрастает pH сточной воды, что способствует ускорению процессов окисления и гидролиза железа и частично марганца с образованием гидроксидов. Двухвалентный марганец… Читать ещё >
Очистка от соединений марганца (реферат, курсовая, диплом, контрольная)
Соединения марганца содержатся в сточной воде металлургических, машиностроительных и химических производств. При концентрации марганца более 0,05 мг/л вода окрашивается в темный цвет. Некоторые производства предъявляют жесткие требования к содержанию марганца в воде (бумажная, текстильная, кинокопировальная, синтетических волокон, пластмасс). Удаление из воды марганца может быть достигнуто следующими методами: 1) обработкой воды перманганатом калия; 2) аэрацией, совмещенной с известкованием; 3) фильтрованием воды через марганцевый песок или марганцевый катионит; 4) окислением озоном, хлором или диоксидом хлора.
При обработке воды перманганатом калия достигается одновременная очистка от марганца и от железа. Перманганат калия окисляют с образованием малорастворимого диоксида марганца:
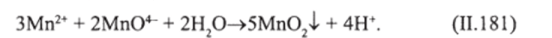
В этом процессе 1 кг КМп04 окисляет 0,53 мг Мп2 Наибольший эффект достигается при обработке воды дозой 2 мг КМп04 на 1 мг. Осадок диоксида марганца удаляют фильтрованием.
Удаление марганца аэрацией с подщелачиванием воды применяют при одновременном присутствии в ней марганца и железа. При аэрации воды удаляется часть диоксида углерода и происходит ее насыщение кислородом воздуха. При удалении С02 возрастает pH сточной воды, что способствует ускорению процессов окисления и гидролиза железа и частично марганца с образованием гидроксидов.
Двухвалентный марганец медленно окисляется в трехи четырехвалентный растворенным в воде кислородом. Окисление марганца происходит при pH = 9−9,5. Образующийся гидроксид марганца выпадает в осадок в виде Мп (ОН)3 и Мп (ОН)4. Растворимость этих соединений 0,01 мг/л, образующийся Мп (ОН)4 снова участвует в процессе, являясь катализатором окисления марганца.
При pH = 9,5 марганец удаляется почти полностью, при рН<7,5 кислородом воздуха он почти не окисляется. Для ускорения процесса окисления марганца воду после аэрации до подачи на фильтры подщелачивают известью или содой для повышения pH, затем осветляют в осветлителях или отстойниках. Процесс окисления Мп2* резко ускоряется, если аэрированную воду фильтруют через контактный фильтр, загруженный дробленым пиролюзитом (Мп02 Н20), либо кварцевым песком, предварительно обработанным оксидами марганца.
Двухвалентный марганец может быть удален из воды в процессе окисления его хлором, озоном или диоксидом хлора. Скорость окисления Мп хлором зависит от pH среды. При pH = 7 за 60−90 минут окисляется всего 50% Мп2*. При подщелачивании известью до pH = 8 Мп окисляется практически полностью. Расход С12 на окисление 1 кг Мп составляет 1,3 мг. При наличии в воде аммонийных солей расход хлора увеличивается.
Диоксид хлора и озон при pH = 6,5−7 окисляют Мп2' за 10−15 минут. На окисление 1 мг Мп2+ расходуется 1,35 мг С102 или 1,45 мг 03. Однако применение этих окислителей требует строительства сложных установок, поэтому их практически нс используют.
Марганец может быть удален из воды биохимическим окислением. Процесс проводят следующим образом. На песке фильтра высеивают особый вид марганецпотребляющих бактерий, которые в процессе своей жизнедеятельности поглощают из воды марганец. Отмирающие бактерии образуют на зернах песка пористую массу с высоким содержанием оксида марганца, который служит катализатором процесса окисления.
Марганец из воды может быть удален при помощи марганцевого катионита, который приготовляют, пропуская через любой катионит в натриевой форме растворы хлорида марганца и перманганата калия. При этом происходят следующие реакции:
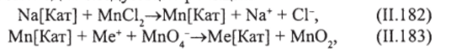
(где Me — катион Na* или К+).
В этих процессах перманганат калия окисляет марганец с образованием оксидов марганца, которые в виде пленки оседают на поверхности зерен катионита. При регенерации пленку восстанавливают раствором перманганата калия.
Из рассмотренных методов наиболее эффективным является метод обработки перманганатом калия. Он не требует сложного оборудования и просто контролируется.
Вопросы для повторения
- 1. Рассмотрите использование процесса нейтрализации для очистки сточных вод, а также области его применения, достоинства, недостатки и эффективность.
- 2. Объясните суть процессов очистки сточных вод окислением хлором, кислородом, озоном. Назовите области применения и эффективность.
- 3. Рассмотрите основные схемы и аппараты процессов озонирования.
- 4. Рассмотрите основы реагентных методов удаления из сточных вод ионов тяжелых металлов. Достоинства и недостатки методов и эффективность.