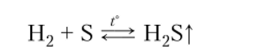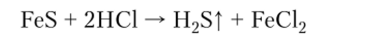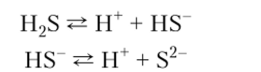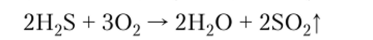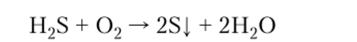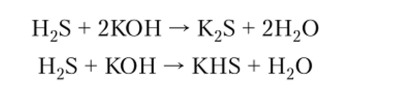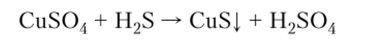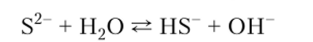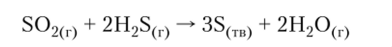Сероводород H2S — ядовитый бесцветный газ с запахом тухлых яиц, хорошо растворяется в воде. Для серы свойственно также образование полисульфанов H2Sп. Соединения с числом атомов серы п = 2-^8 выделены в индивидуальном состоянии, более высокие гомологи существуют в виде смесей. Полисульфаны неустойчивы и легко диспропорционируют на сероводород и свободную серу.
Получение. В промышленности сероводород образуется при взаимодействии серы с водородом, часто является нежелательным продуктом химического производства: 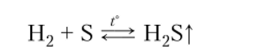
В лаборатории сероводород получают в аппарате Киппа при взаимодействии сульфидов металлов и кислоты:
Химические свойства сероводорода заключаются в следующем.
1. Раствор сероводорода в воде — слабая двухосновная кислота; ее средние соли называются сульфидами:
2. С избытком кислорода газ образует взрывчатую смесь:
При недостатке 02 наблюдается осаждение вещества желтого цвета:
3. Сероводород реагирует со щелочами с образованием кислых или средних солей: 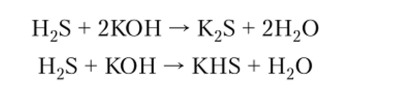
4. Способность сероводорода осаждать сульфиды из растворов солей используется в аналитической химии как качественная реакция на катионы:
Большинство сульфидов нерастворимо в воде, цвет осадков нерастворимых сульфидов: CuS — коричневый, ZnS — белый, PbS — черный, HgS — красный.
5. Растворимые сульфиды в водных растворах легко подвергаются гидролизу по аниону с образованием щелочной среды:
6. Сероводород и все сульфиды являются сильными восстановителями, в растворах окисляются до серы или сульфат-аниона:
7. Реакция сероводорода с диоксидом серы имеет практическое применение для регенерации серы из отходящих газов металлургического производства: 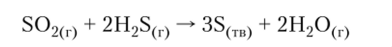
Кислородсодержащие соединения серы приведены в табл. 16.4.
Таблица 16.4
Кислородсодержащие соединения серы.
Степень окисления. | (+4). | (+6). |
Оксид. | so2 | SO;,. |
Кислота (соль). | H2SO:) сернистая (сульфит). | H2so< серная (сульфат). |