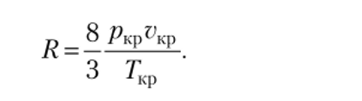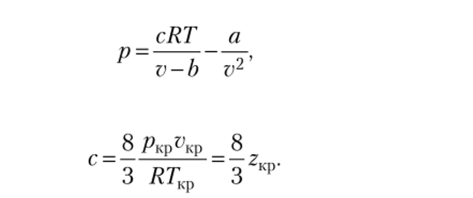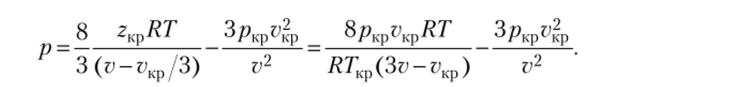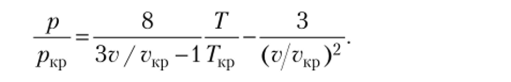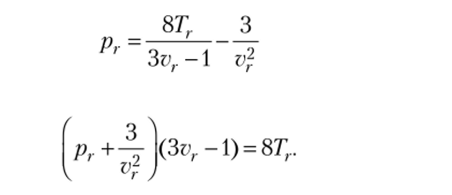Как можно заметить, мы использовали лишь два условия из трех для определения параметров а и b уравнения состояния Ван-дер-Ваальса. Иногда можно встретить попытки «уточнения» газовой постоянной R в критической точке с помощью соотношения.
На наш взгляд, это только приводит к путанице, и, если необходимо, лучше ввести третий параметр с в уравнение Ван-дер-Ваальса, записав его в виде где.
Подставляя коэффициенты а, b и с, выраженные через критические параметры в уравнение Ваи-дер-Ваальса, получаем.
Это соотношение можно записать так:
Безразмерные величины.
называются приведенными параметрами, с их помощью уравнение состояния можно записать в обобщенном виде таким образом:
или Уравнение состояния Ван-дер-Ваальса в обобщенном виде нс зависит от свойств какого-либо вещества. Переход от обобщенного уравнения состояния к уравнению состояния конкретного вещества осуществляется с использованием параметров критической точки этого вещества.
Возможность представления уравнения состояния Ван-дер-Ваальса в обобщенном виде является проявлением закона соответственных состояний.
Соответственными называют такие состояния разных веществ, которые имеют одинаковые значения приведенных параметров.
Для уравнений состояния кубического типа из закона соответственных состояний следует, что если совпадают значения двух приведенных параметров, то должны совпадать и значения третьего приведенного параметра.
Следует иметь в виду, что уравнение Ван-дер-Ваальса имеет скорее теоретическое, чем прикладное значение, поскольку с его помощью можно получить в большинстве случаев только качественное описание p—v—T зависимости реальных газов.