Процессы радиолиза.
Атомная и ядерная физика: радиоактивность и ионизирующие излучения

При радиолизе аммиака распад его молекулы происходит с образованием атома водорода и радикалов NH2 (NH3—>NH2 + Н), которые затем по реакции рекомбинации превращаются в молекулярный водород и гидразин NH2-NH2. Выход гидразина мал (1−2 молекулы на юо эВ), но радиационный процесс перспективен, т. к. существующие методы получения гидразина трудоёмки и сложны. При облучении углекислого газа образуются… Читать ещё >
Процессы радиолиза. Атомная и ядерная физика: радиоактивность и ионизирующие излучения (реферат, курсовая, диплом, контрольная)
Газы
При действии радиации на многие вещества образуются газообразные продукты. Так, при облучении аммиака NH3 получается гидразин N2H4 и молекулярный водород; оксиды марганца в результате облучения выделяют кислород; при облучении твёрдого нитрата образуется нитрит натрия, молекулярный азот и кислород.
Процессы, происходящие при облучении простых неорганических соединений, разнообразны, но все их можно свести к превращениям ионов, возбужденных молекул, и радикалов. Например, при действии ионизирующего излучения на кислород в небольших количествах образуется более реакционноспособный озон. Взаимодействуя с возбужденными молекулами и атомами кислорода, он вновь превращается в кислород. Выход озона в жидком кислороде (G=13.6) много выше выхода образования озона в газообразном кислороде (G=1.5).
Аллотропные переходы, наблюдаемые при облучении кислорода (кислород—юзон), происходят и при действии излучения на другие простые соединения. Так, при облучении белое олово переходит в серое, алмаз в графит, аморфный селен в кристаллический. В результате действия излучения разрываются связи между атомами простого соединения, и эти атомы перестраиваются в новую молекулу или образуют кристалл с другой решёткой, чем была раньше.
При радиолизе аммиака распад его молекулы происходит с образованием атома водорода и радикалов NH2 (NH3—>NH2 + Н), которые затем по реакции рекомбинации превращаются в молекулярный водород и гидразин NH2-NH2. Выход гидразина мал (1−2 молекулы на юо эВ), но радиационный процесс перспективен, т. к. существующие методы получения гидразина трудоёмки и сложны. При облучении углекислого газа образуются оксид углерода и молекулярный кислород. Разложение С02 протекает с выходом 8 молекул на юо эВ. При облучении смеси азота и кислорода образуется оксиды азота: N20, N0 и N02. Есть и другие радиационнохимические превращения в смесях газов, например, процессы окисления S02 в S03, и преобразования НС1 в С1а. Выходы продуктов в таких цепных процессах достигают тысяч молекул на юо эВ.
Основной продукт разложения воды — гремучий газ (смесь двух объёмов водорода и одного объёма кислорода), который является взрывчатым веществом. Эта особенность радиолиза воды создала большие трудности при её использовании в атомном реакторе.
При прохождении ионизирующего излучения через воду в ней образуются ионы и возбужденные молекулы:

Появляющийся ион Н20+ и свободный электрон очень быстро реагируют с молекулами воды. 
Путём превращения первоначально неустойчивых ионов образуются радикалы Н и ОН и новые, устойчивые в воде ионы гидроксония Н30+ и гидроксила ОН'. Атомарный водород и радикал гидроксил неустойчивы, время их жизни не превышает миллисекунд. За это время движущиеся в воде радикалы Н и ОН успевают вступить в дальнейшие взаимодействия.

В результате этих реакций вновь образуется вода, и появляются новые, уже устойчивые соединения — молекулярный водород и перекись водорода. Они называются молекулярными продуктами радиолиза воды в отличие от неустойчивых радикальных продуктов Н и ОН. Происходящие при радиолизе воды процессы можно представить в виде цепочки последовательных превращений: вода—>ионы (Н20+, е)—^радикалы (Н и ОН)—^молекулярные продукты (Н2, Н202).
Молекулярные продукты при облучении воды накапливаются в очень малой концентрации — не более десятитысячных долей процента от количества исходного вещества. Это вызвано разрушением образующихся соединений радикалами Н и ОН.

Радикалы, порождая молекулярные продукты, их же и разрушают. Происходит круговорот:
вода —> продукты радиолиза —? вода. (13).
Однако этот круговорот можно нарушить. Один способ — уводить из системы продукты радиолиза, откачивая водород или превращая перекись водорода в перекись бария, выпадающую в осадок. Другой — вводить какиелибо вещества, которые, не реагируя с молекулярными продуктами радиолиза воды, будут реагировать с радикалами Н и ОН, тем самым защищая молекулярные продукты радиолиза воды от разрушения.
Кроме приведенных выше реакций протекают ещё две.

В результате всех этих превращений в воде остается только малое количество молекулярного кислорода и молекулярного водорода.
Если облучать не чистую воду, а раствор какого-либо соединения, то радикалы Н и ОН вместо того, чтобы разрушать молекулярные продукты радиолиза воды, будут реагировать с молекулами растворенного соединения, вызывая различные его превращения — окисление, восстановление, деструкцию, полимеризацию и т. д.
Радикал гидроксила ОН обнаружен при облучении водных растворов акрилонитрила CH2=CHCN. Молекула акрилонитрила не содержит в своём составе атомов кислорода, однако при его облучении в водном растворе образуется полиакрилонитрил с гидроксильными группами. Методом парамагнитного резонанса было подтверждено образование радикала Н (атомарный водород) и радикала гидроксила. Атомарный водород является сильным восстановителем (способен легко отдавать свой электрон), а радикал гидроксила — окислителем (энергично отнимает электрон у других соединений), поэтому они оказывают противоположное воздействие на растворенные вещества, как это можно видеть на следующих примерах:
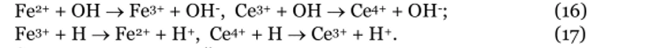
Это косвенное воздействие излучения. В концентрированных растворах превращение растворённого соединения может происходить и в результате «прямого» действия излучения, когда оно взаимодействует непосредственно с молекулами растворённого вещества, вызывая их ионизацию, которая, в свою очередь, приводит к появлению радикальных и молекулярных продуктов. В разбавленных растворах преобладает косвенное воздействие, а в концентрированных — оба эффекта.
Для большинства соединений, превращения которых идут не по цепному механизму, выходы составляют 44−5 ионов или молекул на 100 эВ. В более концентрированных растворах они несколько повышаются, достигая 12 ионов или молекул на юо эВ. В случае воды и водных растворов коэффициент полезного использования энергии излучения мал — не более ю%. Поэтому для промышленности важны только цепные радиационнохимические процессы, либо процессы, в которых образуется соединение, которое если и можно получить другими методами, то с большими затратами энергии. Примерами являются окисление бензола в фенол, этилена в уксусный альдегид и др.