Аминокислоты.
Белки. Практические работы и семинарские занятия по органической химии

Реактив Миллона готовят растворением 1 г ртути в 2 мл концентрированной HN03 (d = 1,42) сначала на холоду, а затем при нагревании? осторожно, под тягой! < Реактив разбавляют двойным объемом воды, оставляют на 2 ч и декантацией сливают с осадка. Реакция на серу в белках. В 1 мл 10%-го раствора яичного альбумина вливают 1 мл 30%-го раствора гидроксида натрия и 3—4 капли раствора ацетата свинца. При… Читать ещё >
Аминокислоты. Белки. Практические работы и семинарские занятия по органической химии (реферат, курсовая, диплом, контрольная)
Все описываемые ниже качественные реакции приведены для а-аминокислот, имеющих наиболее важное значение в жизни организмов. Аминокислоты других типов обычно обнаруживают, используя качественные реакции на аминои карбоксильную группы.
Реакция аминокислот с FeClq. При действии FeCl3 в водных растворах на аминокислоты образуются хелаты, окрашенные в красный цвет:
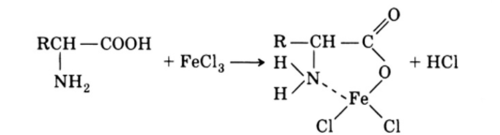
При добавлении минеральных кислот окраска исчезает.
К 0,05 г а-аминокислоты, растворенной в 1 мл воды, добавляют каплю 3%-го раствора FeCl3. Возникшая красная окраска доказывает присутствие аминокислот[1].
Реакция с нингндрином. Трикетогидринден (I) дегидрирует аминокислоту (II) до иминокислоты (III), превращаясь в спирт (IV). Иминокислота разлагается, образуя альдегид, С02 и NH3. Последний конденсируется с избытком нингидрина (I) и спиртом (IV), давая сине-фиолетовый краситель (V):
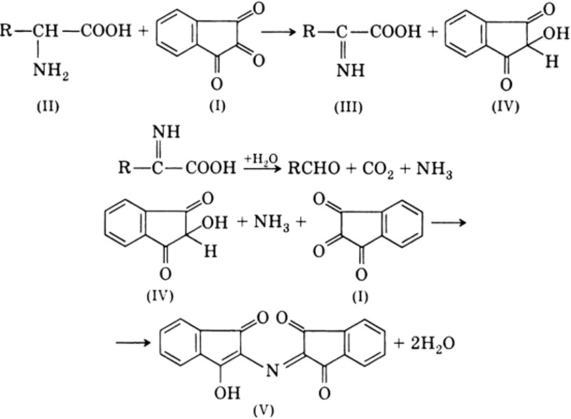
В 1 мл 1%-го раствора аминокислоты вливают каплю 0,03%-го раствора нингидрина. Смесь в микропробирке нагревают до кипения. Появление желтой, красной или синей окраски подтверждает присутствие аминокислоты.
Реакция с солями меди. В слабокислых средах аминокислоты дают с солями меди ярко-синие хелаты:
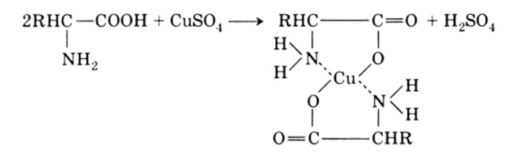
Для сдвига равновесия реакции вправо ее лучше проводить в буферном растворе с добавкой ацетата натрия.
В 1 мл 1%-го раствора аминокислоты вносят кристаллик медного купороса и кристаллик ацетата натрия. В присутствии аминокислоты раствор становится густо-синим.
Ксантопротеиновая реакция на белки. В пробирку вносят около 1 мл 10%-го раствора яичного альбумина и 1 мл концентрированной азотной кислоты.
Примечание. Белок куриного яйца отделяют от желтка, растворяют при размешивании в 200 мл воды и фильтруют через вату.
Образующийся при нагревании сгусток белка окрашивается в желтый цвет, который от добавления крепкого раствора аммиака переходит в оранжевый. Окрашивание возникает в результате нитрования остатков ароматических аминокислот белковой молекулы.
Ксантопротеиновая реакция обнаруживает наличие в белке одиночных пли конденсированных ароматических ядер, т. е. остатков таких кислот, как фенилаланин, тирозин, триптофан. Желтое окрашивание появляется в результате нитрования этих ядер азотной кислотой и образования полинитросоединений. Переход в щелочной среде желтой окраски подобных веществ в оранжевую обусловлен образованием более интенсивно окрашенных анионов.
Кислотные альбуминаты, образующиеся при энергичном действии кислот на белки, нерастворимы в воде и в разбавленных растворах солей, но хорошо растворяются в щелочах и разбавленных кислотах. Кислотные альбуминаты связывают значительно большее количество щелочи, чем исходный белок.
Чистый желатин не содержит аминокислот, перечисленных выше, и не дает ксантопротеиновой реакции.
Биуретовая реакция на белки. В пробирку с 1 мл 10% -го раствора яичного альбумина вливают 1 мл 10%-го раствора гидроксида натрия и 2 капли 2%-го раствора медного купороса. Появляется красно-фиолетовое окрашивание, указывающее на наличие в белковой молекуле пептидных связей —СО—NH—.
Продукты распада белка — полипептиды — также дают биуретовую реакцию. Цвет образующихся медных комплексов определяется числом аминокислот, связанных пептидной связью. Дипептиды дают синюю окраску, трипептиды — фиолетовую, а тетрапептиды и более сложные пептиды — красную. Фиолетовый цвет медного комплекса с белком в условиях проведения биуретовой реакции указывает на преобладание в сложной белковой частице трипептидных группировок (это подтверждается и другими данными).
Некоторые атомные группы, как —CS—NH—, —C (NH)NH—, накапливаясь в молекуле, также дают биуретовую реакцию. При ее проведении следует избегать избытка медной соли, так как образующийся в этом случае синий гидроксид меди (И) маскирует появление фиолетовой окраски.
Реакция на серу в белках. В 1 мл 10%-го раствора яичного альбумина вливают 1 мл 30%-го раствора гидроксида натрия и 3—4 капли раствора ацетата свинца. При кипячении выделяется коричнево-черный осадок сульфида свинца.
Реакция Миллона. При использовании реакции Миллона как реакции на белок основываются на присутствии в большинстве белков тирозина, являющегося замещенным фенолом.
К 1 мл 10%-го раствора яичного белка прибавляют 1 мл реактива Миллона и нагревают смесь в пробирке. Образование кирпично-красного сгустка указывает на присутствие белка.
Реактив Миллона готовят растворением 1 г ртути в 2 мл концентрированной HN03 (d = 1,42) сначала на холоду, а затем при нагревании? осторожно, под тягой! < Реактив разбавляют двойным объемом воды, оставляют на 2 ч и декантацией сливают с осадка.
- [1] См. также реакцию фенолов и енолов (с. 130).