Кинетика возникновения зародышей новой фазы в метастабильной системе

Следуя Я. Б. Френкелю, применим представления о распределении частиц по размерам к анализу кинетики возникновения зародышей новой фазы при фазовых переходах. Приложение уравнения (VI.9), описывающего распределение частиц по размерам, к мстастабильной системе, т. е. при Др' = цст — ц" > 0 (и в предположении о том, что межфазное натяжение не зависит от размера частиц), дает кривую распределения… Читать ещё >
Кинетика возникновения зародышей новой фазы в метастабильной системе (реферат, курсовая, диплом, контрольная)
Термодинамическое рассмотрение возникновения зародышей новой фазы в макроскопической системе, находящейся в метастабильном состоянии, показывает, что для различных фазовых переходов и при разных условиях зародышеобразования (гомогенное или гетерогенное) существует энергетический барьер, препятствующий появлению зародышей. Возникновение зародышей может рассматриваться при этом как флуктуационный процесс преодоления системой энергетического барьера. Как и для других подобных процессов, можно полагать, что частота возникновения зародышей новой фазы J должна экспоненциально зависеть от высоты энергетического барьера, т. е. от работы образования критического зародыша Wc:

Величина Wc уменьшается по мере внедрения в метастабильную область, а также при введении поверхностей, избирательно смачиваемых новой фазой; напротив, предэкспоненциальный множитель/0 не зависит (или слабо зависит) от глубины внедрения в метастабильную область и определяется механизмом преодоления зародышами новой фазы энергетического барьера.
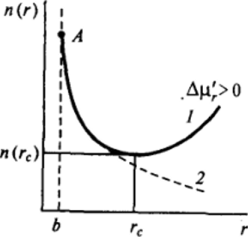
Следуя Я. Б. Френкелю, применим представления о распределении частиц по размерам к анализу кинетики возникновения зародышей новой фазы при фазовых переходах. Приложение уравнения (VI.9), описывающего распределение частиц по размерам, к мстастабильной системе, т. е. при Др' = цст — ц" > 0 (и в предположении о том, что межфазное натяжение не зависит от размера частиц), дает кривую распределения концентрации частиц по радиусам п (г) с минимумом (рис. VI-26). Такая форма кривой распределения означает, что термодинамически равновесному состоянию отвечает образование частиц только большого размера. Следует иметь в виду, что начальному состоянию системы соответствует крайняя левая точка А (состояние гомогенности молекулярного раствора); равновесная кривая распределения должна возникать постепенно, начиная с самых малых размеров частиц, причем частицы, оказавшиеся крупнее тех, которым отвечает минимум на кривой п (г), увеличивают свои размеры.
В первом приближении можно полагать, что сравнительно быстро установится квазиравновесное распределение, отвечающее только левой ветви (до минимума) равновесной кривой. Тогда n (rt) отражает концентрацию критических зародышей, и для перехода к частоте возникновения зародышей с размерами, большими критических (сверхкритических зародышей), эту концентрацию следует разделить на некоторое характерное время существования критического зародыша tt. Время tt может быть оценено, например, как среднее время, необходимое для присоединения к критическому зародышу еще одной молекулы, переводящей его в «сверхкритическое состояние*. Используя выражение (VI .9) для определения концентрации n{rt) частиц радиусом г, в равновесной системе, можно оценить частоту перехода зародышей новой фазы через критический радиус г{ (т. с. через энергетический барьер):
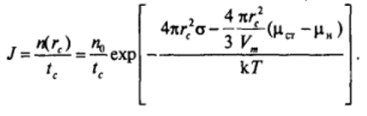
Соответственно, учитывая (VI.9), имеем:
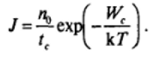
Рис. VI-26. Равновесное распределение частиц по размерам при Дц * К" «К > О по Уравнению (VI.9) (кривая /) и стационарное распределение при образовании зародышей новой фазы (кривая 2).
Таким образом, предэкспоненциальный множитель /0 выражения (VI. 18) может рассматриваться как величина, определяемая отношением числа молекул в единице объема метастабильной фазы nt ко времени жизни критического зародыша tt. Такое рассмотрение подчеркивает, что формирование зародышей новой фазы — это не столкновение сразу большого числа молекул (такое столкновение было бы слишком маловероятным), а постепенное «дорастание* частиц до критического размера. Следуя Я. Б. Зельдовичу, этот процесс можно рассматривать как «диффузию частиц в пространстве размеров*. Среди множества частиц, которые, случайно возникнув, затем растворяются, не достигнув критического размера, встречаются немногие («наиболее упрямые*), которые все-таки, в результате затянувшейся во времени флуктуации, превращаются в критический зародыш и затем в частицу новой фазы. Более полное рассмотрение должно учитывать, что быстрый рост сверхкритических зародышей (и тем самым их «выход из игры*) приводит к изменению формы кривой распределения (рис. VI-26, кривая 2) и появлению в выражении для частоты образования зародышей некоторого «фактора неравновесности*, меньшего 1. Вместе с тем следует иметь в виду время установления распределения частиц по размерам, близком к равновесному.
Предполагая, что предэкспоненциальный множитель выражения (VI. 18) определяется отношением числа молекул в единице объема метастабильной фазы по ко времени жизни критических зародышей /с, проанализируем влияние природы фазового перехода на частоту зародышеобразования.
Величину 1С можно представить в виде (5^)", где Sc — поверхность критического зародыша; q — частота присоединения молекул к единице поверхности новой фазы.
При конденсации паров с давлением р" частота присоединения молекул к единице поверхности критического зародыша может считаться равной частоте соударения молекул с поверхностью. Эта последняя в соответствии с молекулярно-кинетической теорией определяется выражением.
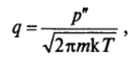
где т — масса молекулы. Следовательно, в этом случае частота образования зародышей новой фазы может быть оценена как.
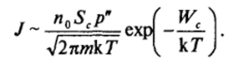
Для частиц радиусом ~10 нм при давлении, отвечающем давлению паров воды при комнатной температуре 20 мм рт. ст., т. е. 3 • 103 Н/м2, и массе молекул воды ~ 3 • 1(Г25 г, такие оценки приводят к 1С ~ 10″10 с; при по «6 • 1023 молекул в кубическом метре Уо — Ю34 м»3— с" 1. Заметим, что подобная оценка дает значение предэкспоненциального множителя, несколько завышенное по сравнению с более точным теоретическим рассмотрением.
При фазовых превращениях в конденсированных фазах зародыш контактирует с большим числом молекул исходной метастабильной фазы. Время жизни критического зародыша определяется в этом случае числом молекул на его поверхности SJb2 СЪ— межмолекулярное расстояние), частотой их колебаний vM и энергетическим барьером «пристраивания» новой молекулы к поверхности зародыша U. Частота тепловых колебаний молекул может быть приближенно оценена из соотношения vM = k 7/h, где h — постоянная Планка. Это позволяет записать предэкспоненциальный множитель Уо в виде.
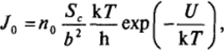
при (/ = 0 оценка У0 дает значение ~1045 м" 3 • с'1.
Энергетический барьер U «пристраивания молекул» к поверхности зародыша имеет важное значение при затвердевании силикатных расплавов и органических жидкостей, особенно высокомолекулярных веществ. В этом случае Vсоответствует по смыслу энергии активации диффузии молекулы или ее отдельных сегментов из объема жидкой фазы к поверхности зародыша. Резкое уменьшение скорости диффузии, связанное с ростом вязкости подобных жидкостей при понижении температуры, приводит к тому, что зависимость частоты возникновения зародышей новой фазы от температуры имеет максимум при некотором переохлаждении А7* (рис. VI-27). При быстром охлаждении таких жидкостей до температур, значительно меньше температуры TfUI — Д71*, скорость образования кристаллических зародышей оказывается очень малой, а вязкость очень большой, и жидкость переходит в аморфное стеклообразное состояние. Скорости возникновения и роста зародышей в стеклах при низких температурах настолько малы, что метастабильное аморфное состояние может сохраняться достаточно долго. Так, обычные силикатные стекла обнаруживают заметную кристаллизацию («расстекловывание») лишь после сотен лет хранения. Существуют методы искусственного ускорения такой кристаллизации силикатных стекол с помощью введения определенных затравок (например, диоксида титана) и соответствующей термообработки стекла. Получающиеся при этом материалы, называемые ситаллами, сохраняя высокую прочность при обычных температурах, обнаруживают существенно более высокую жаропрочность. Они не столь хрупки, как простые стекла, и менее подвержены влиянию на прочность поверхностных дефектов и активной среды. Разработаны методы аморфизации и некоторых металлических сплавов. Такие «аморфные металлы», получающиеся при быстром охлаждении, обладают некоторыми необычными ценными свойствами.
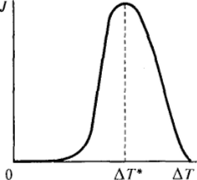
Рнс. VI-27. Зависимость частоты возникновения J зародышей новой фазы от переохлаждения Д Т