Калибровка прибора в режиме измерения концентрации

После применения нормирующего коэффициента зависимость нормированной проводимости и концентрации имеет вид, показанный на рис. 3.18. Далее приступают к определению коэффициентов, связывающих измеренное значение УЭП с концентрацией серной кислоты при каждой из температур в виде. Нормирующий коэффициент п определяется как минимальный относительный температурный коэффициент УЭП анализируемого… Читать ещё >
Калибровка прибора в режиме измерения концентрации (реферат, курсовая, диплом, контрольная)
При калибровке кондуктометра для работы в режиме определения концентраций необходимо учитывать сложный характер зависимости УЭП анализируемого раствора от его концентрации и температуры. Зависимость УЭП от концентрации может быть не только нелинейной, но и неоднозначной. На рис. 3.16 показаны зависимости УЭП от концентрации анализируемого раствора для хлористого натрия (NaCl), серной (H2SO4) и соляной (НС1) кислот. Зависимость УЭП от концентрации для всех трёх приведённых веществ нелинейна, а для серной кислоты и неоднозначна. На участках, где зависимость УЭП от концентрации неоднозначна (имеет экстремумы в точках 3, 5 и 6), использование кондуктометров, если не имеется дополнительных датчиков других физико-химических параметров или не проводится предварительная подготовка пробы для анализа (например, разбавление), невозможно. Допустимые рабочие диапазоны: 1−2, 1 — 3, 2 — 3, 3 — 4, 3 — 5, 4 — 5 и 5 — 6. Недопустимы диапазоны, содержащие внутри точки 3, 5, 6, например, 2−4 или 4−6.
Применяют два способа определения концентрации анализируемого раствора по результатам измерения его УЭП и температуры. Их используют для определения зависимости, связывающей определяемую концентрацию, УЭП и температуру анализируемого раствора. В первом случае концентрацию находят как результат расчёта концентрации по экспериментально определённой зависимости вида.
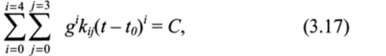
где С — определяемая концентрация, % или г/л; g = * - n (f —10); t — температура анализируемого раствора; U, — температура нормирования; п — нормирующий коэффициент; Аг, у — постоянные коэффициенты.

Рис. 3.16. Зависимость УЭП от концентрации водных растворов.
Получение калибровочных коэффициентов можно пояснить на примере их определения для анализа раствора серной кислоты в диапазоне от 92 до 97%, который является самым трудным для реализации кондуктометрического анализатора. На рис. 3.17 показаны зависимости УЭП растворов серной кислоты, концентрация которых находится в этих пределах, а температура — от 20 до 70 °C.
Нормирующий коэффициент п определяется как минимальный относительный температурный коэффициент УЭП анализируемого раствора. Его применение необходимо, когда зависимость УЭП анализируемого раствора от температуры существенно больше, чем от его концентрации.
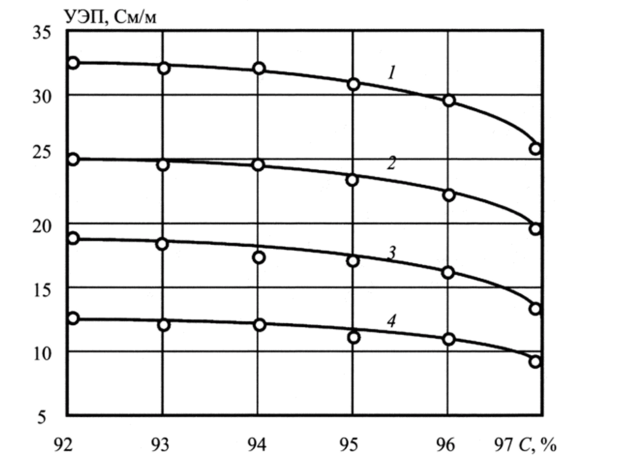
Рис. 3.17. Зависимость УЭП от концентрации серной кислоты и температуры анализируемого раствора:
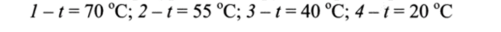
После применения нормирующего коэффициента зависимость нормированной проводимости и концентрации имеет вид, показанный на рис. 3.18. Далее приступают к определению коэффициентов, связывающих измеренное значение УЭП с концентрацией серной кислоты при каждой из температур в виде.
полинома второго порядка С g’k,. Коэффициенты к, также.
/=о зависят от температуры анализируемого раствора. Эта зависимость нелинейна. На рис. 3.19 показана зависимость к" от температуры анализируемого раствора.
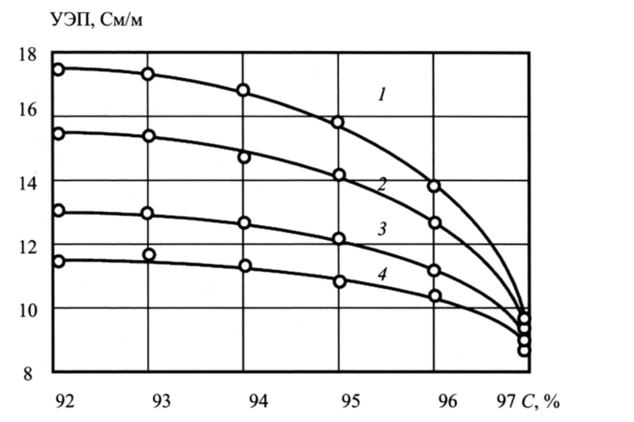
Рис. 3.18. Зависимость скорректированной УЭП от концентрации.
Зависимость коэффициентов, связывающих измеренную УЭП с концентрацией, хорошо описывается полиномом третье;
з го порядка ку =V к,/. Результат расчёта концентрации серной.
/=о кислоты по результатам измерения его УЭП и температуры, т. е. статическая характеристика кондуктометра, показана на рис. 3.20.
Относительная погрешность измерения концентрации серной кислоты кондуктометром не превысила ±0,5%.
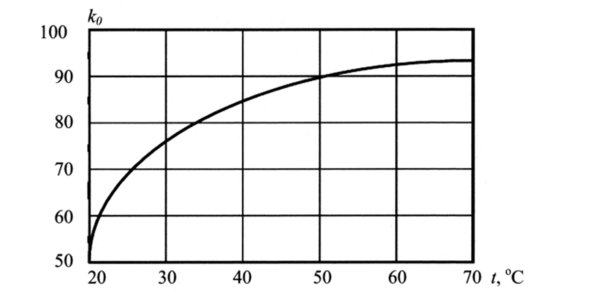
Рис. 3.19. Зависимость коэффициента кп от температуры.

Рис. 3.20. Статическая характеристика кондуктометра: О — результаты расчёта концентрации при температуре 20 °C;? — результаты расчёта при температуре 70 °C.
Коэффициенты kif для определения концентрации наиболее распространённых веществ приведены в табл. 3.5.
Таблица 3.5.
Коэффициенты ktj для определения концентрации наиболее распространённых веществ.
NaCl 1 — 15% / = 0−40 °С п = 0. | |||||
У. | i | ||||
1,217 113-КГ2 | 9,34 489−10'1 | 7,397−103 | 4,45 445−10‘3 |
| |
— 2.29 977- 1(Н. | — 1,79 978−10'2 | —5,2 722* 10″ -*. | — 1,56 134−10"'. | 8,40 074; ю-*1 | |
3,1 238−10-*. | 1,38 185−10^. | 6,53 537−10"**. | 1,6 095 710-6 |
| |
NaOH 1 — 10% /=0−40°С * = 0. | |||||
У. | |||||
— 7,670 851 *10″ '. | 6,75 393−10 '. | 2,67 347 810-2 | 1,9 125−103 | ||
7,96 547−10'2 | — 3,53 000 И О" 2 | 2,578 036-Ю'*. | — 9,249 375-Ю'5 | ||
— 2,247 651 -10″ 3 | 1,632−10*. | 8,192 269−10 *. | 2,78 176 610"**. | ||
2,410 602−10″ 5 | — 1,2 344 510 *. | 8,644 196−10″ 7 | — 2,842 897−1 O'*. | ||
H2S04 1 — 10% / = 0−10% / = 0−40°С /? = 0. | |||||
У. | i. | ||||
7,80 688−10 *. | 3,333-Ю''. | — 2,3 785−1 (Г1 | 9,3 310 510 *. | ||
— 1.97 769 10^*. | — 5,56 196−10 ! | 7,56 467−10'5 | — 4,43 223-Ю" *. | ||
1,13 717−10'5 | 6,8 201−10'5 | — 1,18 349-Ю" 6 | 6,51 971;10*. | ||
H2S< | Э4 92−96% /=20−40 °С /1 = 0,2775. | ||||
У. | i | ||||
1,82 677−103 | — 3,85 035-Ю2 | 2,85 872−10'. | — 7,8 653*10 1 | ||
— 109 078−103 | 2,55 447−10'. | — 1,99 109. | 5,16 652-Ю-2 | ||
1,13 737−10'. | — 256 783. | 1,93 307−10-'. | — 4,85 185−10-3 | ||
— 1,8 452. | 2,3 850 710-'. | — 1,74 605 10‘2 | 4,25 528−10"*. | ||
H2S04 92−96% / = 40 — 70 °C /1 = 0,3 433 333. | |||||
У. | i | ||||
7,41 041 -102 | — 8,53 358 10'. | 3,78 240. | — 5,62 448−102 | ||
— 3.37 964 10'. | 4,71 530. | — 2.19 218−10-'. | 3.39 791 103 | ||
1,6 681. | — 1.45 669 10″ '. | 6,65 352-Ю'*. | 1,1 578−10"*. | ||
Продолжение табл. 3.5.
H2S04 95−99% / = 40−70 °С п = 0. | |||||
j | |||||
1,1 696−102 | — 5,18 833−10″ '. | 3,60 447−10″ 2 | — 1,1468 10‘3 | ||
— 8,2 397−10″ 3 | 1.8 607−10″ 2 | — 1,48 138 Ю" 3 | 7,28 758 10″ 5 | ||
—7,15 577−10"*. | — 1,521−10″ 5 | 2,5814−10″ 5 | — 2,2 574−10″ *. | ||
S03 15 — 28% / = 40 — 70 °C п = 8,946 667−10‘2 | |||||
j | |||||
— 4,65 377-I02 | 3,80 363−102 | — 1,8 022−102 | 1,3449−101 |
| |
— 1,8 859 710'. | 1,27 623−10'. | — 3,16 671. | 3,38 661−10″ '. |
| |
2,15 659. | — 1,62 107. | 4.51 393−10″ '. | — 5,51 103−10″ 2 |
| |
НС1 30−40% / = 20−50°С п = 0. | |||||
j | |||||
— 3.38 931−10*. | 2,5742−10'. | — 5,37 156−10″ '. | 3,43 204−10″ 3 | ||
— 2.84 865 10-'. | — 3.34 331 10-'. | 1,20 791 — О" 2 | — 9,96 654−10 ^. | ||
4,29 599−10″ ^. | 1,82 504−10 ^. | — 8,92 977−10″ 5 | 8,51 592−10″ 7 | ||
Иногда применяют и другой способ определения концентрации, обратный предыдущему. Он основан на использовании зависимости УЭП от концентрации и температуры анализируе;
4 4.
мого раствора в виде / = II c’cijjit — t0). Концентрацию рас;
1=0 у=о твора определяют по параметру с, который изменяется до тех пор, пока рассчитанное по этой зависимости значение УЭП при измеренной температуре не совпадёт с измеренной УЭП. Полученное при выполнении этого условия значение с принимают за концентрацию анализируемого компонента в растворе. В некоторых случаях такой способ даёт лучшие результаты, чем предыдущий. Можно объяснить это тем, что УЭП анализируемого раствора зависит от его концентрации, а не наоборот.
Калибровка кондуктометра для работы в режиме анализатора концентрации бинарного раствора состоит в занесении в память микроконтроллера коэффициентов, связывающих УЭП, температуру и концентрацию анализируемой жидкости.