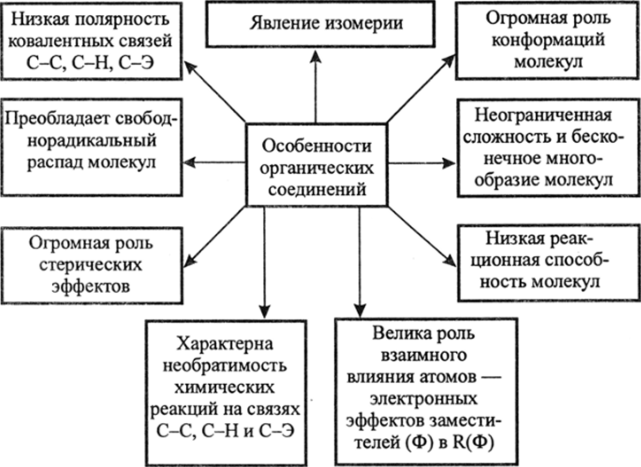
Особенности органических соединений

Которые протекают практически мгновенно (107—Ю10 с" 1). В отличие от них органические реакции на связях С-С, С-Н и С-К идут при обычных условиях очень медленно или вовсе не идут даже с такими активными реагентами, как CI2, H2S04, КМп04, NaOH и т. д. Это обусловлено необходимостью разрыва ковалентных связей, высокими энергиями активации и отсутствием ускоряющего действия растворителя за счет… Читать ещё >
Особенности органических соединений (реферат, курсовая, диплом, контрольная)
Органические соединения, а точнее углеводороды, имеют принципиальные отличия в сравнении с неорганическими соединениями такими, как кислоты и основания, оксиды и соли и даже по сравнению с неорганическими гидридами — Н20, NH3, SiH*, HF, H2S, AsH3 и др. Эти принципиальные особенности органических молекул (как правило, гидридов углерода и углеводородных остатков функциональных производных углеводородов) суммированы на схеме В.2, из которой следует:
1. Неограниченная сложность строения и многообразие молекул органических соединений. Достаточно назвать природные биополимеры — белки, полисахариды, синтетические полимеры — капрон, лавсан, полиэтилен и т. д., витамины, гормоны и особенно нуклеиновые кислоты, молекулярная масса которых доходит до 4* 109. Эта особенность органических соединений обусловлена способностью атома углерода образовывать бесконечно длинные цепи.
I.
(—С—), Друг с другом и с многими другими атомами (О, N, S, Р и др.).
I.
Такое свойство атома углерода называется катенацией (сцеплением).
I I I.
Атомы углерода могут образовывать как цепи …—С—С—С—… или.
I I I.
- 111 V г/
- —С—С—С— > так и циклы от минимального циклопропанового /С—С
'_А_| V
I.
С.
/ /.
до бесконечно больших так называемых макроциклов /С—(С)яЧч. При этом в цепях или циклах отдельные атомы углерода могут быть заменены на.
гстероатомы (О, S, N, Р и т. д.). Это создает бесконечное многообразие органических молекул, на основе которых и возникла жизнь, как важнейшее явление природы.
2. Органическим соединениям присуще явление изомерии и наличие у соединений определенного состава двух или большего числа изомеров. Изомеры — это химические соединения, имеющие одинаковый атомный и изотопный состав, т. е. одну аналитическую формулу, одну и ту же молекулярную массу, но отличающиеся друг от друга структурной формулой и свойствами.
Так, соединение с аналитической формулой СзН^О имеет 9 изомеров, из них 7 стабильных:
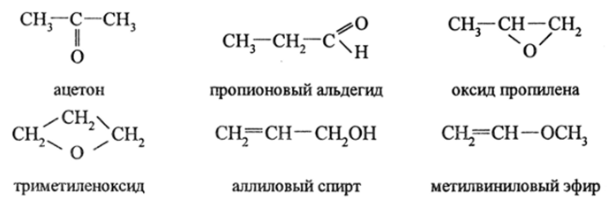
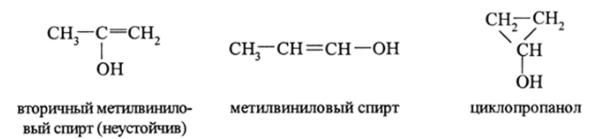
Эти изомеры относятся к различным классам соединений и сильно различаются по свойствам. Причины изомерии могут быть разные и типы изомеров тоже разные. В приведенном примере изомерия молекул обусловлена изменением положения атома кислорода в углеродной цепи. Такая изомерия называется изомерией положения. Возможна также скелетная изомерия, цистрапс-изомерия, оптическая изомерия и др.
Впервые явление изомерии, открытое шведским химиком Й. Берцелиусом в начале XIX в., объяснил крупнейший русский химик А. М. Бутлеров — создатель классической теории строения органических соединений и автор структурных химических формул.
Теория химического строения Бутлерова (1861) явилась фундаментом, на котором строилась теоретическая органическая химия. Основные ее положения необходимы для изучения химии и в современной формулировке сводятся к следующему:
а) Молекула любого вещества имеет единственно возможную последовательность расположения атомов, которая на плоскости изображается формулой строения (см. изомеры С3Н60), или структурной формулой (рис. В.1).
Классическая структурная формула изображает молекулу на плоскости и ничего не говорит о пространственном строении молекулы, т. е. о стереохимической формуле. Так, структурная формула метана по Бутлерову (рис. В.1, а) и стерсохимическая формула по Вант-Гоффу (рис. В.1, б) существенно отличаются.
б) Любое изменение последовательности связей атомов приводит к изменению физико-химических свойств вещества, т. е. приводит к изомерии. Подтверждение этому дают изомеры С3Н60.

Рис. В.1. Структура метана по Бутлерову (а) и по Вант-Гоффу (б)
в) Атомы в молекуле находятся в состоянии химического взаимодействия и оказывают взаимное влияние друг на друга независимо от того, находятся ли они по соседству друг с другом (в контакте) или же разделены другими атомами. Поэтому одни и те же атомы (атом кислорода у изомеров С3Н60) будут иметь различные свойства в зависимости от местоположения в молекуле. Так, в СН. СН—СН, кислород легко взаимодействует с Н20:
V
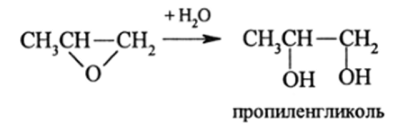
тогда как в других изомерах С3Н60 он инертен к Н20.
г) Строение вещества может быть установлено по его химическим и физическим свойствам. И, наоборот, по формуле строения можно судить о свойствах вещества. Поэтому установление правильной формулы строения имеет решающее значение для познания природы вещества.
Главной задачей современного химика является умение на основании структурной формулы предсказать пространственное строение и химические свойства вещества.
3. Ковалентность и низкая полярность главных химических связей С-С, С-Н и С-К, где К — контактный атом функциональной группы, который непосредственно контактирует с атомом углерода. Так, в спиртахС-ОН, аминахС-NH2, сульфокислотахC-S020H химическая связь углерода с контактными атомами О, N, S ковалентна и слабо полярна.
Числовые значения электрических моментов диполей связей в органических соединениях очень малы. Несколько выше электрический момент диполя и полярность связей С—Галоген.
Низкая полярность химических связей С-С, С-Н и С-Э приводит к коренным отличиям органических и неорганических соединений, т. е. характера их диссоциации в растворе и в газовой фазе, а также реакционной способности. Как известно, ионные и сильнополярные неорганические соединения, такие как кислоты, основания, соли, в водных растворах диссоциируют на ионы, т. е. подвергаются гетеролитической (ионной) диссоциации:
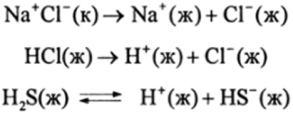
Сильные электролиты распадаются сполна и необратимо, а слабые частично и обратимо. В отличие от них органические соединения по связям С-С, С-Н и С-К в растворах практически не диссоциируют. Гетеролитическая диссоциация по этим связям имеет место только в очень жестких условиях и в небольшой степени. В газовой фазе для органических соединений при действии электромагнитного или термического поля наблюдается гемолитический (свободнорадикальный) распад. Например:
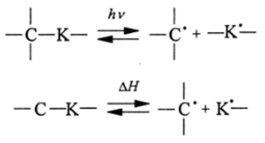
В редких случаях такой распад происходит и в растворе. Так, в бензольном растворе гексафенилэтан образует желтые трифенилметилрадикалы:
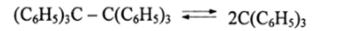
(степень диссоциации, а = 2—9% в бензоле) Функциональные группы органических соединений диссоциируют по ионному (гетеролитическому) типу подобно неорганическим молекулам, от которых они произошли:
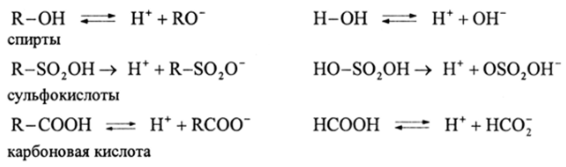
Из этих примеров следует вывод о принципиальном различии двух составных частей сложных органических соединений — углеводородной части ® и функциональных групп (Ф) в молекулах Я (Ф), где Ф = -ОН, -S020H, — СООН и т. д.
4. Из ковалентности связей С-С, С-Н и С-Э и низкой склонности их к диссоциации вытекает низкая реакционная способность органических соединений в отличие от неорганических. Большинство неорганических реакций являются ионными или нон-молекулярными, как, например, реакции осаждения, нейтрализации и комплексообразования: 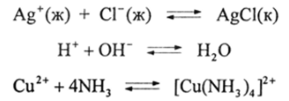
которые протекают практически мгновенно (107—Ю10 с" 1). В отличие от них органические реакции на связях С-С, С-Н и С-К идут при обычных условиях очень медленно или вовсе не идут даже с такими активными реагентами, как CI2, H2S04, КМп04, NaOH и т. д. Это обусловлено необходимостью разрыва ковалентных связей, высокими энергиями активации и отсутствием ускоряющего действия растворителя за счет сольватации в большинстве реакций органических соединений.
Реакционная способность вещества определяется скоростью химической реакции при стандартных условиях (298 К, 1 моль/л).
Если реакция бимолекулярная.
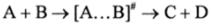
dCA. ->go.
то скорость реакции x> = —— = kv cAcQ в стандартных условиях характеризуем ется константой скорости к™ .
Чем она выше, тем больше реакционная способность. Для органических реакций к™ в тысячи раз меньше, чем для неорганических. Реакционная способность сильно зависит от температуры и эта зависимость определяется энергией активации Е или энтальпией активации A//*. При этом.
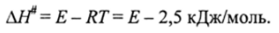
Растворитель оказывает сильное влияние на реакционную способность, так как влияет на сольватацию реагентов, А и В и переходного состояния [А…В]*, которое проявляется в энтропиях активации AS*.
Большинство органических реакций в отличие от неорганических является необратимыми. Следовательно, закон действующих масс к ним неприменим, и они, естественно, не имеют таких характеристик, как константы равновесия.
Количественными характеристиками необратимых органических реакций являются константа скорости, энтальпия и энтропия активации. Органическая химия поэтому строится преимущественно на теориях химической кинетики и меньше на теориях химической термодинамики.
5. Современная органическая химия является химией конформационной, в которой определяющую роль имеют вращательные состояния молекулы (т. е. конформации). Она является также химией электронных и пространственных эффектов. Эти особенности органических молекул будут рассмотрены позднее.