Работа 17.6.5. Определение гидрокарбонатной щелочности воды

Ход определения. 1. Определение pH анализируемой воды. Пользуясь универсальным индикатором, определяют pH воды. Если pH находится в пределах 5,0—8,0, то щелочность воды практически равна концентрации гидрокарбонат-ионов. Титрование. Приступая к титрованию, проверяют уровень раствора кислоты в бюретке. Он должен быть на нулевой отметке по нижнему мениску. Кроме того, в носике бюретки не должно… Читать ещё >
Работа 17.6.5. Определение гидрокарбонатной щелочности воды (реферат, курсовая, диплом, контрольная)
Одним из важнейших показателей качества воды является щелочность (символ — Щ, единица — ммоль/л). Общая щелочность определяется суммой анионов слабых кислот, способных реагировать с хлороводородной или серной кислотой. Общая щелочность включает в основном гидрокарбонатную и карбонатную. Если величина pH не превышает 8,4, то щелочность определяется концентрацией гидрокарбонат-ионов. При более высоких значениях pH (от 8,4 до 12) гидрокарбонатная щелочность постепенно уменьшается при одновременном увеличении карбонатной щелочности. При pH > 12 гидрокарбонатная щелочность равна нулю.
При значениях pH < 4,5 в воде присутствует только свободная углекислота (С02). В различных водах pH обычно находится в пределах 6,5— 8,5; в атмосферных осадках — 4,6—6,1; в морских водах — 7,9—8,3. Норматив водородного показателя питьевой воды — 6,0—9,0. Следовательно, наиболее часто щелочность воды определяется присутствием гидрокарбонат-ионов. Кроме того, гидрокарбонаты кальция и магния обусловливают карбонатную жесткость воды Жк. Она почти полностью устраняется кипячением, при котором гидрокарбонаты разлагаются:
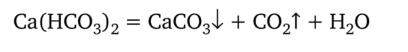
Предельно допустимая концентрация (ПДК) гидрокарбонат-ионов в питьевой воде составляет 60 мг/дм3.
Содержание гидрокарбонат-ионов определяют титрованием воды раствором НС1 с метиловым оранжевым. Химизм процесса выражается уравнениями.
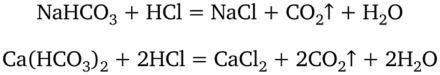
Ионно-молекулярное уравнение:
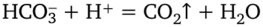
Реактивы и оборудование: титрант — раствор НС1; индикатор — метиловый оранжевый и универсальный индикатор; анализируемая вода (0,5 л); мерная пипетка на 100 мл для взятия объема анализируемой воды; штатив с бюреткой (для НС1); коническая колба для титрования; стакан для слива.
Ход определения. 1. Определение pH анализируемой воды. Пользуясь универсальным индикатором, определяют pH воды. Если pH находится в пределах 5,0—8,0, то щелочность воды практически равна концентрации гидрокарбонат-ионов.
- 2. Подготовка бюретки к работе (см. работу 17.6.1).
- 3. Подготовка анализируемой воды к титрованию. Чистой мерной пипеткой вместимостью 100 мл переносят 100 мл анализируемой воды в коническую колбу. Прибавляют 2—3 капли метилового оранжевого, раствор окрасится в желтый цвет.
- 4. Приготовление раствора-«свидетеля» (см. работу 17.6.1).
- 5. Титрование. Приступая к титрованию, проверяют уровень раствора кислоты в бюретке. Он должен быть на нулевой отметке по нижнему мениску. Кроме того, в носике бюретки не должно быть воздуха.
Титруют воду раствором НС1 до перехода желтой окраски индикатора в бледно-розовую. Повторяют титрование 2—3 раза и заносят результаты титрования в таблицу.
Пример
Данные титрования воды хлороводородной кислотой.
№ п/п. | У (Н20), мл. | V (HC1), мл. | сэк(НС1), моль/л. | Щ (НСОз)' ммоль/л. |
12,20. | 0,1016. | |||
12,30. | ||||
Уср = 12,25. |
Чтобы вычислить гидрокарбонатную щелочность (по ГОСТу), находят молярную концентрацию эквивалентов гидрокарбонат-ионов и умножают ее на 1000:
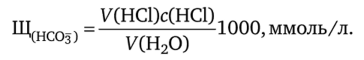
Пример.
На титрование 100,0 мл воды пошло в среднем 12,25 мл 0,1016 н. раствора кислоты. Тогда 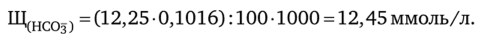
Зная концентрацию гидрокарбонат-ионов в воде, можно вычислить массу их в 1 л воды:
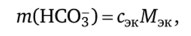
где сэк = Щ • IQ-3 = 12,45 • 0,001 = 0,1 245 моль/л; Мэк(НСОз) = 61 г/моль. 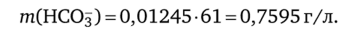
В агрохимическом анализе часто используют ацидиметрическое титрование для определения содержания гидрокарбонатионов в воде и почвенных вытяжках.