Общая характеристика флавоноидов и их значение

Одним из ценных свойств флавоноидов является их положительное влияние на функцию печени: они усиливают желчеотделение, улучшают ее детоксицирующую способность по отношению к таким веществам, как барбитураты, мышьяк. Детоксикации организма способствует свойство флавоноидов оказывать мочегонное влияние. Некоторые флавоноиды из семейства норичниковых благоприятно влияют на пищеварение, понижают… Читать ещё >
Общая характеристика флавоноидов и их значение (реферат, курсовая, диплом, контрольная)
Флавоноидами называется группа фенольных соединений с двумя ароматическими кольцами, объединенных общим структурным составом С6-С3-С6. Первое бензольное кольцо, конденсированное в большинстве классов с кислородосодержащим гетероциклом С или непосредственно прилежащее к карбонильной группе пропанового фрагмента, как в халконах, обозначают буквой А, а боковой фенильный заместитель — буквой В латинского алфавита. Исходя из такого обозначения, порядок нумерации в гетероциклических флавоноидах начинается с гетероатома с переходом на кольцо А, а в кольце В порядок нумерации автономный и начинается с углерода, связанного с остальной частью молекулы.
Большинство флавоноидов можно рассматривать как производные хромона (бензо-г-пирон) [Лебедев, С. И. Физиология растений / С. И. Лебедев. — М.: Колос, 2008. — 544 с.].
Под термином флавоноиды (от лат. flavus — желтый, так как первые выделенные из растений флавоноиды имели желтую окраску, позднее установлено, что многие из них бесцветны) объединены различные соединения, генетически связанные друг с другом, но обладающие различным фармакологическим действием [Беликов, П. С. Физиология растений: Учебное пособие. / П. С. Беликов, Г. А. Дмитриева. — М.: Изд-во РУДН, 2002. — 248 с.].
Изучение флавоноидов относится к началу XIX в., когда в 1814 г. Шевроле выделил из коры особого вида дуба кристаллическое вещество, названное кверцетрином. Спустя 40 лет Риганд установил гликозидный характер этого вещества и агликон назвал кверцетином. В 1842 г. Вайс сообщил о выделении рутина из Ruta graveolens. Впервые в 1864 г. в индивидуальном виде был получен хризин из тополя; строение его было подтверждено в 1898 г. Косанецким путем синтеза метилового эфира хорацетофенона с этиловым эфиром бензойной кислоты. В 1903 г. Валяшко установил строение рутина. Систематическое изучение строения природных флавоноидов многие годы проводили польские химики. Большую работу по изучению антоцианов провел Вильштеттер. Исследованиями катехинов занимались А. Л. Курсанов, М. Н. Запраметов, К. Фрейденберг и др. Интерес к флавоноидным соединениям особенно возрос в 40-е годы нашего столетия: флавоноиды привлекают внимание ученых разносторонней биологической активностью и чрезвычайно низкой токсичностью. После 1970 г. выделено свыше 1400 соединений, относящихся к флавоноидам. Перспективным направлением является поиск биологически активных соединений группы ксантонов — близких по строению к флавоноидам [Кретович, В. Л. Биохимия растений /В.Л. Кретович. — М.: Высшая школа, 2000. — 445 с.].
В зависимости от степени окисления и гидроксилирования пропанового скелета С6-С3-С6, положения фенильного радикала и величины гетероцикла флавоноиды делятся на несколько групп:
I. Собственно флавоноиды (эуфлавоноиды) с боковым фенильным радикалом у С2.
II. Изофлавоноиды с фенильным радикалом у С3.
III. Неофлавоноиды с фенильным радикалом у С4.
IV. Бифлавоноиды.
В растениях флавоноидные соединения, кроме катехинов и лейкоантоцианов, сравнительно редко встречаются в свободном состоянии. Подавляющее большинство их представлено в виде разнообразных гликозидов. Многообразие флавоноидных гликозидов обусловлено значительным набором сахаров и возможностями присоединения их в ряде положений, а также тем, что сахара могут иметь различную величину окисных циклов, конфигурацию гликозидных связей порядок сочетаний между ними. Причём такие сложные смеси часто встречаются в одном и том же растительном материале.
В качестве углеводной части могут быть моно-, дии трисахариды. Моносахаридами являются обычные для растений сахара: D-глюкоза, D-галактоза, D-ксилоза, L-рамноза и др. В некоторых случаях встречаются специфические дисахариды: рутиноза (рамноза и глюкоза), софороза (2 молекулы глюкозы).
Сахара могут присоединяться к агликону в 3, 7, 3', 4' и др. положениях. Для флавоноидов характерно гидроксилирование. Оно возможно почти во всех положениях. У некоторых флавоноидов гидроксилы метилированы.
Основную группу флавоноидов составляют О-гликозиды, в которых сахара cвязаны с агликоном полуацетальной связью через атом кислорода. О-гликозиды в зависимости от количества сахаров, положения и порядка присоединения делятся на моногликозиды, биозиды, дигликозиды и смешанные гликозиды.
Вторую группу составляют С-гликозиды или гликофлавоноиды, которые можно подразделить на С-моногликозиды, С-дигликозиды, С-О-дигликозиды, С-О-биозиды. В гликофлавоноидах углеводные заместители связаны с агликоном через углеродный атом в 6 или 8-м положении.
К третьей группе флавоноидных гликозидов относятся так называемые комплексные соединения. Они представляют собой ацилированные гликозиды различных групп и в зависимости от положения ацильного заместителя делятся на гликозиды депсиноидного типа и гликозиды со сложноэфирной связью в сахарных заместителях. Из кислот, выделенных из комплексных гликозидов, идентифицированы бензойная, n-оксибензойная, кофейная, уксусная, пропионовая, n-оксикоричная и другие кислоты [Кретович, В. Л. Биохимия растений /В.Л. Кретович. — М.: Высшая школа, 2000. — 445 с.].
К флавоноидам относятся производные халкона, катехины, антоцианидины, ауроны. Катехины относятся к полифенолам, входят в состав конденсированных дубильных веществ. Катехины представляют собой наиболее восстановленные флавоноидные соединения. Многие красные и синие окраски цветков с различными оттенками обусловлены присутствием антоцианидинов. В зависимости от рН среды окраска цветков меняется. В кислотной среде они образуют розовую, красную окраску, в щелочной среде — от голубой до синей с разными оттенками. Ауроны имеют разнообразную структуру. Они встречаются в растениях семейства астровых. В растениях присутствуют в форме гликозидов [Физиология растений: Учебник для студентов вузов. / Н. Д. Алехина, Ю. В. Балнокин, В. Ф. Гавриленко и др.; Под ред. И. П. Ермакова. — М.: Издательский центр «Академия», 2005. — 640 с.].
В растениях флавоноиды локализуются в различных органах, но чаще в надземных: цветках, обуславливая окраску лепестков (бессмертник песчаный, василек синий, пижма обыкновенная); в траве (фиалка, чистец, рута, горец), плодах (боярышник, софора японская); значительно меньше их в стеблях и подземных органах (солодка, шлемник байкальский, стальник полевой). Наиболее богаты ими молодые цветки, незрелые плоды. Локализуются в клеточном соке в растворенном виде. Содержание флавоноидов в растениях различно: в среднем 0,5−5%, иногда достигает 30% (в цветках софоры японской).
В клетках растений флавоноиды накапливаются в форме гликозидов, главным образом в вакуолях, а в свободном состоянии — в специальных образованиях, зачастую имеющих довольно сложное строение — смоляных и эфирномасличных ходах, канальцах, вместилищах, железках и т. д. В надземных частях растений более 85% суммы флавоноидов локализуется в клетках эпидермы и только 15% - в остальных тканях [Третьяков, Н. Н. Физиология и биохимия сельскохозяйственных растений. / Н. Н. Третьяков, Е. И. Кошкин, Н. М. Макрушин и др.; Под ред. Н. Н. Третьякова. — М.: Колос, 2000. — 640 с.].
В лепестках цветков обычно находятся антоцианы, обуславливая окраску большинства алых, красных, розово-лиловых и синих цветков. В окраске желтых цветов принимают участие флавоноловые гликозиды, ауроны, и халконы, хотя наиболее важным источником этого цвета являются каротиноиды. Поскольку антоцианиды и флавонолы особенно близко связаны структурно и биогенетически, то они часто присутствуют вместе в одинаковых гликозидных структурах. С антоцианами совместно могут находиться также гликозиды флавонов, флавононов, ауронов и халконов. Очевидно, в зависимости от сочетаний этих соединений лепестки цветков приобретают разные оттенки. Гликолизирование флавоноидных пигментов цветков имеет существенное значение. С одной стороны, это состояние обеспечивает их устойчивость к свету и к действию ферментов, с другой — в форме гликозидов улучшается растворимость пигментов в клеточном соке.
В большинстве плодов основной их окраски являются также антоцианы. Широко распространены и флавоноловые гликозиды. В листьях главными являются флавоноловые гликозиды, а антоцианов в них сравнительно мало. В семенах флавоноиды могут находиться как в свободном, так и в связанном состоянии. Например, это может относиться к флавонолу кверцетину. Функция флавоноидов в семенах неясна. Высказано предположение, что они могут быть ингибиторами прорастания [Медведев, С. С. Физиология растений: Учебник. / С. С. Медведев. — СПб.: Изд-во Санкт-Петерб. ун-та, 2004. — 336 с.].
Биологическая роль флавоноидов в жизни растений изучена еще недостаточно.
Некоторые авторы считают, что флавоноиды принимают участие:
- * в окислительно-восстановительных процессах растений;
- * в выработке иммунитета;
- * в защите растений от неблагоприятных воздействий ультрафиолетовых лучей и низких температур. Предполагается, что благодаря способности поглощать ультрафиолетовое излучение (330−350 нм) и часть видимых лучей (520−560 нм) флавоноиды защищают растительные ткани от избыточной радиации. Это подтверждается локализацией флавоноидов в эпидермальных (близких к поверхности) клетках растений.
- * в процессе оплодотворения высших растений;
- * обуславливают огромное разнообразие окрасок цветков и плодов, что привлекает насекомых и тем самым способствуют опылению;
- * некоторые флавоноиды защищают аскорбиновую кислоту от окисления (т.е. являются антиоксидантами).
Входя в состав экстрактивных веществ древесины, флавоноиды способны придавать ей особую прочность и устойчивость к поражениям патогенными грибами [Уоринг Ф., Филлипс И. ''Рост растений и дифференцировка'', Москва, Мир, 1984 г.].
Неспецифическая антиоксидантная роль флавоноидов:
При большинстве стрессов в клетке в избытке образуются активные формы кислорода (супероксид-анион, синглетный кислород, гидроперoксильный радикал и т. д.). Выступая в качестве повреждающих факторов, они приводят к образованию различных перекисных соединений, например, липидов. Обладая способностью к обратимому окислению, флавоноиды являются эффективными природными антиоксидантами, способными прерывать каскад реакций перекисного окисления липидов и, тем самым, предотвращать последствия окислительного стресса для клеток. Хорошо изучено такое действие флавоноидов на организмы животных и человека [6, 12, 17]. Аналогичной предполагается защитная антиоксидантная роль флавоноидов при стрессе и у растительных организмов.
Считается, что антиоксидантная активность флавоноидов может реализовываться через 3 основных механизма [12]:
1) Ингибирование активных форм кислорода (АФК) — радикал ингибирующая функция. Флавоноиды являются идеальными ловушками АФК, сами становясь при этом радикалами, но гораздо менее агрессивными и более устойчивыми. Основными структурными элементами, сообщающие молекулам этих веществ антирадикальные свойства являются следующие группировки (рис. 1):
Рис 1. Структурные элементы молекул флавоноидов, обеспечивающие антирадикальную активность
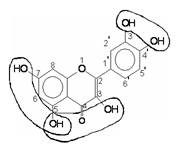
Примечания: 1- 5, 7 — дигидроксизамещение кольца А; 2- 3', 4'- дигидроксизамещение кольца В; 3 — сочетание 5-ОН-группы в кольце А, 3-ОН группы и 4-оксогруппы с наличием в кольце С двойной связи.
Антирадикальную активность флавоноидов принято оценивать в единицах TEAC (тролокс-эквивалентах, trolox equivalent antioxidant capacity, мМ, миллимоль), то есть в условных единицах концентрации, получаемых при сравнении антиоксидантной активности исследуемых веществ с активностью синтетического антиоксиданта тролокса, используемого в качестве стандарта [12].
Из всех флавонов и флаванонов всеми вышеуказанными структурными элементами обладает кверцетин, и его антиоксидантная активность в ТЕАС составляет 4,70 мМ, что для флавоноидов является одним из самых высоких показателей. Однако, представители другого класса флавоноидов — флаван-3-олов могут иметь более высокие значения антирадикальной активности. Это в частности, может происходить с теафлавинами (флаван-3-олами, накапливаемыми в черном чае). Эти вещества могут образовывать эфирные связи с галловой кислотой — С6-С1 фенольным соединением, у которого к бензольному кольцу присоединены 3 ОНгруппы, очевидно способствующие его антирадикальной активности. Установлено, что по мере увеличения количества присоединенных остатков антирадикальная активность возрастает, и у теафлавин 3,3'- дигаллата показатель ТЕАС достигает 6,18 мМ.
Таким образом, антирадикальная активность молекул флавоноидов в ходе биосинтеза может меняться, по мере появления или исчезновения соответствующих элементов. Например образование двойной связи С2=С3 при превращении дигидрокверцетина в кверцетин повышает антирадикальную активность с 1,9 до 4,7 мМ ТЕАС, а уменьшение в ходе биосинтеза количества ОН-групп в кольце В у антоцианов приводит с снижению этого показателя. Негативно на антирадикальной активности сказывается также и гликозилирование молекул (кверцетин — 4,7 мМ, гликозид кверцетина рутин — 2,9 мМ ТЕАС), однако для разных классов величина снижения этого показателя различна [12]. Однако следует упомянуть, что на сегодняшний момент отсутствует единая методика определения антиоксидантной активности веществ. Поэтому численные значения показателей антирадикальной активности соединений могут различаться, в зависимости от выбранной методики, хотя в целом зависимость этого показателя от природы вещества сохраняется [18].
2) Ингибирование ферментов, связанных с продуцированием АФК — фермент-ингибирующая функция. Флавоноиды способны ингибировать ферменты, ответственные за синтез супероксид-аниона — протеинкиназу и ксантиноксидазу и др. Наиболее хорошо изучены механизмы взаимдействия флавоноидов с ксантиноксидазой, модибден-содержащего фермента, превращающего гипоксантин в ксантин и ксантинв мочевую кислоту, что сопровождается образованием АФК. Структурные элементы молекул флавоноидов, предположительно способные конкурировать с молекулами ксантина в активном центре ксантиноксидазы, представлены на рисунке 2:
Рис 2. Структурные элементы молекул флавоноидов — ингибиторов ксантиноксидазы
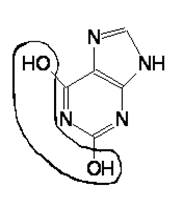
флавонол ксантин.
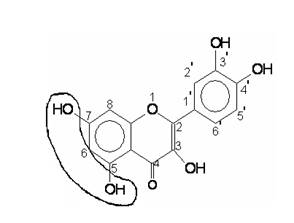
Как следует из рисунка, фермент-ингибирующую функцию молекулам флавоноидов предположительно обеспечивает одна из группировок, обуславливающая и антирадикальную активность этих модекул — гидроксильные группы, присоединенные к кольцу, А в положениях 5 и 3 (см. также рис. 2).
3) связывание в хелатные соединения металлов, включенных в процесс ферментативного продуцирования свободных радикалов — хелатирующая функция. Известно, что ионы металлов (меди, железа, цинка и т. д.) могут инициировать реакции образования активных форм кислорода [19, 20, 21]. Поэтому связывание этих ионов способствует снижению скорости свободнорадикальных процессов.
Сайты молекул флавоноидов, участвующие, согласно современным представлениям [12], в связывании ионов двухвалентных металлов, представлены на рисунке 3.
Рис 3. Возможные сайты хелатирования ионов металлов молекулами флавоноидов
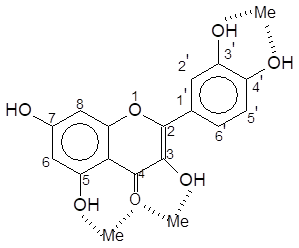
Примечание: Me — Fe2+, Cu2+ и др.
Как следует из представленных данных, в хелатном связывании ионов металлов участвуют группировки молекул флавоноидов, которые отвечают и за их антирадикальную активность.
Подводя итог вышесказанному, можно сделать следующие обобщения:
- 1) Антиоксидантная активность молекул возрастает по мере увеличения количества приосединенных гидроксильных групп.
- 2) Молекулы с двойной связью между 2 и 3 атомами углерода, обладают более высокой антиоксидантной активностью, чем молекулы с одинарной.
- 3) Гликозилированные формы флавоноидов, как правило, менее активные антиоксиданты, чем негликозилированные.
Таким образом, можно ожидать, что по мере усиления стресса в тканях будет возрастать оксидативный стресс, и растение, в свою очередь, будет усиливать биосинтез и накопление антиоксидантов — флавоноидов.
Таким образом, можно ожидать, что по мере усиления стресса в тканях будет возрастать оксидативный стресс, и растение будет усиливать биосинтез и накопление антиоксидантов — флавоноидов. Различными авторами накопление флавоноидов изучалось на следующих видах стрессов:
1) Повышенное содержание тяжелых металлов в растениях. Существуют данные, что воздействие тяжелых металлов может сказываться на накоплении растениями флавоноидов по-разному и запускать различные защитные механизмы [20]. Показано, что влияние повышенных концентраций меди в почве угнетающим образом сказывается на продукции флавоноидов тысячелистником благородным (Achillea nobilis L.) в условиях Башкирского Зауралья [7]. Аналогичная картина обратной зависимости между содержанием меди и флавоноидов в тканях была отмечена и на другом характерном для этого региона растении — можжевельнике казацком (Juniperus sabina L.) [22, 23].
В то же время было показано, что обработка каллуса растительных тканей препаратами кадмия способно вызвать прямо противоположный эффектрост содержания флавоноидов. Это было выявлено на каллусе льнадолгунца (Linum isitatissimum L.) [19] и чая (Camellia sinensis L, Kuntse) [24] и наблюдаемый эффект предположительно был объяснен защитной ролью этих соединений. Обработка растений препаратами цинка, в зависимости от концентрации, может привести как к увеличению, так и к уменьшению содержания в них флавоноидов, что было показано на зверобое продырявленном (Hypericum perforatum L.) [25].
- 2) Техногенное загрязнение. Анализ работ, посвященных изучению влияния различных техногенных воздействий на накопление растениями фенольных соединений, показывает, что в целом, картина достаточно противоречивая. Встречаются работы, в которых описывается рост содержания отдельных веществ или целых классов в ответ на негативное техногенное воздействие [26]. В таких случаях авторы обычно объясняют полученную картину защитной (чаше всего антиоксидантной ролью фенольных веществ). В то же время достаточно часто встречаются работы, в которых описываются прямо противоположные явленияпри техногенном воздействии содержание тех или иных фенольных соединений снизилось. В этом случае авторы объясняют наблюдаемую картину угнетением исследуемых событий вредными экологическими факторами [19, 23, 24, 27, 28].
- 3) Избыточная ветровая нагрузка. Этот вид стресса может также вызывать повышенное накопление флавоноидов, что показано, например, у растений, обитателей Куршской косы в Калининградской области [29].
- 4) Экстремальные значения температур. Возрастание содержания флавоноидов в надземной части при снижении температур было зарегистрировано у озимых сортов пшеницы (Triticum aestivum L.) [30] При повышении температуры до 40 и более градусов аналогичная картина была зарегистрирована для проростков пшеницы и тыквы (Cucurbita pepo L.) [31]. У других культур была зарегистрирована более сложная картина. Например, в корнях проростков гороха (Pisum sativum L.) выращивание при низких положительных температурах не выявило с контролем значимых различий в содержании общей суммы флавоноидов. Однако содержание флаванов на начальных этапах роста было ниже, но впоследствии этот показатель значительно возрос и стал превышать аналогичный показатель контрольных растений на 40% [32] .
- 1) Условия увлажнения. Рядом авторов выявлена роль уровня доступной влаги в накоплении флавоноидов. Так, согласно Поляковой с соавт. [9], изучавших динамику накопления флавоноидов в градиенте увлажнения в разнообразных эколого-ценотических рядах у бобовых растений нескольких видов, накопление флавоноидов было максимальным в условии пойменных лугов, что по данным авторов, соответствует мезофильной предковой экологии вида. Соответственно, предполагается, что любое отклонение условий увлажненности от исходных. соответствующих предковой экологии вида, может вызывать уменьшение содержания флавоноидов.
- 2) Сезонная динамика и фазы онтогенеза. Имеется много работ, в которых описывается сезонная динамика накопления растениями фенольных соединений вообще и флавоноидов в частности. Например, для растений чины приморской (Lathyrus Maritimus L), колосняка песчаного (Leymus arenarius (L.) Hocht), песколюба песчаного (Ammophila arenaria Host) и осоки песчаной (Carex arenaria L.) динамика накопления рутина повышается в начале онтогенеза и в период летнего максимума температур [29]. В то же время для растений рода рододендрон (Rhododendron spp., L) максимум накопления рутина и других флаваноидов зафиксирован при переходе растений к зиме, поздней осенью перед заморозками [33]. Последнее обстоятельство авторы объясняют возможной криопротекторной функцией флавоноидов, обусловленной входящими в состав гликозилированных форм молекулами углеводов. Имеются данные и о других перспективных видах, в частности о сабельнике болотном (Comarum palustre L.), для которого установлена сложная динамика накопления фенольных веществ и распределения их между органами [34].
- 3) Режим освещенности и спектральный состав света. Показано, что характер освещенности и спектральный состав света может значительно сказываться на составе накапливаемых растениями флавоноидов и их производных. Например, на растениях ряски (Spirodela intermedia, клон 115) было установлено, что замена освещения красным, дальним красным и синим светом на освещение белым привела к снижению в растениях содержания витексина, ориентина и цианидин-3 могоглюкозида [35].
В целом установлено, что экспрессия генов ферментов, отвечающих за синтез флавоноидов, индуцируется светом [5]. Однако есть данные, что для накопления растениями флавоноидов важен оптимальный уровень освещенности. Например, у Анектохилуса (Anoectochilus formosanus Wall.), ценного лекарственного растения, было установлено, что наибольшее накопление флавоноидов, а равно как и биомассы, происходит в условиях малой освещенности, оптимальной для этого тенелюбивого вида [36].
- 1) Защита от избыточного ультрафиолетового излучения, в частности, на больших высотах произрастания. На сравнительно больших высотах, порядка 1−1,5 км было показано, что содержание флавоноидов в надземных частях растений может достигать максимума. По мнению авторов, это связано, очевидно с их фотопротекторной функцией. Так, показано что, сумма флаваноидов и дубильных веществ возрастает по мере увеличения высоты над уровнем моря до отметки в 1550 км у растений шалфея мутовчатого (Salvia verticillata L.) [37]. У растений клевера лугового (Trifolium pratense L.) содержание изофлаваноидов в высокогорье выше по значению, чем содержание этих же соединений у растений из предгорных популяций [38]. По мере увеличения высоты над уровнем моря у растений мяты длиннолистной увеличивается сумма флаваноидов в стеблях и уменьшается в листьях и соцветиях, [39]. Аналогичная картина ранее наблюдалась на проростках нескольких популяций березы в модельных опытах по изучению влияния ультрафиолетового излучения на состав накапливаемых флаваноидов. Показано, что воздействие УФ-излучением (280−320 нм) на надземную часть проростков повышало содержание в них флавоноидов, однако полученная картина накопления веществ зависила от дозы излучения и от места расположения популяции [40]. В ходе лабораторные опыты по изучению влияния УФ-излучения на каллус табака (Nicotiana spp. L.) были выявлены значительные изменения в динамике накопления флавоноидов по сравнению с контролем — максимум накопления веществ сместился с 25 на 45 день эксперимента [41].
- 2) Участие во взаимоотношениях растений с бактериями и грибами.
Кроме хорошо известной фитоиммунной активности, для фенольных соединений, выделяемых корнями, характерна аллелопатическая активность. Показано ингибирование ими клубеньковых бактерий у бобовых трав в сложных травосмесях [15]. Активно изучается также стимуляция и ингибирование флавоноидами nod-генов бобовых и сопутствующие события [42, 43, 44, 45]. В частности, при изучении белого клевера (Trifolium repens L.) установлено, что образующиеся в корнях при нодуляции флаваноиды участвуют в регуляции баланса в этих клетках ауксинов [ 46, 47]. Показано участие флавоноидов в стимуляции nod-генов у ризобий при организации их отношений с люцерной [48]. Но особенно сложную динамику эти вещества имеют в случае инфицирования растения фитопатогеном, что показано на фенольных комплексах ржи, ячменя и пшеницы [49, 50]. Установлено, что источником флавоноидных гликозидов могут служить как ткани растения — хозяина, так и внедрившийся фитопатоген. Изначально при облигатном паразитизме отношения скорее дружественные (синергизм), но в дальнейшем между фенольными соединениями, синтезируемыми фитопатогенном и растениемхозяином, возникает дисбаланс, что и вызывает у растенияхозяина защитную реакцию. При этом установлено, что облигатные фитопатогены индуцируют более сильное и длительное накопление фенольных соединений, чем факультативные [49].
3) Рострегулирующая активность.
Имеются данные о функционировании флавоноидов в качестве гормоноподобных соединений [51]. При этом обсуждаются:
- 1) непосредственная гормональная активность этих соединений. Некоторыми авторами отмечается, что гликозилированные формы флавоноидов обладают рострегулирующей активностью. Активность их растет в ряду: флавоны <�флавонолы < оксикумарины < фенолкарбоновые кислоты. Отмечается, что гликозиды флавонов флавонолов и оксикумаринов по сравнительной активности уступают агликонам [50].
- 2) участие в изменении активности самих растительных гормонов. Например, было показано, что флавоноиды могут регулировать, и в частности подавлять системы, ответственные за трансмембранный перенос ауксинов (auxin efflux carrier complex) у арабидопсиса сначала in vitro, а затем in vivo [52]. Также было показано воздействие и на полярный транспорт ауксинов. В результате этого у различных растений может нарушаться гравитропизм и снижается скорость роста корней [53].
- 3) регуляция их активности гормонами растений. Например, на развивающихся цветках петунии (Petunia hybrida Hort.) было показано, что гиббереллины повышают активность халкон-флаванон-изомеразы — одного из важнейших ферментов биосинтеза флавоноидов. При этом активируется также и синтез антоцианов [54].
- 4) Участие в морфогенезе и функционировании генеративных органов. У разных растений (в частности, у кукурузы и петунии) было выявлено активное участие флавоноидов в процессах полового размножения — развитии пыльцы и пестика, привлечении опылителей, прорастании пыльцевой трубки и т. д. В частности, растениях томата (Solanum lycopersicum L) показано, что РНК-зависимое блокирование гена халкон-синтазы, работа которого лежит в основе всего метаболизма флавоноидов, приводит к образованию плодов партенокарпического типа, не имеющих семян [16].
Считается, что эволюция растений и эволюция их метаболических путей биосинтеза флавоноидов тесно связаны [3, 55]. Существует даже теория, что, появляясь в ходе эволюции, отдельный вид растений изначально синтезирует максимально возможный список флавоноидов. Это можно наблюдать в местах, соответствующих «предковой экологии вида» [9]. Показано, что у бобовых растений это связано с «оптимальностью» условий влагообеспеченности. По мере расселения из мест с оптимальными условиями список синтезируемых соединений постепенно уменьшаться, отражая эволюционноэкологическое становление вида [8]. Следовательно, можно ожидать, что на границах ареала пластичность и многообразие синтезируемых соединений будут минимальными.
Таким образом, влияние условий произрастания на качественный и количественный состав накапливаемых растениями флавоноидов велико и многообразно. Поэтому можно ожидать, что в тех регионах, в которых наблюдается высокое разнообразие экологических условий, разнообразие накапливаемых растениями флавоноидов будет также высоко. Южный Урал, и особенно его горные районы, относится именно к таким регионам [6, 7, 22, 56].
С одной стороны, Южный Урал, в силу уникальности своего географического положения, отличается очень большим количеством произрастающих на его территории лекарственных растений и растений народной медицины. Всего на территории России произрастает 250 видов лекарственных растений, из которых 150 встречаются на территории Республики Башкортостан. [57]. Среди них встречаются и уникальные эндемичные виды [58].
С другой стороны, высокое разнообразие условий произрастания в этом регионе накладывается на специфический погодный режим — это режим непредсказуемого изменения (флуктуирования) неблагоприятных факторов [56]. Годы с устойчивым доминированием какого-то одного режима (только засуха, или только переувлажнение) в этом регионе скорее исключение, чем правило.
В результате произрастающие в этом регионе растения отличаются чрезвычайной пластичностью химического состава.
Так при исследовании химсостава произрастающих в этом регионе растений Можжевельника казацкого (Juniperus sabina L) методом ВЭЖХ всего было выделено:
в мужских растенияхв стеблях — 60, в хвое — 40 соединений;
в женских растениях: — в стеблях — 51, в хвое — 42, в шишкоягодах — 43 соединения. При этом было обнаружено, чтов зависимости от места произрастания содержание выявленных соединений от общего их перечня может варьировать от 35 до 70%. Установлено, что наиболее консервативным химическим составом отличаются шишкоягоды можжевельника, а наиболее пластичным — стебли. [22].
При изучении накопления биологически активных веществ эндемиком Южного Урала солодкой Коржинского (Glycyrrhiza korshinskyi Grig.) было выявлено, что количественный состав накапливаемых метаболитов сильно зависит от микроэлементного состава и показателя кислотности почвы. Так, установлено, что в зависимости от гидролитической кислотности почвы содержание глицирризиновой кислоты в корнях растений этого вида может варьировать от 0,8 до 1,9%, а содержание флавоноидов в корнях при разных концентрациях в почве ионо в алюминия и калия может меняться от 0,08 до 0,18%, т. е. больше чем в 2 раза [59].
В ходе исследований химического состава тысячелистника великолепного (Achillea nobilis L) на Южном Урале было выявлена значительная пластичность в накоплении этими растениями эфирных масел и флавоноидов. Так содержание эфирных масел в корнях варьировало от 6 до 8, в корнях от 5 до 9%. [7, 60] Количество метаболитов зарегистрированных методом ВЭЖХ, накопленных в отдельных соцветиях, варьировало в пределах от 52 до 65,5% от максимально возможного (29 соединений), у листьев этот показатель составил 38,2 от 55,9% (всего-34 вещества), а у стеблей — от 55 до 85% (всего -20 веществ).Таким образом, максимальная пластичность химического состава зарегистрирована у листьев, минимальная — у стеблей тысячелистника великолепного. Соцветия по этому показателю занимали промежуточное положение. 7,60].
В результате можно ожидать, что в силу высокой мозаичности условий жизни, растения Южного Урала будут отличаться повышенным, по сравнению с другими регионами, разнообразием состава накапливаемых флавоноидов. Более того, не исключено, что у отдельных видов растений можно будет обнаружить некие уникальные и характерные только для Южного Урала флавоноидные соединения или их комбинации, то есть своеобразные «химические эндемики"[57].
Влияние онтогенетических факторов и условий среды на накопление флавоноидов в растениях:
- 1. На накопление флавоноидов оказывают влияние возраст и фаза развития растения. В молодых растениях их больше; в старых растениях их количество уменьшается. Максимальное содержание флавоноидов наблюдается в цветках, листьях и травах в период бутонизации и цветения, а к фазе плодоношения содержание снижается; в плодах и семенах — в период молочной зрелости — полного созревания; в корнях — в период увядания надземной массы осенью.
- 2. На накопление флавоноидов влияет освещенность. Содержание флавоноидов в растениях увеличивается с ростом освещенности, а степень их гидроксилирования (числоОН групп) — с увеличением высоты над уровнем моря.
- 3. На накопление флавоноидов влияет температура. Содержание антоцианов увеличивается при понижении температуры (покраснение листьев у щавеля), у других групп флавоноидов, наоборот, содержание увеличивается при повышении температуры [Курсанов, А. Л. Транспорт ассимилятов в растении /А.Л. Курсанов. — М.: Наука, 1999. — 648 с].
Применение флавоноидов в медицине и других отраслях народного хозяйства:
Диапазон терапевтического применения растительного сырья, богатого флавоноидами, очень широк. Флавоноиды не токсичны для человека при любом способе введения.
Ранее других биологических свойств флавоноидов было обнаружено их сосудоукрепляющее действие. Благоприятное влияние флавоноидов на состояние капиллярной системы обычно проявляется в снижении патологически повышенной проницаемости капилляров и в устранении их ломкости и хрупкости. Именно это свойство витамина Р открывает широкие возможности для терапевтического его применения, так как повышение проницаемости и ломкости сосудов довольно часто встечается в патологии человека. Так, изменение сосудистой стенки наблюдается при ревматизме, гипертонической болезни, базедовой болезни, пневмониях и при многих инфекционных заболеваниях.
Установленно, что флавоноиды способствуют сохранению аскорбиновой кислоты в организме, приводят к её накоплению в органах, прежде всего в надпочечниках. Учитывая эти данные, флавоноиды рекомендуют больным С-гиповитаминозом в комплексе с аскорбиновой кислотой.
Кроме того, флавоноиды оказывают нормализующее влияние на лимфоток, с чем, по-видимому, согласуется их противоотечное действие.
Наряду с действием на сосуды, флавоноиды известны и как слабые кардиотонические средства: они способны урежать ритм сердечных сокращений и увеличивать их амплитуду. По другим данным, кверцетин, рутин и другие флавонолы восстанавливают силу утомленного или гиподинамического сердца, нормализуют пульс. Некоторые флавоноиды обладают слабым гипотензивным действием.
Флавоноидные соединения влияют на состав крови, снижают уровень холестерина и в-липопротеидов, что наблюдали под действием кверцетина, лютеолина и других Р-витаминных препаратов.
Одним из ценных свойств флавоноидов является их положительное влияние на функцию печени: они усиливают желчеотделение, улучшают ее детоксицирующую способность по отношению к таким веществам, как барбитураты, мышьяк. Детоксикации организма способствует свойство флавоноидов оказывать мочегонное влияние. Некоторые флавоноиды из семейства норичниковых благоприятно влияют на пищеварение, понижают тонус гладкой мускулатуры кишечника, и оказывают спазмолитическое действие при спазмах мускулатуры желудочно-кишечного тракта. Большое значение придается противовоспалительному действию флавоноидов, с чем, возможно, связаны их противоязвенное, ранозаживляющее, жаропонижающее и вяжущее действия. Привлекают внимание и антимикробные свойства флавоноидов. Так, выявлено отрицательное влияние кверцетина на граммположительных бактерий, флавонов и халконов — на стафилококка. Антимикробное действие отмечается у антоцианов.
В заключение перечня свойств флавоноидов необходимо упомянуть об их противоопухолевом, радиозащитном, также об эстрогенном действии одной из групп — изофлавонов, которые благодаря этому свойству могут воздействовать на воспроизводительную функцию организма [Кретович, В. Л. Биохимия растений /В.Л. Кретович. — М.: Высшая школа, 2000. — 445 с.].