Задачи по химии с использованием понятий «эквивалент», «нормальная концентрация»

Молярная масса водорода 2 г/моль, а объем при н.у. — 22,4 л/моль. Эквивалентная масса водорода равна 1 г/моль и, следовательно, эквивалентный объем — Vэкв (H2) = 11,2 л/моль. Отсюда можно вывести формулу для расчета эквивалентной массы неизвестного металла. Фактор эквивалентности окислителя (восстановителя) — величина, обратная количеству электронов, которое присоединяет (отдает) в данной… Читать ещё >
Задачи по химии с использованием понятий «эквивалент», «нормальная концентрация» (реферат, курсовая, диплом, контрольная)
Эквиваленты
Эквивалент — реальная или условная частица вещества, которая химически равноценна одному иону водорода (для обменных реакций) или одному электрону (для окислительно-восстановительных реакций).
Фактически это частица, обладающая одной единицей валентности или оперирующая одним электроном.
Формулы для вычисления эквивалентов:
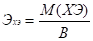
где В — валентность химического элемента.
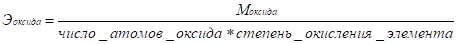
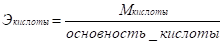
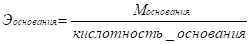
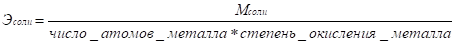
Эквивалент элемента — такое его количество, которое соединяется с 1 моль атомов водорода или замещает то же количество атомов водорода в химических реакциях.
Эквивалент Э часто обозначают Мэкв — эквивалентная масса.
[Мэкв]=г/моль.
Для атомов элементов с переменной валентностью необходимо предвидеть схему химического процесса, в котором предполагается использовать вещество с целью установления валентности в данном случае.
Фактор эквивалентности — число, показывающее, какая доля реальной частицы вещества Х эквивалентна одному иону водорода в данной обменной реакции или одному электрону в данной окислительно-восстановительной реакции.
Например, в обменной реакции хлорида железа (III) с гидроксидом натрия возможны три варианта обмена:
FeCl3 + NaOH = FeOHCl2 + NaCl (1).
FeCl3 + 2NaOH = Fe (OH)2Cl + 2NaCl (2).
FeCl3 + 3NaOH = Fe (OH)3 + 3NaCl (3).
В реакции (1) эквивалентная масса хлорида железа (III) равна молярной массе, в реакции (2) она равна Ѕ*M (FeCl3), в реакции (3) — 1/3*M (FeCl3).
Мэкв(FeCl3) = f* M (FeCl3), где f — фактор эквивалентности.
В рассмотренных случаях он равен 1, Ѕ или 1/3 соответственно для трех уравнений реакций.
Фактор эквивалентности окислителя (восстановителя) — величина, обратная количеству электронов, которое присоединяет (отдает) в данной окислительно-восстановительной реакции одна молекула или один ион окислителя (восстановителя).
Для процессов, связанных с перераспределением электронов, важно знать частицу, способную отдать или принять один электрон.
8HNO3 + 2HNO3 + 4Mg = 4Mg (NO3)2 + N2O + 5H2O.
+5 +1.
окислитель 2N + 8e 2N *1 пр. восстановления.
0 +2.
восстановитель Мg — 2e Mg *4 пр. окисления Молярная масса эквивалента азотной кислоты как окислителя равна ј ее молярной массы, т. е. фактор эквивалентности ее в этом процессе равен ј.
При расчетах по уравнениям химических реакций необходимо применять закон эквивалентов.
Закон эквивалентов:
- — вещества взаимодействуют друг с другом в количествах пропорциональных их эквивалентам;
- — массы (объемы) реагирующих веществ пропорциональны их эквивалентным массам (объемам).
Массы веществ, участвующих в химическом процессе, относятся как их эквивалентные массы:
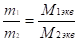
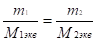
или или n1экв = n2экв.
Задачи, в решении которых используется понятие «эквивалент»
1. Неизвестный трехвалентный металл массой 0,36 г при обработке избытком раствора серной кислоты выделяет 448 мл (н.у.) водорода. Определите, какой металл вступил в реакцию с серной кислотой.
Решение:
1) Вычисляем объем, который при нормальных условиях занимает эквивалентная масса водорода.
Vэкв(H2).
Молярная масса водорода 2 г/моль, а объем при н.у. — 22,4 л/моль. Эквивалентная масса водорода равна 1 г/моль и, следовательно, эквивалентный объем — Vэкв(H2) = 11,2 л/моль. Отсюда можно вывести формулу для расчета эквивалентной массы неизвестного металла.
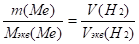
2) Вычисляем эквивалентную массу неизвестного металла.
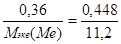
Mэкв(Me) = 9 г/моль.
3) Вычисляем молярную массу металла.
M (Me) = Mэкв(Me)/f = 9/(1/3) = 27 г/моль.
Ar = 27
Ответ: алюминий Al.
2. При взаимодействии 2,6 г неизвестного двухвалентного металла с кислотой было получено 896 мл водорода (н.у.). Какой металл взаимодействовал с кислотой?
Решение:
Me0— 2з Me+2
2H+1 + 1з * 2 H20
Me + 2H+ Me2+ + H2
;
г/моль.
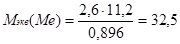
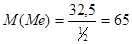
г/моль Ответ: металл — цинк Zn.
3. Выведите формулу оксида неизвестного металла, если 1,775 г его при растворении в разбавленной серной кислоте образуют 3,775 г сульфата этого металла.
Решение:
1. Mэкв (оксида) = Mэкв (Me) + Mэкв (O), а эквивалентная масса сульфата равна сумме эквивалентных масс иона металла и сульфат-иона.
Mэкв(сульфата) = Mэкв(Ме) + Mэкв(SO4)
2. Вычисляем эквивалентную массу метала, обозначив ее через x.
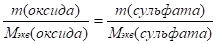
.
но Mэкв(оксида) = (x + 8) г/моль,.
а Mэкв(сульфата) = (x + 48) г/моль и.
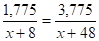
3. Вычисляем молярную массу металла:
M (Me) = Mэкв(Me) / f = 27,5 / 1 = 27,5 г/моль.
При f = 1 — такого металла нет; при f = ½M (Me) = Mэкв(Me) / f = 27,5 / 0,5 = 55 г/моль Это марганец.
Ответ: оксид марганца (II) MnO.
4. Вычислите эквивалентную массу серной кислоты, если в реакции с гидроксидом калия получается гидросульфат.
Решение:
H2SO4 + KOH = KHSO4 + H2O.
из приведенной записи видно, что в реакции с одним молем КОН участвует 1 моль серной кислоты, и фактор эквивалентности равен 1.
Находим эквивалентную массу серной кислоты:
Мэкв(H2SO4)=f*М (H2SO4)=1*98г/моль=98г/моль Ответ: Мэкв(H2SO4) =98г/моль.
5. Вычислите эквивалентную массу ортофосфорной кислоты, если в реакции ее с гидроксидом натрия образуется гидрофосфат натрия.
Решение:
H3PO4 + 2NaOH = Na2HPO4 + 2H2O.
Mэкв(H3PO4) = Ѕ* M (H3PO4) = Ѕ * 98 г/моль = 49 г/моль.
(молярная масса эквивалента (эквивалентная масса)).
Ответ: Mэкв(H3PO4) = 49 г/моль.
6. Вычислите эквивалентную массу сульфата алюминия, если при взаимодействии с щелочью образуется дигидросульфат алюминия.
Решение:
Al2(SO4)3 + 4NaOH = [Al (OH)2]SO4 + 2Na2SO4
Mэкв(Al2(SO4)3) = ј * M (Al2(SO4)3) = 342г/моль / 4 = 85,5 г/моль Ответ: Mэкв(Al2(SO4)3) = 85,5 г/моль.
7. Вычислить эквивалент и эквивалентную массу сероводорода, если он окисляется до серной кислоты.
Решение:
Н2S + 4 H2O = SO42- + 10H+ +8e.
f=1/8.
M (Н2S)=34 г/моль, Мэкв(Н2S)=f* M (Н2S)=1/8 *34=4,25 г/моль Ответ: Мэкв(Н2S)=4,25 г/моль.
- 8. Вычислить эквивалентную массу серной кислоты в следующих реакциях:
- а) Zn + H2SO4(разб) = ZnSO4 + H2;
- б) 2НBr + H2SO4(конц) =Br2 + SO2 + 2H2O;
- в) 8HI + H2SO4(конц) =I2 + H2S + 4 H2O.
Решение:
а) Мэкв(Н2SO4)=f* М (Н2SO4); f=½ Мэкв(Н2SO4)=f* М (Н2SO4).
Мэкв(Н2SO4)=49г/моль б) SO42- +4Н+ +2е SO2 + Н2О; f=½.
Мэкв(Н2SO4)=49г/моль в) SO42- +10Н+ +8е Н2S + 4Н2О; f=1/8.
Мэкв(Н2SO4)=12,25г/моль.
9. Вычислить эквивалентные массы следующих восстановителей: хлорида олова (II); фосфора, если он окисляется до Н3РО4; пероксида водорода, окисляющегося до молекулярного кислорода.
Решение:
а) SnCl2 Mэкв=f*М (в-ва).
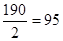
Sn2+ — 2e Sn4+ f=½ Mэкв(SnCl2)=г/моль.
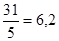
б) Р0 — 5е Р+5 f=1/5 Мэкв(Р)=г/моль.
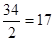
- в) 2О-1 -2е О20 f=½ Мэкв(H2O2)= г/моль
- 10. Чему равны эквивалент и эквивалентная масса перхлората калия КСlО4, если он восстанавливается: а) до диоксида хлора; б) до свободного хлора; в) до хлорид-иона?
Решение:
а) СlО4— +4Н+ + 3е ClO2 + 2H2O.
f=1/3 Mэкв(КСlO4)=1/3*138,5=46,17г/моль б) 2СlО4— +16Н+ + 14е Cl2 + 8H2O.
f=1/7 Mэкв(КСlO4)=1/7*138,5=19,79г/моль в) СlО4-+8Н+ + 8е Cl— + 4H2O.
f=1/8 Mэкв(КСlO4)=1/8*138,5=17,3г/моль.
11. Сколько эквивалентов КI необходимо для восстановления в кислой среде 1 моля: а) К2Сr2О7; б) КМnО4?
Решение:
- а) Сr2О72- +14Н+ +6е 2Сr3+ + 7Н2О * 1
- 2I- — 2e I2 * 3
По определению фактора эквивалентности восстановителя f для КI равен 6 моль.
- б) МnО4- + 8Н+ +5е Мn2+ + 4Н2О * 2
- 2I- — 2e I2 * 5
f для КI равен 5 моль.
Нормальная концентрация (нормальность) — число эквивалентов растворенного вещества, содержащееся в 1 л раствора.
![Нормальная концентрация - это отношение количества вещества эквивалента к объему раствора:; [CH]=моль/л.](/img/s/9/32/1759432_17.png)
Нормальная концентрация — это отношение количества вещества эквивалента к объему раствора:; [CH]=моль/л.
Тип 1.
Уровень 1
Задачи, при решении которых используется понятие «молярная концентрация».
1.1.1. Какова нормальность раствора, если в 300 мл его содержится 0,24 г NaOH?
Решение:
Мэкв(NaOH)=40 г/моль.
n экв(NaOH)=.
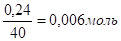
Сн(NaOH)=.
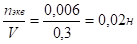
Ответ: Сн(NaOH)=0,02н.
1.1.2. Определите массу серной кислоты, которая содержится в 3500 мл 0,4 н раствора?
Решение:
n экв(Н2SO4)=Сн*V =0,4 * 3,5 =1,4 моль.
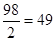
Мэкв(Н2SO4)=г/моль.
m (Н2SO4)=1,4моль * 49г/моль = 68,6 г Ответ: m (Н2SO4) = 68,6 г.
- 1.1.3. Вычислить массу серной кислоты, необходимую для приготовления 500 мл 0,1 н раствора.
- 1.1.4. Как приготовить:
- а) 1 л 1 н раствора NaOH из твердого NaOH;
- б) 2 л 0,5 н раствора H2SO4 из 100%-ной H2SO4;
- г) 250 мл 0,1 н раствора Al2(SO4)3 из твердого Al2(SO4)3;
- д) 2 л 0,01 н раствора AgNO3 из твердого AgNO3?
Уровень 2
эквивалент реакция химический концентрация Связь нормальной концентрации с другими способами выражения концентрации растворов.
1.2.1. Плотность 15%-ного раствора серной кислоты равна 1,105г/мл. Вычислить нормальность раствора.
Решение:
Пусть m (H2SO4)15%=100г, тогда m (H2SO4)=15г.
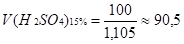
мл г/моль моль.
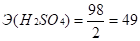
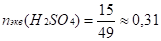
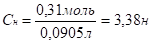
Ответ: Сн(H2SO4)=3,38н.
1.2.2. Какова нормальная концентрация 22%-ного раствора серной кислоты?
Решение:
Пусть mр-ра(H2SO4) = 100 г.
Мэкв(H2SO4) =г/моль Сн(H2SO4) =.
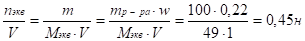
Ответ: Сн (H2SO4) =0,45н.
- 1.2.3. Как приготовить:
- в) 500 мл 2 н раствора НСl из 36,5%-ного раствора НСl;
- 1.2.4. Определите массовую долю гидроксида натрия в 2 н растворе плотностью 1,08?
- 1.2.5. Определите объем 96%-ной серной кислоты плотностью 1,84 нужно взять для приготовления 1 л 0,5 н раствора?
- 1.2.6. Определите массу медного купороса CuSO4*5H2O надо взять для приготовления 2 л 0,1 н раствора?
- 1.2.7. Перепишите таблицу в тетрадь, заполните пустые места в таблице.
раствор | объем раствора. | масса в объеме раствора. | количество вещества. | молярность раствора. | количество вещества эквивалентов. | нормальность раствора. |
а)серной кислоты Н2SO4 | 1 л. | 0,5. | 0,5. | |||
б)серной кислоты Н2SO4 | 500 мл. | 24,5. | ||||
в)серной кислоты Н2SO4 | 2 л. | |||||
г)гидроксида натрия NaOH. | 1 л. | |||||
д)гидроксида натрия NaOH. | 0,1. | |||||
е)гидроксида натрия NaOH. | 500 мл. | |||||
ж)сернокислого алюминия Al2(SO4)3 | 250 мл. | 0,1. |
- 1.2.8. В 1 л воды растворили 1 моль сульфата натрия. Концентрация соли в растворе (с=1,03г/мл) процентная, молярная, нормальная равна:
- 1) 12,43%; 1,25 М; 2,50н.
- 2) 15,05%; 0,96 М; 1,70н.
- 3) 13,45%; 0,96 М; 1,92н.
- 4) 12,43%; 0,95 М; 1,80н.
- 1.2.9. В 1 л воды растворили 23,4 г дигидрофосфата кальция. Концентрация соли в полученном растворе, имеющим плотность 1,05 г/мл процентная, молярная, нормальная равна:
- 1) 2,3%; 0,103 М; 0,0515н.
- 2) 1,4%; 0,114 М; 0,0570н.
- 3) 1,5%; 0,120 М; 0,0600н.
- 4) 1,6%; 0,128 М; 0,0640н.
Тип 2.
Уровень 1
Расчеты по химическим уравнениям, где один из реагентов — раствор с заданной нормальностью.
2.1.1. Определить массу карбоната кальция, который выпадает в осадок, если к 400мл 0,5н раствора СаСl2 прибавить избыток раствора соды?
Решение:
nэкв(СаСl2)=Сн*V (СаСl2)= 0,5*0,4 =0,2моль.
nэкв(СаСО3)=0,2моль Мэкв(СаСО3)=f* М (СаСО3) f (СаСО3)=½.
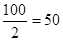
Мэкв(СаСО3)=г/моль.
m (СаСО3)=0,2моль*50г/моль= 10 г Ответ: m (СаСО3)=10г.
2.1.2. Определить массу осадка, если к 100 мл 1 н раствора хлорида магния прилить 400 мл 0,5 н раствора нитрата серебра.
Уровень 2
Использование закона эквивалентов.
- 2.2.1. Сколько миллилитров 0,1 н раствора серной кислоты пойдет на нейтрализацию:
- а) 10 мл 0,1 н раствора гидроксида натрия;
- б) 25 мл 0,2 н раствора гидроксида калия;
- в) 50 мл 0,01 н раствора гидроксида кальция;
- г) 100 мл 0,2 н раствора гидроксида бария?
- 2.2.2. Сколько 0,5 н раствора гидроксида натрия требуется для нейтрализации:
- а) 100 мл 0,5 н раствора соляной кислоты;
- б) 100 мл 0,5 н раствора серной кислоты;
- в) 100 мл 0,5 М раствора серной кислоты;
- г) 100 мл 0,5 н раствора фосфорной кислоты;
- д) 100 мл 0,1 н раствора серной кислоты;
- е) 100 мл 1 н раствора азотной кислоты;
- ж) 10 мл 1 н раствора азотной кислоты;
- з) 10 мл 1 М раствора азотной кислоты?
- 2.2.3. Вычислите нормальность раствора серной кислоты, если для титрования:
- а) 10 мл 1 н раствора гидроксида натрия потребовалось 20 мл раствора серной кислоты;
- б) 20 мл 0,1 н раствора гидроксида калия потребовалось 24 мл раствора серной кислоты;
- в) 50 мл 0,5 н раствора гидроксида натрия было израсходовано 40 мл раствора серной кислоты?
- 2.2.4. Какой объем 0,12н раствора гидроксида натрия потребуется для реакции с 40 мл 0,15н раствора серной кислоты? (50мл)
Решение:
2NaOH + H2SO4 = Na2SO4 + 2H2O.
Сн(H2SO4) * V (H2SO4) = Сн(NaOH) *V (NaOH) (закон эквивалентов).
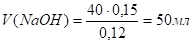
Ответ: V (NaOH)=50мл.
2.2.5. Для нейтрализации 40мл раствора серной кислоты потребовалось 24мл 0,2н раствора щелочи. Определить нормальность раствора серной кислоты. (0,12н)
Решение:
Сн(H2SO4) * V (H2SO4) = Сн(NaOH) *V (NaOH) (закон эквивалентов).
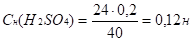
Ответ: Сн(H2SO4)=0,12н.
2.2.6. Какой объем 0,2н раствора щелочи потребуется для осаждения в виде Fe (OH)3 всего железа, содержащегося в 100мл 0,5н раствора хлорида железа (III)?
Решение:
Сн(FeCl3) * V (FeCl3) = Сн(NaOH) *V (NaOH) (закон эквивалентов).
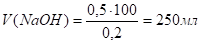
Ответ: V (NaOH)=250мл.
2.2.7. На нейтрализацию 40мл раствора щелочи израсходовано 24мл 0,5н раствора серной кислоты. Какова нормальность раствора щелочи? Какой объем 0,5н раствора соляной кислоты потребовался бы для той же цели?
Решение:
Сн(H2SO4) * V (H2SO4) = Сн(щ) *V (щ) (закон эквивалентов) Сн(щ)=.
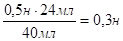

Ответ: V (HCl)=24мл.
2.2.8. Для нейтрализации 30 мл раствора фосфорной кислоты Н3РО4 потребовалось 20 мл 2 н раствора гидроксида натрия NaOH. Определить нормальную концентрацию кислоты?
Решение:
Н3РО4 + 3 NaOH = Na3РО4 + 3 Н2О Сн(к) * V (к) = Сн(щ) *V (щ) (закон эквивалентов) Сн(к)=.
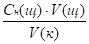
Сн(Н3РО4)=.
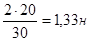
Ответ: Сн(Н3РО4)=1,33н.
2.2.9. Определить нормальность раствора соляной кислоты, если известно, что для нейтрализации 20,2 мл ее потребовалось затратить 18,6 мл 0,126 н раствора NaOH.
Решение:
Сн(к) * V (к) = Сн(щ) *V (щ) (закон эквивалентов) Сн(НСl)=.
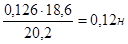
Ответ: Сн(НСl)=0,12н.
2.2.10. Для нейтрализации 20мл 0,1н раствора кислоты потребовалось 8мл раствора NaOH. Сколько граммов NaOH содержит 1л этого раствора?
Решение:
Сн(к) * V (к) = Сн(NaOH) *V (NaOH) (закон эквивалентов) Сн(NaOH)=.
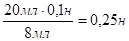
nэкв(NaOH)= Сн(NaOH)* V (NaOH)=0,25н*1л=0,25моль Мэкв(NaOH)=40г/моль.
m (NaOH)=0,25моль*40г/моль=10г Ответ: m (NaOH)= 10 г.
2.2.11. Смешали 15 мл 2 н раствора щелочи и 10 мл 3 н раствора кислоты. Какую реакцию (кислую, щелочную или нейтральную) будет иметь полученный раствор?
Решение:
Сн(к) * V (к) = Сн(щ) *V (щ) (закон эквивалентов).
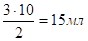
V (щ)= ————- совпадает с условием ==> рН=7.
- 2.2.12. Сколько миллилитров 2 н раствора Na2CO3 надо прибавить к 50 мл 1,5 н раствора ВаСl2, чтобы полностью осадить барий в виде ВаСО3?
- 2.2.13. На нейтрализацию 10 мл раствора гидроксида натрия пошло 6 мл 0,5 н раствора соляной кислоты. Вычислить нормальность раствора щелочи.
- 2.2.14. Какой должна быть реакция раствора на индикаторы (кислая, щелочная или нейтральная), если:
- а) к 10 мл 0,1 н раствора Н2SO4 прилить 10 мл 0,1 н раствора NaOH;
- б) к 50 мл 1 н раствора НСl прилить 100 мл 0,5 н раствора КОН;
- в) к 50 мл 0,1 н раствора NaOH прилить 20 мл 0,2 н раствора Na2SO4?
Как во всех этих случаях изменится окраска метилоранжа и фенолфталеина?
2.2.15. Для нейтрализации раствора, содержащего 2,25 г кислоты, потребовалось 25 мл 2 н раствора щелочи. Определить эквивалентную массу кислоты.
Решение:
m (к)=Мэкв(к)*nэкв(к).
nэкв(к)= nэкв(щ) по закону эквивалентов.
nэкв(к)=Сн*Vр-ра = 0,025*2 = 0,05 моль.
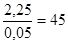
Мэкв(к)=г/моль Ответ: Мэкв(к)=45 г/моль.
2.2.16. На нейтрализацию 20 мл раствора, содержащего в 1 л 12 г щелочи, израсходовано 24 мл 0,25 н раствора кислоты. Рассчитайте эквивалентную массу щелочи.
Решение:
nэкв(к)= nэкв(щ)= 0,024*0,25 = 0,006 моль.
- 1 л щелочи ————- 12 г щелочи х=m (щ)=0,24 г
- 0,02 л ————- х
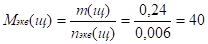
г/моль Ответ: Мэкв(щ)= 40 г/моль.
Уровень 3
Комбинированные задачи.
2.3.1. Для полного осаждения сульфата бария из 100 г 15%-ного (по массе) раствора хлорида бария потребовалось 14,4 мл серной кислоты. Найти нормальность раствора серной кислоты.
Решение:
ВаСl2 + H2SO4 = BaSO4 + 2HCl.
m (ВаСl2)=mр-ра(ВаСl2)*w (ВаСl2)= 100* 0,15 = 15 г М (ВаСl2)=г/моль.
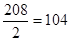
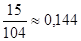
nэкв(ВаСl2)=моль.
nэкв (H2SO4)= 0,144 моль Сн(H2SO4)=.
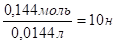
Ответ: Сн(H2SO4)=10н.
2.3.2. После упаривания 5 л 2 н раствора гидроксида калия КОН получено 2 л раствора. Сколько миллилитров этого раствора необходимо для нейтрализации 10 мл 4%-ного раствора H2SO4.
Решение:
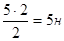
- 1) Сн(КОН)= — после упаривания
- 2) пусть mр-ра(Н2SO4)= 100 г, тогда
Мэкв(H2SO4) =г/моль.
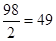
Сн(H2SO4) =.

3) Сн(к) * V (к) = Сн(щ) *V (щ) (закон эквивалентов).
V (щ)=.
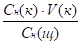
V (КОН)=.
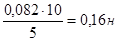
Ответ: V (КОН)=0,16н.
2.3.3. В лаборатории имеется раствор нитрата калия неизвестной концентрации. Для её определения 200 мл раствора выпарили, полученный остаток высушили и затем прокалили до постоянной массы. При этом выделилось 0,244 л газа (измеренного при н.у.). Определить нормальную концентрацию исходного раствора соли.
Решение:
2КNO3 ==2 KNO2 + O2
nэкв(О2)=.
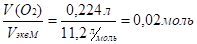
nэкв(КNO3)= nэкв(О2) (закон эквивалентов).
nэкв(КNO3)=0,02 моль Сн(КNO3)=.
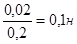
Ответ: Сн(КNO3)=0,1н.
2.3.4. Имеется смесь карбоната и гидрокарбоната натрия. На нейтрализацию 20 мл раствора этой смеси пошло 5 мл 1 н раствора гидроксида натрия. После упаривания полученного раствора и высушивания остатка на воздухе до постоянной массы получено 2,86 г кристаллогидрата Na2CO3*10H2O. Каков состав смеси (в процентах)?
Решение:
NaHCO3 + NaOH = Na2CO3 + H2O.
1) m (Na2CO3*10H2O)=2,86 г ——— wкр(Na2CO3)=.
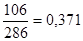
m кр(Na2CO3)=2,86*0,371= 1,06 г.
2) nэкв(NaOH)= Cн * V=1н * 0,005л=0,005моль.
nэкв(NaOH)= nэкв(NaНСO3).
nэкв(NaНСO3)=0,005 моль; Мэкв(NaНСO3)=84г/моль.
mэкв(NaНСO3)=84 * 0,005 = 0,42 г.
3) nэкв(Na2СO3)=0,005 моль —- по уравнению реакции Мэкв(Na2СO3)=53 г/моль; m (Na2СO3)= 53 * 0,005 = 0,265 г.
- 4) m (Na2СO3)=1,06 — 0,265 = 0,795 г — в смеси
- 5) m (смеси)=0,42 + 0,795= 1,215 г
w (NaHCO3)=34,5% w (Na2CO3)= 65,4%.
Ответ: w (NaHCO3)=34,5% w (Na2CO3)= 65,4%.
- 2.3.5. Хлороводород растворен в 1 л воды. На нейтрализацию 10 мл полученного раствора истрачено 5 мл 0,1 н раствора гидроксида натрия. Какой объем хлороводорода растворен и какова нормальная концентрация полученного раствора кислоты?
- 2.3.6. 1 л 0,5 М раствора гидроксида натрия смешали с 1 л 0,4 н раствора серной кислоты. Сколько молей, и какого вещества осталось в избытке?
- 2.3.7. На титрование 10 мл раствора соляной кислоты пошло 15 мл 0,5 н раствора щелочи. Вычислить: 1) нормальность раствора соляной кислоты; 2) концентрацию раствора (г/л).
- 2.3.8. Какую массу оксалата аммония (NH4)2C2O4 можно окислить действием 50 мл 0,2 н раствора перманганата калия в кислой среде?
Решение:
nэкв(КМnО4)=0,05 * 0,2 =0,01 моль.
nэкв((NH4)2C2O4)= 0,01 моль.
C2O42- -2е 2СО2
f=½.
Мэкв((NH4)2C2O4)=.
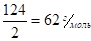
m ((NH4)2C2O4)=62*0,01=0,62 г Ответ: m ((NH4)2C2O4) =0,62 г.
- 1. Б. Н. Архипов. Задачи и упражнения по неорганической, органической и аналитической химии. М.: изд. «Высшая школа». 1965.
- 2. 500 задач по химии: Пособие для учащихся А. С. Гудкова, К. М. Ефремова, Н. М. Магдесиева, Н. В. Мельчакова. 2-е изд. М.: Просвещение, 1981.
- 3. Задачи по химии: Нет ничего проще: учебное пособие для 8−11 кл./Крестинин А.Н. М.: Издат. дом «Генжер», 1998.
- 4. Готовимся к ЕГЭ: Химия/О.С.Габриелян, П. В. Ремстов, И. Г. Остроумов и др. М.: Дрофа, 2003.
- 5. Глинка Н. Л. Задачи и упражнения по общей химии. Учебное пособие для вузов/ Под ред. В. А. Рабиновича и Х. М. Рубиной. Л.: Химия, 1984.
- 6. Г. П. Хомченко. Пособие по химии для поступающих в ВУЗы. М. 1967.
- 7. Практические занятия по химии в классах естественнонаучного профиля. Пособие для учащихся. СПб.: Санкт-Петербургский Государственный университет, химический факультет. 1998.
- 8. Ф. П. Платонов. Практикум по неорганической химии. Изд. «Высшая школа». М. 1968.