Экспериментальная часть.
Получение, очистка и исследование процесса коагуляции коллоидного раствора

Для проверки правильности предположения о заряде коллоидной частицы и правил электролитной коагуляции очищенный коллоидный раствор подвергают коагуляции путем действия на него различных электролитов. Полноту очистки коллоидного раствора проверяют проведением качественной реакции на хлорид-ионы, проходящие из диализатора во внешний сосуд. Растворы электролитов для исследования процесса коагуляции… Читать ещё >
Экспериментальная часть. Получение, очистка и исследование процесса коагуляции коллоидного раствора (реферат, курсовая, диплом, контрольная)
Приборы и реактивы:
электрическая плитка;
коническая колба для получения коллоидного раствора;
раствор для получения золя: 2% FeCl3;
дистиллированная вода;
диализатор;
раствор AgNO3 для проведения качественной реакции на хлорид-ионы;
три бюретки, заполненные растворами 4,0 моль-экв/л NaCl, 0,01 моль-экв/л Na2SO4, 0,001 моль-экв/л K3 [Fe (CN) 6].
три штатива с пробирками для исследования процесса коагуляции;
растворы электролитов для исследования процесса коагуляции: 0,1 М KF, 0,0025 М K2S04, 0,001 М K3 [Fe (CN) 6], 1,0 М КС1, 0,01 MCdCl2, 0,005 МА1С13.
Xoд работы.
1. Получение золя гидроксида железа (III).
Золь гидроксида железа (III) получают гидролизом хлорида железа (III).
FeCl3 + 3H2O > Fe (OH) 3 + ЗHCl.
В конической колбе нагревают до кипения 85,0 мл дистиллированной воды. К кипящей воде, отключив электроплитку, постепенно приливают 15,0 мл 2% -ого раствора FeCl3. Получают золь гидроксида железа красно-коричневого цвета.
Знак заряда коллоидных частиц в определяют методом капиллярного анализа.
Знак — положительный Строение мицеллы полученного золя можно изобразить следующим образом:
{ [Fe (OH) 3 • nFeO+] n+ • (n-x) Cl-}x+ • xCl-
2. Очистка коллоидного раствора Полученный коллоидный раствор гидроксида железа подвергают очистке методом диализа. В диализатор, сосуд из полупроницаемой мембраны, наливают полученный раствор гидрозоля; диализатор помещают в широкий стакан, наполовину наполненный дистиллированной водой. При многократном опускании и поднимании диализатора в воде происходит очистка гидрозоля: загрязняющие золь ионы переходят через мембрану в воду, а очищенный коллоидный раствор остается в диализаторе. В процессе диализа воду во внешнем сосуде (стакане) меняют 3−4 раза.
Полноту очистки коллоидного раствора проверяют проведением качественной реакции на хлорид-ионы, проходящие из диализатора во внешний сосуд.
Сl - + AgNO3 > AgCl v +NO3
Диализ заканчивают, когда качественная реакция на хлорид-ионы дает отрицательный результат.
3. Исследование процесса коагуляции коллоидного раствора.
Для проверки правильности предположения о заряде коллоидной частицы и правил электролитной коагуляции очищенный коллоидный раствор подвергают коагуляции путем действия на него различных электролитов.
Предварительно записывают формулу мицеллы гидрозоля и определяют знак заряда коллоидной частицы. Поскольку коллоидный раствор имеет положительно заряженные коллоидные частицы, то коагуляцию должны вызывать анионы, причем, тем быстрее, чем выше заряд аниона.
В каждую из четырех конических колб приливают по 10,0 мл полученного и очищенного раствора гидрозоля железа.
коагуляция коллоидный раствор гидроксид Заполняют три бюретки растворами электролитов: 4,0 моль-экв/л NaCl, 0,01 моль-экв/л Na2SO4 и 0,001 моль-экв/л K3 [Fe (CN) 6], устанавливают объем электролитов в бюретке на нулевой отметке. В каждую из трех колб с золем приливают растворы электролитов из бюреток по каплям до появления первых признаков коагуляции (появления мути, изменения цвета золя и др.). Отмечают объем электролита, пошедшего на коагуляцию. Четвертая пробирка с золем является контрольной.
4. Расчеты.
Электролит-коагулятор | NaCl. | Na2SO4 | K3 [Fe (CN) 6]. |
Исходная концентрация электролита С1, моль-экв/л. | 4,0. | 0,01. | 0,001. |
Объем электролита, вызвавшего коагуляцию золя V1, мл. | 12,5. | 8,2. | 8,7. |
Объем электролита V2, пересчитанный на концентрацию 0,001 моль-экв/л, мл. | 8,7. | ||
lgV2 | 4,70. | 2,91. | 0,94. |
Валентность иона-коагулятора, z. | |||
Порог коагуляции, г. | 0,082. | 0,0085. |
1. Вычисление порога коагуляции:
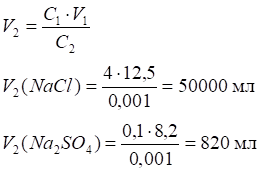
2. Пересчет объемов электролита на одинаковую концентрацию:
С1V1=C2V2
3.
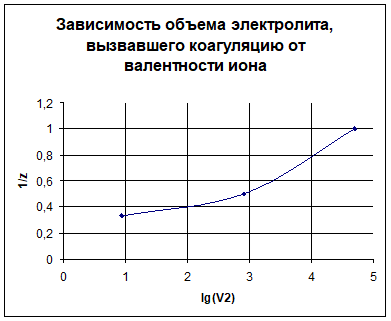
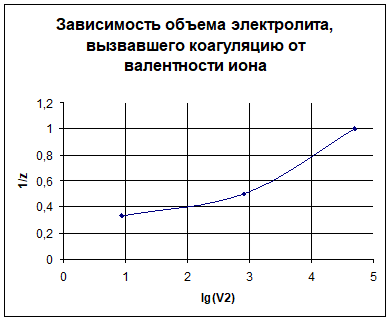
5. Вывод правила значности:
г1: г2: г3 = 5: 0,082: 0,0085 = 588: 10: 1.