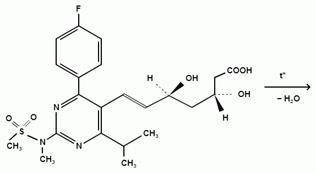
Розувастатин — (Rosuvastatin)

Метаболизм Биотрансформируется в печени в небольшой степени (около 10%), являясь непрофильным субстратом для изоферментов системы цитохрома Р450. Как и в случае других ингибиторов ГМГ-КоА-редуктазы, в процесс печеночного захвата препарата вовлечен специфический мембранный переносчик — полипептид, транспортирующий органический анион (ОАТР) 1В1, выполняющий важную роль в его печеночной элиминации… Читать ещё >
Розувастатин — (Rosuvastatin) (реферат, курсовая, диплом, контрольная)
ИЮПАК: 3R, 5S, 6E) — 7 — [4- (n-Фторфенил) — 6-изотропил-2- (N-Метилметансульфонамидо) — 5-пиримидинил] - 3,5-дигидрокси-6-гептеноевая кислота.
МНН: Розувастатин.
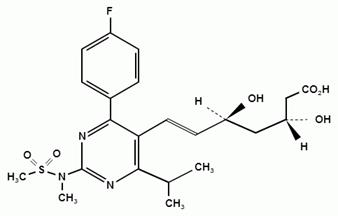
Получение и очистка розувастатина:
Розувастатин обычно производят, в соответствии с опубликованным патентом ЕР 521 471, из натриевой соли (E) — 7 — [4- (4-фторфенил) — 6-изопропил-2 — [метил (метилсульфонил) амино] пиримидин-5-ил] (3R, 5S) — 3,5-дигидрокси-6-гептеновой кислоты и подходящей водорастворимой соли кальция, пред-почтительно из хлорида кальция.
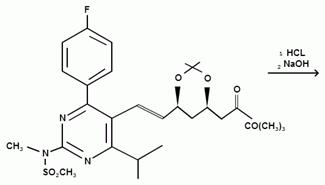
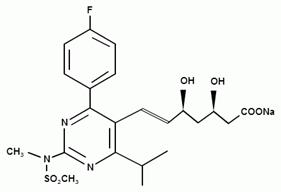
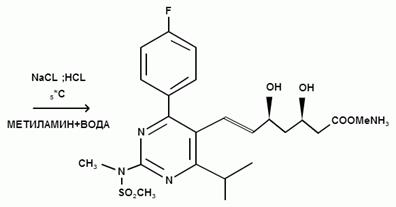
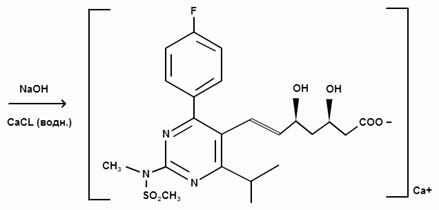
Исходная натриевая соль может быть получена согласно вышеупомянутому патенту из трет-бутил- (Е) — (6 — [2 — [4- (4-фторфенил) — 6-изопропил-2 [метил (метилсульфонил) амино] пиримидин-5-ил] винил] (4R, 6S) — 2,2-диметил — [1,3] диоксан-4-ил) — ацетата путем гидролиза в растворе гидроксида натрия в этиловом спирте.
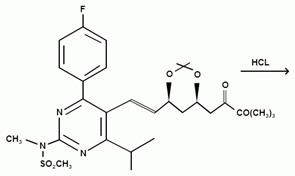
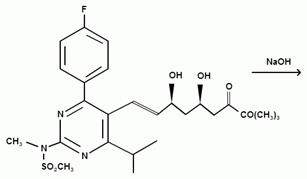
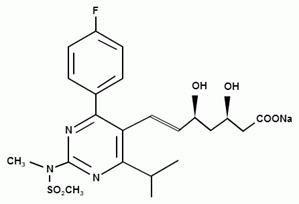
Этот промежуточный продукт сначала превращают в соответствующую натриевую соль путем последовательного перемешивания сначала с соляной кислотой, а затем с гидроксидом натрия. Затем, добавляя хлорид кальция к водному раствору натриевой соли, получают кальциевую соль.
Торговое название:
Крестор, Акорта, Мертенил, Розувастатин, Розувастатин кальция, Розувастатин Канон, Розукард. Розулип, Роксера, Тевастор.
Таблица.
Действующие вещества. | Вспомогательные вещества. | Кинетические особенности. | |
Крестор (Crestor) оригинальный препарат. | Розувастатин кальция. | Вспомогательные вещества: лактозы моногидрат —, целлюлоза микрокристаллическая, кальция фосфат, кросповидон, магния стеарат. Состав оболочки: лактозы моногидрат, гипромеллоза, триацетин (глицерола триацетат), титана диоксид, краситель железа оксид красный. | Всасывание Cmax розувастатина в плазме крови достигается приблизительно через 5 ч после приема препарата внутрь. Абсолютная биодоступность — примерно 20%. Системная экспозиция розувастатина увеличивается пропорционально дозе. Фармакокинетические параметры не изменяются при ежедневном приеме. Распределение Розувастатин накапливается преимущественно в печени. Vd — примерно 134 л. Связывание с белками плазмы (преимущественно с альбумином) составляет приблизительно 90%. Метаболизм Розувастатин подвергается ограниченному метаболизму (около 10%) в печени. Является непрофильным субстратом для изоферментов системы цитохрома Р450. Основным изоферментом, участвующим в метаболизме розувастатина, является CYP2C9. Изоферменты CYP2C19, CYP3A4 и CYP2D6 вовлечены в метаболизм в меньшей степени. Основными выявленными метаболитами розувастатина являются N-дисметил и лактоновые метаболиты. N-десметил примерно на 50% менее активен, чем розувастатин, лактоновые метаболиты фармакологически неактивны. Более 90% фармакологической активности по ингибированию циркулирующей ГМГ-КоА-редуктазы обеспечивается розувастатином, остальное — его метаболитами. Выведение Около 90% дозы розувастатина выводится в неизмененном виде с калом. Оставшаяся часть выводится с мочой. Плазменный T½ — примерно 19 ч. T½ не изменяется при увеличении дозы препарата. Среднее значение плазменного клиренса составляет приблизительно 50 л/ч (коэффициент вариации 21.7%). Как и в случае других ингибиторов ГМГ-КоА-редуказы, в процесс печеночного захвата розувастатина вовлечен мембранный переносчик Хс, выполняющий важную роль в печеночной элиминации розувастатина. |
Розукард. (Rosucard). | Розувастатин. | Вспомогательные вещества: лактозы моногидрат, целлюлоза микрокристаллическая, кроскармеллоза натрия, кремния диоксид коллоидный, магния стеарат. Состав пленочной оболочки: гипромеллоза, макрогол, титана диоксид, тальк, краситель железа оксид красный. | Всасывание Максимальная концентрация (Сmax) розувастатина в плазме крови достигается приблизительно через 5 ч после приема препарата. Абсолютная биодоступность — примерно 20%. Системная экспозиция розувастатина увеличивается пропорционально дозе. Фармакокинетические параметры не изменяются при ежедневном приеме. Распределение Проникает через плацентарный барьер. Розувастатин поглощается приемущественно печенью, которая является основным местом синтеза ХС и метаболизма ХС-ЛПНП. Объем распределения — 134 л. Связывание с белками плазмы (преимущественно с альбумином) составляет приблизительно 90%. Метаболизм Биотрансформируется в печени в небольшой степени (около 10%), являясь непрофильным субстратом для изоферментов системы цитохрома Р450. Как и в случае других ингибиторов ГМГ-КоА-редуктазы, в процесс печеночного захвата препарата вовлечен специфический мембранный переносчик — полипептид, транспортирующий органический анион (ОАТР) 1В1, выполняющий важную роль в его печеночной элиминации. Основным изоферментом, участвующим в метаболизме розувастатина, является CYP2C9. Изоферменты CYP2C19, CYP3A4 и CYP2D6 вовлечены в метаболизм в меньшей степени. Основными метаболитами розувастатина являются N-дисметил и лактоновые метаболиты. N-дисметил примерно на 50% менее активен, чем розувастатин, лактоновые метаболиты фармакологически неактивны. Более 90% фармакологической активности по ингибированию циркулирующей ГМГ-КоА-редуктазы обеспечивается розувастатином, остальное — его метаболитами. Выведение Около 90% дозы розувастатина выводится в неизмененном виде через кишечник, оставшаяся часть — почками. Период полувыведения (Т½) — примерно 19 ч, не изменяется при увеличении дозы препарата. Среднее значение плазменного клиренса составляет приблизительно 50 л/ч (коэффициент вариации 21,7%). У пациентов с легкой и умеренно выраженной почечной недостаточностью плазменная концентрация розувастатина или N-дисметила существенно не меняется. У пациентов с выраженной почечной недостаточностью (клиренс креатинина (КК) менее 30 мл/мин) концентрация розувастатина в плазме крови выше в 3 раза, а N-дисметила — в 9 раз, чем у здоровых добровольцев. Концентрация розувастатина в плазме крови у пациентов, находящихся на гемодиализе, примерно на 50% выше, чем у здоровых добровольцев. У пациентов с баллом 7 и ниже по шкале Чайлд-Пью не выявлено увеличения Т½ розувастатина; у больных с баллами 8 и 9 по шкале Чайлд-Пью отмечено удлинение Т½ в 2 раза. Опыт применения препарата у пациентов с более выраженными нарушениями функции печени отсутствует. |
Мертенил (Mertenil). | розувастатин кальция. | вспомогательные вещества: целлюлоза микрокристаллическая 12, лактозы моногидрат, магния гидроксид, кросповидон (тип А), магния стеарат. Состав пленочной оболочки: Опадрай II белый (тальк, макрогол 3350, титана диоксид (Е171), поливиниловый спирт). | Абсорбция Cmax розувастатина в плазме крови достигается через 5 ч после приема внутрь соответствующей дозы. Абсолютная биодоступность составляет примерно 20%. Распределение Розувастатин поглощается преимущественно печенью, которая является основным местом синтеза Хс и клиренса метаболизма Хс-ЛПНП. Vd розувастатина составляет примерно 134 л.90% розувастатина связывается с белками плазмы крови, в основном с альбумином. Метаболизм Подвергается ограниченному метаболизму (примерно 10%). Розувастатин является достаточно непрофильным субстратом для метаболизма ферментами системы цитохрома Р450. CYP2C9 является основным изоферментом, участвующим в метаболизме, в то время как изоферменты CYP2C19, CYP3A4 и CYP2D6 вовлечены в метаболизм в меньшей степени. Основной метаболит — N-десметил, который на 50% менее активен, чем розувастатин. Лактоновые метаболиты фармакологически неактивны. Более 90% фармакологической активности по ингибированию циркулирующей ГМГ-КоА-редуктазы обеспечивается розувастатином, остальное — его метаболитами. Выведение Примерно 90% от принимаемой дозы розувастатина выводится в неизмененном виде из организма через кишечник (включая абсорбированный и не абсорбированный розувастатин), а оставшаяся часть выводится в неизмененном виде почками. T½ составляет 19 ч, не изменяется при увеличении дозы препарата. Средний геометрический плазменный клиренс составляет приблизительно 50 л/ч (коэффициент вариации 21.7%). Как и в случае с другими ингибиторами ГМГ-КоА-редуктазы, в процесс «печеночного» захвата розувастатина вовлечен мембранный переносчик холестерина через мембраны — транспортный протеин С органических анионов. Данный переносчик играет большую роль в выведении розувастатина печенью. |
Примечание: Розувастатин является синтетическим статином III генераци.
Выраженный ХС-снижающий эффект розувастатина связан и с продолжительным периодом его полувыведения (19 ч), что позволяет длительно блокировать активность ключевого фермента биосинтеза ХС. Розувастатин — один из немногих статинов, под влиянием которого активизируется синтез основного белка ЛПВП — аполипопротеина (апо) АI: он повышается на разных дозах от 5 до 15%. Препарат применяется в дозах 5−40 мг. Стартовая доза 5−10 мг. Терапевтический эффект розувастатина появляется в течение 1 нед. после начала терапии, через 2 нед. лечения достигает 90%. Максимальное действие препарата регистрируется обычно к 4-й нед. и поддерживается при постоянном приеме.
Методика анализа:
Получение исходного, стандартные и испытуемые растворы:
Исходный раствор (500 мкг / мл) розувастатина кальция, был подготовлен путем отмеривания 25 мг испытуемого вещества в 50 мл мерную колбу и добавлением 20 мл смеси воды и ацетонитрила. Смесь обрабатывают ультразвуком в течение 2 мин, чтобы растворить розувастатин кальций, и раствор затем разбавляли до объема с той же смесью растворителей. Стандартный раствор (50 мкг / мл), полученного разбавлением 5 мл стандартного раствора до 50 мл, в мерную колбу с той же смесью растворителей.
Для подготовки исходного раствора (500 мкг / мл) для анализа 20 таблеток взвешивают и перемешивают. Аликвоту порошок эквивалентной массой 5 таблеток точно взвешивали и переносили в 100 мл мерную колбу. Вода-ацетонитрил, 60 мл, добавляли в колбу и смесь обрабатывали ультразвуком в течение 10 мин. Содержимое колбы затем оставляют остыть до комнатной температуры и разбавили до объема той же смеси растворителей. Этот раствор (10 мл), фильтровали через 0,45-мкм фильтр шприца нейлона.
Двадцать таблеток взвешивали и рассчитывали среднюю массу таблетки использовали для анализа расчета.
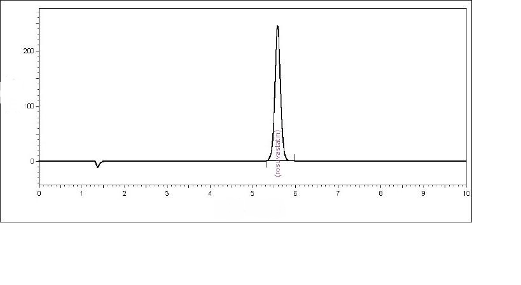
Рис. 4. Хроматограмма необработанных препаратов в растворе таблетка (50 мкг / мл).
Исследования деградации:
Для выполнения принудительной деградации исследовании 50 мг препарат был подвергнут воздействию кислотных, щелочных, окислительная, тепловые и фотолитических условиях.
Для кислотной деградации препарат нагревают с обратным холодильником с 0,1 М HClпри 80*в течении 2 ч и нейтрализуют смесь.
Для щелочной деградации препарата обрабатывали 0,1 М NaOH при 80 є течение 2 ч и смесь нейтрализовали.
Для деградации в окислительных условиях препарат нагревают с обратным холодильником 6% H 2 O 2 при 80° в течение 2 часов Для термической деградации порошкообразный препарат был выставлен на 70° в течение 48 час.
Для фотолитическим деградация порошкообразный препарат подвергается воздействию солнечного света в течение 48 часов.
Плацебо также подвергали же стресс условия, чтобы определить, какие пики возникло от заявленной наполнителями. После завершения процедуры решения остались до комнатной температуры и разбавляли вода-ацетонитрил (50: 50) с получением 50 мкг / мл растворов. Чистоту препарата пик, полученный от напряженного образца измеряли с использованием КПК детектора.
Рис. 5. Хроматограмма ускоренный распад исследования профилей розувастатина таблеток после применения к ним (а) кислые, (б) щелочной, (в) окислительные, (г) тепловой и (е) фотолитических деградации.
Точность:
Точность оценивали путем определения восстановление методом при трех различных концентрациях (соответствующий 50, 100 и 150% от концентрации теста раствор) путем добавления известных количеств стандартных с плацебо препарата. Для каждой концентрации, три набора были подготовлены и вводили в двух экземплярах.
Надежность:
Надежность метода оценивалась путем анализа испытуемые растворы после небольших, но преднамеренных изменений в условиях анализа. Фактор выбран для этого исследования было расход (± 0,1 мл / мин), подвижной фазы (ацетонитрил-вода, 38: 62 и 42: 58), и с использованием другой партии колонки ВЭЖХ.
Стабильность раствора:
Стабильность в растворе оценивали по стандартным раствором и тестируемого препарата. Растворы хранили при 5° и при температуре окружающей среды без защиты от света и испытывают после 12, 24, 36 и 48 час. Ответы для престарелых решения были оценены по сравнению с свежеприготовленных растворов.
Длина волны детекции 242 нм была выбрана после сканирования стандартного раствора в диапазоне 190−370 нм с использованием КПК детектора. Детекция при 242 нм в результате хорошей реакции и хорошей линейности.
Хранение розувастатина:
В недоступном месте для детей. При температуре не выше 30*С.