Осветленная и умягченная вода

Пропуск осветленной воды через механический фильтр снижает концентрацию взвешенных веществ (шлама) до 1 мг/л и предупреждает случайные забросы шлама из осветлителя. После Na-катионитных фильтров уменьшается общая жесткость воды до величины остаточной жесткости — ЖoNa=0,1 мг-экв/л. При этом в воду поступает эквивалентное удаленному количество Na+, мг-экв, согласно уравнению химической реакции… Читать ещё >
Осветленная и умягченная вода (реферат, курсовая, диплом, контрольная)
Принципиальная схема предочистки и умягчения воды может быть представлена по рис. 8.
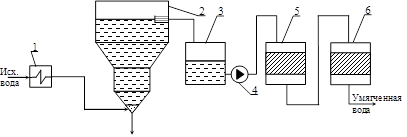
Рис. 8. Принципиальная схема осветления и умягчения воды: 1 — подогреватель сырой (исходной) воды; 2 — осветлитель; 3 — бак осветленной воды; 4 — насос подачи осветленной воды на механические фильтры; 5 — механические фильтры; 6 — Na-катионитные фильтры
В подогревателе 1 исходная вода подогревается до температуры 30ч50 єС для ускорения химических реакций. В осветлителе производится коагуляция коллоидных (органических) примесей и удаление шлама и грубодисперсных (взвешенных) примесей. Обычно при ЩО > 2 мг-экв/л рекомендуется наряду с коагуляцией производить известкование воды в осветлителе 2 в целях снижения щелочности (или всех форм углекислоты) в воде. Обычно при этом уменьшается общая жесткость и кремнесодержание воды. Переливом вода из осветлителя поступает в бак осветленной воды 3, откуда насосом 4 прокачивается через механические 5 и Na-катионитные фильтры 6. При этом из воды удаляется «проскочивший» из осветлителя шлам и удаляются катионы накипеобразователи (Ca2+, Mg2+) в обмен на Na+из катионита. Умягченная вода накапливается в баке и расходуется на технологические нужды, в том числе, на питание установок обратного осмоса в целях обессоливания.
В рассматриваемом примере щелочность природной воды по табл. 4 равна 2,6 мг-экв/л, т. е. более 2 мг-экв/л, и в этом случае рекомендуется совмещение коагуляции воды с ее известкованием в осветлителе. Принципиальная схема осветлителя для коагуляции с известкованием приведена на рис. 9.
В качестве коагулянта используется обычно сульфат железа (II), кристаллогидрат которого имеет химическую формулу FeSO4?7H2O. Известь вводится в виде известкового молока — суспензии Ca (OH)2 в воде. В ряде случаев используется насыщенный раствор Ca (OH)2, чтобы избежать процесса растворения твердого Ca (OH)2 и ускорить химические реакции.
Химические реакции, протекающие в воде при известковании, изложены в книге Чебанова С. Н. и Ларина Б. М. «Водоподготовка и водный режим тепловых электростанций», гл. 5, с. 81 — 89. Там же на с. 322 — 324 приведены расчетные уравнения для определения требуемой дозы извести и коагулянта, количества и качества образующегося щлама. Показатели качества осветленной воды при разных схемах осветления воды могут быть определены по табл. 6.
Таблица 6. Показатели качества осветленной воды после разных схем предочистки
Показатель. | — М; | — К-М; | — К-И-М; | — К-И-С-М; | |
Остаток коагулянта, мг/л. | ; | <0,2. | <0,1. | <0,1. | |
Снижение окисляемости, %. | 50−75. | 40−50. | 40−50. | ||
Снижение содержания кремниевой кислоты, %. | 10−20. | 30−40. | 30−40. | ||
Свободная углекислота, мг/л. | +Dк | ||||
Щелочность общая, мг-экв/л: гидратная карбонатная бикарбонатная. |
| — Dк
— Dк |
|
| |
Жесткость общая, мг-экв/л, в т. ч. Жнк ЖMg | +Dк
|
| |||
Сульфаты, мг-экв/л. | + Dк | + Dк | + Dк | ||
Взвешенные в-ва, мг/л. | |||||
Прозрачность «шрифт», см. | |||||
рН. | рНисх | рНисх-(0,1ч0,5). | 9,5−10,5. | 9,5−10,5. | |
Солесодержание, мг/л. | Sисх | Sисх +ЭкDк | Sисх-Эк· Dк-50·Що-3,5·Ок. | ||
Примечание. исх — соответствует концентрации такого показателя в исходной воде; ос — соответствующий концентрации такого показателя в осветленной воде; Эк — эквивалент коагулянта; Дк — доза коагулянта, мг-экв/л; Ок — окисляемость исходной воды, гО/л. | |||||
- 1. В рассматриваемом здесь примере при дозе коагулянта Дк=0,07•Ок=0,07•8,3=0,6 мг-экв/л показатели качества осветленной воды будут следующими:
- — окисляемость — Окосв=0,5•8,5=4,25 мгО/л;
- — щелочность: общая ЩО=0,8 мг-экв/л;
гидратная ЩГ=0,2 мг-экв/л;
карбонатная ЩК=0,6 мг-экв/л;
— жесткость общая.
Жоосв=Щоосв+ЖНКисх+ДК=0,8+2,14+0,5=3,44 мг-экв/л;
— сульфаты.
[SO42-]осв=[SO42-]исх + ДК=1,94+0,5=2,44 мг-экв/л;
- — взвешенные вещества — 2 мг/л;
- — рН — 10 ед. рН;
- — натрий — 0,3мг-экв/л;
- — хлориды — 0,2 мг-экв/л;
- -ЖоОсв = ЩоОсв + Жнк + Дк = 0,8+???+0,5=2,4 мг-экв/л
- — Ж Са2+осв = Жоосв— Ж Mg2+осв =3,44 — 0,69=2,75 мг-экв/л;
- — Ж Mg2+осв =0,5•Ж Mg2+исх=0,5•1,38=0,69 мг-экв/л.
Проверка ионного состава примесей по уравнению электронейтральности дает ошибку:
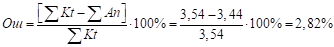
Расчетная (требуемая) величина дозы извести, вводимой в обрабатываемую воду (Дитр,.
мг-экв/л), определяется по уравнению.
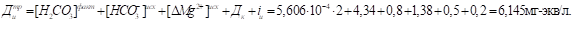
при выражении всех концентраций в мг-экв/л.
При этом избыток извести (iи) можно принять равным гидратной щелочности осветленной.
воды (Щг): iи= Щг=0,2 мг-экв/л.
Величину =0,8• мг-экв/л.
Количество образующегося в осветлителе осадка, мг/л.
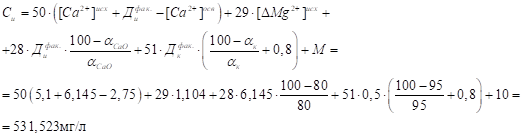
где СаО — содержание окиси кальция в технической извести, % от общей массы; М — содержание механических примесей, мг/л; к — содержание коагулянта FeSO4 в техническом продукте, % от общей массы; [Са2+]исх, [Са2+]осв — концентрация катионов кальция в исходной и в осветленной воде, мг/л;
— фактическая доза извести, мг-экв/л,.
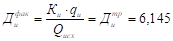
мг-экв/л, Здесь Ки — концентрация извести в баках-мерниках, г-экв/л;
qи — расход рабочего раствора известкового молока в осветлителе, л/ч;
Qисх — расход воды через осветлитель, м3/ч.
Основной характеристикой химического состава шлама, показывающей отношение Mg (OH)2/СаСО3, является м. Оптимальные значения м составляют от 0,050,1 до 0,20,25.
Расчетом параметр м определяется как:
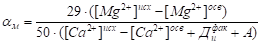
.
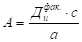
где (а — масса Са (ОН)2 в известковом молоке, мг/л; с — количество СаСО3 в известковом молоке, мг/л; можно принять с/а=0,05).
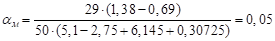
Пропуск осветленной воды через механический фильтр снижает концентрацию взвешенных веществ (шлама) до 1 мг/л и предупреждает случайные забросы шлама из осветлителя. После Na-катионитных фильтров уменьшается общая жесткость воды до величины остаточной жесткости — ЖoNa=0,1 мг-экв/л. При этом в воду поступает эквивалентное удаленному количество Na+, мг-экв, согласно уравнению химической реакции ионного обмена:
2NaR+Ca2+ CaR2+2Na+.
Таким образом для нашего случая в фильтрате Na-катио-нитного фильтра имеем:
Жo=0,1 мг-экв/л; [Na+]=0,3+2,75=3,05 мг-экв/л.
Концентрации других ионных примесей остаются неизменными. Если требуется более глубокое удаление из воды катионов кальция и магния, то применяют 2-ю ступень умягчения воды на Na-катионитных фильтрах, что позволяет снизить общую жесткость воды до 0,01 мг-экв/л. Концентрации примесей в воде при ее осветлении и умягчении приведены в табл. 7.
Таблица 7. Показатели качества воды по стадиям обработки
Стадия обработки. | Жо,. мг-экв/л. | Концентрация ионов,. мг-экв/л. | Що,. мг-экв/л. | рН. | Взв. в-ва, мг/л. | Ок, мгО/л. | |||
Na+ | SO42- | Cl- | |||||||
|
|
|
|
|
|
|
<1. <1. |
| |