Химические основы Клаус-процесса

Клаус-процесс с разделенным потоком Разветвленный способ (одна треть — две трети) применяется при содержании сероводорода в кислых газах 5−15% об. По этой схеме одна треть кислого газа подвергается сжиганию с получением сернистого ангидрида, а две трети поступают на следующий этап, минуя печь-реактор. В первой каталитической ступени процесса серу получают при взаимодействии сернистого ангидрида… Читать ещё >
Химические основы Клаус-процесса (реферат, курсовая, диплом, контрольная)
Сущность процесса Клауса заключается в переработке сероводородного газа в серу по окислительному методу с применением двух-трех каталитических ступеней. Термическая стадия заключается в высокотемпературном сжигании сероводорода в топке котла-утилизатора при подаче стехиометрического количества воздуха и протекает при температуре в интервале 1000−1300 °C согласно реакции:
2Н2S + О2 2H2O + S2 + Q.
В топочной части печи-реактора протекают следующие целевые реакции:
Н2S + ½О2 SO2 + H2O;
2Н2S + SO21,5S2 + 2H2O;
СН4 + 2O2CO2 + 2H2O.
На каталитических ступенях процесса при температурах 200−300 °C происходит взаимодействие Н2S и SО2, непрореагировавших на термической ступени, с образованием элементарной серы на катализаторе по реакции:
- 2Н2S + SO2>3/6S6 + 2H2O;
- 2H2S + SO2>3/8S8 + 2H2O.
Для повышения степени извлечения серы из сероводорода на сегодняшний день были разработаны разнообразные модификации процесса по получению серы. Разновидности процесса в зависимости от содержания Н2S в кислом газе представлены в таблице 1.
Таблица 1 — Объемная доля Н2S в кислом газе.
Объемная доля Н2S в кислом газе, %. | Модификация процесса Клауса. | |
50−100. | Прямоточная. | |
20−50. | Разветвленный поток (1/3−2/3). | |
10−20. | Разветвленный поток с предварительным подогревом газа, воздуха или применение воздуха, обогащенного кислородом. | |
<10. | Рециркуляция серы в виде диоксида серы. | |
<5. | Окисление Н2S кислородом на катализаторе. | |
Разнообразие модификаций процесса Клауса обусловлено необходимостью поддержания в реакционной печи температуры выше минимальной температуры 930 °C, так как ниже этой температуры пламя нестабильно, в продуктах реакции появляется кислород, что указывает на низкую скорость протекания реакции. Для газов, содержащих 50% об. сероводорода и более, необходимая температура в реакционной печи достигается по прямоточной схеме в отличие от газов с низкой концентрацией сероводорода, для которых применяется разветвленная схема. Это связано с тем, что значительная часть теплоты расходуется в первую очередь на нагрев разбавителей — двуоксид углерода и азот. По разветвленной схеме через термическую ступень пропускают 1/3 сероводорода, а 2/3 направляют непосредственно на каталитическую ступень. Таким образом, поддерживают соотношение Н2S: SО2 равным 2:1, что требуется по реакциям Клауса.
Модификации Клаус-процесса Сероводородные газы, образующиеся в процессе очистки углеводородных газов от кислых компонентов, обычно перерабатываются в серную кислоту иди элементарную серу. Для утилизации сероводородного газа в элементарную серу обычно применяется хорошо известный в мировой практике процесс Клауса или его различные модификации.
Выбор промышленной схемы процесса Клауса, определяется содержанием сероводорода в кислых газах, подлежащих переработке, а также наличием в них посторонних компонентов.
Условие при выборе схемы — необходимость обеспечения устойчивого пламенного горения сероводорода в реакционной печи. При содержании сероводорода в кислом газе более 50% использую классическую схему процесса Клауса. Если содержание сероводорода в кислых газах менее 50%, гомогенное горение его в реакционной печи при H2S: O2 = 2 становится неустойчивым, в связи с чем применяют иную схему процесса.
Клаус-процесс с разделенным потоком Разветвленный способ (одна треть — две трети) применяется при содержании сероводорода в кислых газах 5−15% об. По этой схеме одна треть кислого газа подвергается сжиганию с получением сернистого ангидрида, а две трети поступают на следующий этап, минуя печь-реактор. В первой каталитической ступени процесса серу получают при взаимодействии сернистого ангидрида с сероводородом, содержащимся в остальной части (2/3) исходного кислого газа. Выход серы составляет 94−95%. В печи-реакторе разветвленного процесса Клауса осуществляется окисление сероводорода до сернистого ангидрида по реакции:
H2S + 1,5O2 > H2O + SO2.
Затем оставшиеся две трети сероводорода, которые, минуя печь, подаются в смеситель, а затем в каталитический реактор, взаимодействуют на катализаторе с полученным в печи-реакторе сернистым ангидридом с образованием серы: 2H2S + SO2 > 3/nSn + 2H2O. Разветвленный процесс Клауса (треть — две трети) с предварительным подогревом кислого газа и (или) воздуха используется при содержании сероводорода в кислом газе 20−30%, когда при использовании схемы треть — две трети минимально допустимая температура в топке печи-реактора (930 °С) не достигается. Эта схема отличается тем, что для достижения требуемой температуры в печи-реакторе кислый газ и воздух подогревают в теплообменниках перед подачей в реакционную печь. Разветвленный процесс Клауса не отвечает требованиям охраны окружающей среды. Степень конверсии здесь достигает лишь 94−95%.
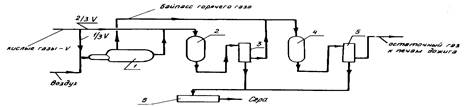
1 — нагреватель кислых газов; 2, 4 — реактор; 3 — конденсатор-холодильник; 5 — конденсатор-охладитель; 6 — приемник серы Рисунок 1 — Схема потоков установки по методу Клауса разделенными параллельными потоками Процесс «Суперклаус».
Экологические требования диктуют необходимость доочистки отходящих газов. В настоящее время в мировой нефтепереработке широкое распространение получил процесс «Суперклаус-99» (разработан фирмой «Компримо» (Нидерланды)). Процесс Суперклаус-99 включает следующие стадии:
- — термическое превращение;
- — три стадии каталитического превращения с промежуточным выводом серы.
Процесс Суперклаус был разработан для извлечения элементарной серы из газов с содержанием H2S, которые поступают с установок очистки газа. Современные установки Суперклаус также способны перерабатывать газы с содержанием H2S/NH3, которые поступают с отпарки кислых стоков, с целью извлечения общей серы с выходом до 99,0% без какой-либо доочистки хвостовых газов.
Стандартный двухконверторный процесс «Клауса» дополнен реактором окисления на специальном катализаторе. Процесс ведут таким образом — что на выходе из второго конвертора в газах содержится только сероводород в количестве 0,8−1,5%, который окисляется на специальном катализаторе в реакторе Суперклауса.
Первые два или три реактора заполнены стандартным катализатором Клауса, в то время как последний реактор заполнен катализатором селективного окисления (оксид железа с модифицирующей добавкой из оксида фосфора). На стадии термического превращения происходит горение кислого газа с субстехиометрическим количеством регулируемой подачи воздуха горения таким образом, что отходящий газ, покидающий последний реактор Клауса, обычно содержит от 0,8−1,0% об. H2S.
Катализатор Суперклаус в последнем реакторе окисляет H2S до серы с выходом более чем 85%. Однако вследствие того, что катализатор Суперклаус не окисляет H2S до SO2 и H2O и не производит обратной реакции серы и воды до образования H2S и SO2, извлечение общей серы и воды до образования с выходом до 99% может быть достигнуто в трехреакторной системе.
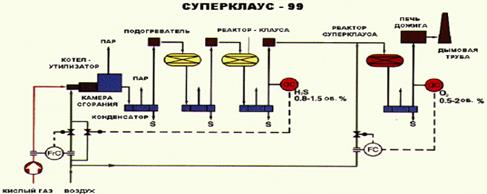
Рисунок 2 — Принципиальная схема процесса Суперклаус-99.
В том случае если необходимо добиться извлечения серы с выходом более чем 99% устанавливается дополнительная реакторная ступень. Для достижения такой глубины отбора в схему Суперклаус-99 добавлена ступень гидрирования. Схема процесса Суперклаус-99,5 состоит из термической ступени, двух реакторов Клауса, реактора гидрирования (работает на никелевом катализаторе) и реактора селективного окисления.
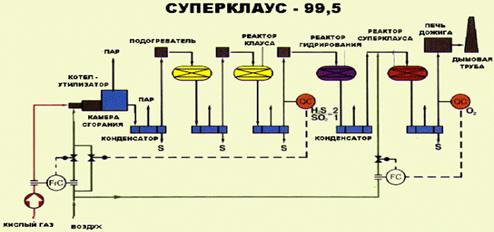
Рисунок 3 — Принципиальная схема процесса Суперклаус-99,5.
Поскольку новый селективный катализатор не чувствителен к воде, отпадает необходимость конденсации воды после реактора гидрирования, типичная почти для всех вариантов процесса Клауса. Газ из реактора гидрирования охлаждается по линии оптимальной температуры на входе в реактор селективного окисления, отпадает также необходимость в термической ступени, так как все сернистые компоненты и пары серы превращаются в сероводород в реакторе гидрирования, и реакторы 1 и 2 могут работать при избыточном содержании сероводорода и отношении H2S/SO2 = 2/1. Желаемая гибкость и в этом варианте процесса достигается введением избытка воздуха в реактор селективного окисления сероводорода.
Процесс может применяться как на вновь строящихся, так и на действующих установках Клауса. Благодаря простоте процесса и аппаратурного оформления дополнительные капитальные затраты (по сравнению с затратами на обычную установку Клауса) незначительны.
Процесс «Селектокс».
В процессе «Селектокс» газ гидрирования после охлаждения и отделения конденсационной воды нагревается и окисляется кислородом воздуха в серу на твердом катализаторе «Селектокс». Суммарная степень извлечения серы 98,5−99,5%; капитальные затраты 45−50% (от капитальных затрат на установку Клауса).
Кислый газ, поступающий на установку, подается в смеси с воздухом на подогрев и далее в термокаталитический реактор, где проводится реакция прямого окисления сероводорода. Традиционный катализатор прямого окисления сероводорода не может эксплуатироваться при температуре выше 350? С, и поскольку разогрев пропорционален концентрации сероводорода, в процессе используется разбавление исходного газа продуктами реакции.
Когда требуется более высокая степень конверсии, процесс доукомплектовывается одной или двумя каталитическими ступенями. Используемое для этого оборудование и принцип работы каталитических ступеней не отличаются от традиционных.
Как правило, в реакторе используется катализатор прямого окисления марки BSR. Оптимальная объемная доля сероводорода во входном потоке для этого катализатора — от 2 до 4%.
Использование реактора позволяет достичь степени конверсии сероводорода 94−97%. К недостаткам процесса следует отнести его низкую эффективность в случае присутствия углеводородов (особенно ароматических) в кислом газе. Это связано с тем, что кислый газ не проходит предварительную огневую обработку, и в результате крекинга углеводородов на поверхности катализатора откладывается углерод, снижающий эффективность процесса.
Это метод используется при переработке в серу сероводородсодержащих кислых газов с небольшой производительностью и концентрацией сероводорода менее 40%. Процесс отличается гибкостью и легкостью управления. Это позволяет рекомендовать данный процесс при освоении малых газовых месторождений.
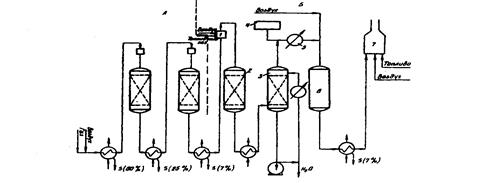
А — секция установки Клауса; Б — секция процесса БСР/селектокс;
1 — генератор газа-восстановителя; 2 — реактор получения водорода; 3 — реактор с катализатором БСР; 4 — анализатор; 5 — конденсатор; 6 — реактор с катализатором селектокс; 7 — печь для сжигания отходящих газов Рисунок 5 — Принципиальная схема процесса Селектокс сера газ клаус химический.