Теоретическая часть.
Исследование методов очистки этил-трет-бутилового эфира от примесей серы

Диалкилсульфиды в сырых нефтях не обнаружены, они обычно образуются при окислении меркаптанов в мягких условиях и поэтому присутствуют в бензинах (до 15%). Основная доля серосодержащих соединений нефтей приходится на так называемую «остаточную» серу, не определяемую стандартными методами. В ее составе преобладают тиофены и их производные, поэтому раньше «остаточную» серу называли «тиофеновой… Читать ещё >
Теоретическая часть. Исследование методов очистки этил-трет-бутилового эфира от примесей серы (реферат, курсовая, диплом, контрольная)
Неуклонное повышение требований НТД к остаточному содержанию общей серы в автомобильных бензинах: от 0.1%мас в ГОСТ 2884–77 к 0.05%мас — в ГОСТ Р 51 105−97 (Евро-2) и до 0.015%мас. — в ГОСТ Р 51 866−2002 (Евро-3) с перспективой ужесточения допустимой нормы до 0.005%мас — (в Евро-4) вызывает необходимость совершенствования технологии их получения и очистки [9]. Согласно ТУ 0272−024−151 638−99 допустимое содержание сероводорода в ППФ составляет не более 0.002%мас., а содержание меркаптанов и серооксида углерода не регламентируется. В ББФ в соответствии с ТУ 0272−027−151 638−99 допустимое содержание меркаптановой серы составляет не более 0.015%мас. — для марки, А и не более 0.02%мас. — для марок Б и В. При использовании ББФ в качестве сырья для получения МТБЭ (ЭТБЭ) или в процессе алкилирования остаточное содержание меркаптановой серы должно быть не более 0.001%мас. [9].
Таблица 3 Содержание общей и меркаптановой серы в нефтях и газоконденсатах Прикаспийской низменности.
сырье. | Содержание серы %(масс) во фракциях. | ||||||||
62 є. | 28−180 є. | 160−250 є. | 180−350є. | ||||||
Общ. | Меркапта-новая. | Общ. | Меркапта-новая. | Общ. | Меркап-тановая. | Общ. | Меркап-тановая. | ||
Газоконден-сат астра-ханский. | 1,38. | 0,38. | 0,5. | 0,4. | 0,43. | 0,25. | 0,5. | 0,32. | |
Газоконден-сат орен-бурский. | 1,0. | 0,70. | 1,05. | 0,85. | 0,9. | 0,6. | ; | ; | |
Газоконден-сат карача-ганакский. | 0,67. | 0,16. | 0,5. | 0,3. | 0,4. | 0,25. | 0,36. | 0,16. | |
Нефть жана-жольская. | 0,47. | 0,18. | 0,6. | 0,56. | 0,3. | 0,23. | 0,36. | 0,17. | |
Нефть тенгизская. | 0,76. | 0,11. | 0,31. | 0,3. | 0,28. | 0,068. | 0,25. | 0,06. | |
Как видно из таблицы 3, значительная часть серы практически во всех фракциях приходится на долю меркаптановой серы [10].
Сероочистка занимает среди методов, повышающих качество нефти и газоконденсатов, ведущее место, поскольку в нефти содержатся почти все представители серо органики, сероводород и даже сера в чистом виде. В легких фракциях нефти растворены сероводород, меркаптаны и сульфиды. По мере роста температуры кипения углеводородной среды усложняется качественный вид серо органики. Появляются дисульфиды, тиофены и другие мало реакционные сераорганические соединения. Очевидно, что наиболее химически активными соединениями серы являются сероводород и тиолы. Меркаптаны в нефти представлены во всем своем многообразии от метилмеркаптана до высокомолекулярных меркаптанов разветвленного строения, например, изопентантиол или 4,4-диметилгексан-2-тиол [10]. Содержание меркаптанов в нефтях месторождений Восточной Сибири, Прикаспийской низменности и значительного количества новых месторождений высоко. Состав общей и меркаптановой серы в нефтях и газоконденсатах Прикаспийской низменности приведены в таблице 3.
Серосодержащие соединения относятся к наиболее представительной группе гетероатомных компонентов газоконденсатных и нефтяных систем. Общее содержание серы в нефтегазовых системах колеблется в широких пределах: от сотых долей процента до 6−8% (масс.) и более. Высокое содержание общей серы характерно для газоконденсатов Астраханского (1,2%0, Карачаганакского (0,9%) и др. месторождений. Содержание серосодержащих соединений в некоторых нефтях достигает 40% (масс.) и выше, в некоторых случаях нефть почти целиком состоит из них.
В нефтегазовых системах присутствуют незначительные количества неорганических серосодержащих соединений (элементная сера и сероводород), они также могут образоваться как вторичные продукты разложения других серосодержащих соединений при высоких температурах в процессах перегонки, деструктивной переработки.
В отличие от других гетероорганических соединений производные серы имеются в нефти в значительных количествах и в дистилатных фракциях. Как правило, содержание серы в прямогонных фракциях возрастает по мере повышения температуры их кипения и общей сернистости исходной нефти [11, 12, 13, 14].
Сырая нефть — 1,86%, бензиновые фракции — 3,4%.
Фракция 200−300 є - 1,33%.
- -" - 300−350 є - 1,84%
- -" - 350−450 є - 2,57%
- -" - 450−500 є - 3,4%
Среди серосодержащих соединений, найденных в нефти, идентифицированы следующие:
1) алифатические, алициклические и ароматические тиолы (меркаптаны) R-SH:
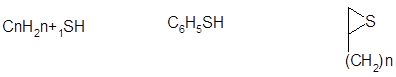
тиолы тиофенолы циклоалканотиолы (n >3).
С6Н5СnH2n+1SH CnH2n+1C6H5SH C10H7SH.
ареноалканотиолы тионафтолы.
2) тиоэфиры (сульфиды) следующих основных типов:
R-S-А C6H5-S-C6H.
тиоалканы, тиоалкены, тиоалкины диарилсульфиды тиоциклоалканы, арилалкилсульфиды арилтиоалканы.
- 3) диалкилдисульфиды R-S-S-R?, где R, R? — алкильные, циклоалкильные или арильные заместители.
- 4) тиофены и их производные, важнейшими из которых являются следующие аренотиофены:
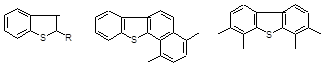
алкилбензотиофены алкилбензонафтотиофены алкилдибензотиофены Распределение различных групп серосодержащих соединений в нефтях и в нефтяных фракциях подчиняется следующим закономерностям [12, 15].
Тиолы содержатся практически во всех сырых нефтях обычно в малых концентрациях и составляют 2−10% (масс.) от общего содержания серосодержащих соединений. В газоконденсатах присутствуют в основном алифатические меркаптаны С1-С3. Некоторые нефти и газоконденсаты и их фракции представляют собой естественные концентраты меркаптанов, примерами которых могут служить бензиновые фракции супергигантского месторождения Прикаспия; фракция 40−200 єС газоконденсата Оренбургского месторождения, содержащая 1,24% (масс.) общей серы, в том числе 0,97% меркаптановой; легкая керосиновая фракция 120−280 єС нефти месторождения Тенгиз, содержащая 45−70% меркаптановой серы от общего содержания серосодержащих соединений. При этом запасы природных тиолов в углеводородном сырье Прикаспийского региона соответствуют уровню их общемирового получения синтетическим путем. Природные тиолы — перспективное сырье для синтеза пестицидов (на основе симметричных триазинов) и одоризации сжиженных газов. Перспективная потребность России в тиолах только для одоризации в настоящее время составляет 6 тыс. т в год [10, 11, 12, 15].
Тиоэфиры составляют до 27% от суммы серосодержащих соединений в сырых нефтях и до 50% - в средних фракциях, в тяжелых вакуумных газойлях содержание сульфидов меньше. Методы выделения нефтяных сульфидов основаны на их способности образовывать комплексные соединения донорно-акцепторного типа за счет передачи неподеленной пары электронов атома серы на свободную орбиталь акцептора. В качестве акцептора электронов могут выступать галогениды металлов, галогеналкилы, галогены. Реакции комплексообразования с нефтяными сульфидами протекают, к сожалению, не селективно; в образовании комплексов могут принимать участие и другие гетероатомные компоненты нефти [11, 12, 13, 15].
Диалкилсульфиды в сырых нефтях не обнаружены, они обычно образуются при окислении меркаптанов в мягких условиях и поэтому присутствуют в бензинах (до 15%). Основная доля серосодержащих соединений нефтей приходится на так называемую «остаточную» серу, не определяемую стандартными методами. В ее составе преобладают тиофены и их производные, поэтому раньше «остаточную» серу называли «тиофеновой». С помощью масс-спектроскопии отрицательных ионов в ней обнаружены ранее не определявшиеся сульфоксиды, сульфоны и дисульфан. В бензиновых фракциях содержание производных тиофена мало, в средних и особенно выкококипящих фракциях оно достигает 50−80% от суммы серосодержащих соединений. Относительное содержание тиофеновых производных, как правило, совпадает со степенью ароматичности нефтяной системы. Трудности, возникающие при выделении серосодержащих соединений (особенно из высококипящих фракций), вызваны близостью химических свойств аренов и тиофенов. Схожесть их химического поведения обусловлена ароматичностью тиофенов, возникающей как результат включения гетероатома серы в р-электронную систему до ароматического секстета. Следствием этого является повышенная склонность нефтяных тиофенов к интенсивному межмолекулярному взаимодействию [1, 15, 16, 17].
Сера, сероводород и меркаптаны в нефтях находятся в небольших количествах и появляются во фракции уже при нагревании до 180−260є за счет разложения сульфидов, дисульфидов.
При температуре 459−650 єС сера взаимодействует с углеводородными газами с образованием сероуглерода и сероводорода:
СН4 + 2S2 > 2H2S + CS2 (3).
В присутствии паров воды образуется только Н2S. При нагревании углеводородов с серой при температуре 220 є происходит дегидрирование с выделением сероводорода:
RH + S2 > H2S + R-CH=CH2 (4).
При температуре 300 є и выше сера взаимодействует с водородом с образованием сероводорода.
При сгорании топлив сера образует высоко коррозионно активный диоксид серы (сернистый ангидрид):
S2 + 2O2 > 2SO2 (5).
В расплавленном состоянии выше 120−130 єС сера взаимодействует со многими металлами и сплавами. Она легко разрушает олово, свинец, медь, в меньшей степени — углеродистую сталь, титан и незначительно алюминий.
Сероводород. Термически устойчив до 1000−1500 єС. Таким образом, сохраняется во всех фракциях. Н2S — газ, реагирует почти со всеми металлами и их оксидами:
H2S + Fe > FeS + H2 (6).
3H2S + Fe2O3 > FeS + 3H2O + FeS2 (7).
Сероводородной коррозии подвержены железо, алюминий, никель, хром, палладий, титан, но наиболее сильно — серебро, медь и их сплавы. В присутствии влаги коррозия начинается при температуре ниже 100 єС. Образующиеся сульфиды играют роль катода по отношению к железу и стали и образуют с ними гальваническую пару с разностью потенциалов 0,2−0,4 в.
Это приводит к быстрому разрушению оборудования в результате образования глубоких язв. Но наиболее опасное действие Н2S — это способность вызывать водородную хрупкость за счет водорода, выделяющегося при взаимодействии с металлами. При этом виде коррозии (сульфидный стресс-крекинг) металл разрушается внезапно без видимых внешних признаков коррозии. Чем тверже сталь, тем она более чувствительна к сульфидной коррозии.
Наиболее интенсивное разрушение наблюдается в интервале 150−250 є, а также при совместном воздействии сероводорода и хлористого водорода.
Все остальные соединения серы по химической активности делятся на 3 группы:
- 1) вещества кислотного типа (меркаптаны, тиолы, сероводород. Содержание меркаптанов 2−10% от общего количества сероорганических соединений. В легких фракциях от 40−50 до 70−75%. С утяжелением фракций их содержание резко падает. И во фракции выше 300 є они практически отсутствуют. Представлены: алкилтиолами с меркаптогруппой при вторичном атоме углерода; тиофенолами; циклоалкилтиолами; ареноалкилтиолами; тионафтолами [12, 14, 17, 18].
- 2) сульфоорганические соединения — сульфиды и дисульфиды, которые в обычных условиях химически нейтральны, но термически нестойки и распадаются с выделением серводорода или меркаптана.
Содержащие серу аналоги спиртов и эфиров называются тиоспиртами R-SH и тиоэфирами R-S-Rґ. Их можно рассматривать как моноалкильные производные сероводорода, который они напоминают по своим качествам. В химическом отношении они обнаруживают сходство со своими кислородными аналогами — спиртами и эфирами. Однако их реакционная способность, особенно по отношению к окислителям, более многообразна.
Тиоспирты (меркаптаны — corpus mеrkurio aptu) легко получаются путем частичного алкилирования сероводорода. Для этой цели на гидросульфид калия при нагревании действуют каким-либо алкилирующим средством, например, галоидалкилом, солью алкилсерной кислоты или диалкилсульфатом [19]. Образующиеся меркаптаны затем отгоняют.
C2H5Cl + KSH > C2H5SH + KCl (8).
C2H5OSO2OK + KSH > C2H5SH + K2SO4 (9).
(CH3)2SO4 + 2KSH > 2CH3SH + K2SO4 (10).
Меркаптаны представляют собой легколетучие вещества: Т кип. первых 6-ти членов этого ряда значительно ниже, чем у соответствующих спиртов. Это явление объясняется меньшей ассоциацией меркаптанов по сравнению со спиртами (метилмеркаптан — газ) [20].
Таблица 4 Температуры кипения различных серосодержащих соединений, входящих в состав нефтей.
Соединение. | Ткип. | Соединение. | Ткип. | |
H2S. | — 61.8. | H2O. | ||
CH3SH. | +5,8. | CH3OH. | 64.5. | |
C2H5SH. | C2H5OH. | |||
перв. С3H7SH. | перв. C3H7OH. | |||
перв. С4Н9SH. | перв. С4Н9ОН. | |||
перв. С5Н11SН. | перв. С5Н11ОН. | |||
Тиоспирты обладают резким неприятным запахом, настолько сильным, что по нему могут быть обнаружены их малейшие количества.
Меркаптаны, как и сероводород, обладают слабыми кислотными свойствами. Водород ихSH группы может замещаться металлом, образуя меркаптиды (соли):
RSH + NaOH > RSNa + H2O (11).
Меркаптаны более сильные кислоты, чем спирты и менее, чем сероводород. С тяжелыми металлами меркаптаны образуют нерастворимые меркаптиды. В отличие от спиртов, меркаптаны легко окисляются [21, 22]. Их можно количественно оттитровать иодом:
2RSH + J2 > R-S-S-R + 2HJ (12).
При этом получаются диалкилсульфиды, образующиеся также при постепенном окислении меркаптанов кислородом воздуха.
В присутствии щелочей и ионов тяжелых металлов скорость окисления повышается. На этой реакции основан принцип удаления тиолов из легких топливных фракций. При t >225 є даже низшие меркаптаны распадаются [22].
>180є.
2RSH ?> 2RH + S2 (13).
> 225є.
2RSH ?> R-S-R + H2S (14).
Cульфиды (тиоэфиры). Наибольшее количество сульфидов находится в средней фракции, где они могут составлять больше половины всех сероорганических соединений. Нефтяные сульфиды делятся на две группы:
1) с атомом серы в открытой цепи — это диалкил-, диарил-, алкиларилсульфиды.
R-S-Rґ, Аr-S-Ar, R-S-Ar;
2) циклические сульфиды или тиоциклоалканы.
Тиоэфиры получают.
- 1) нагреванием сульфидов щелочных металлов с галоидными алкилами:
- 2C2H5J + K2S > (C2H5)2S + 2KJ (15)
- 2) алкилированием меркаптидов щелочных металлов:
С2Н5SK + KOSO2OC2H5 > C2H5-S-C2H5 + K2SO4 (16).
Алкилсульфиды представляют собой нерастворимые в воде жидкости и в совершенно чистом состоянии не обладают неприятным запахом. Они кипят при более высокой температуре, чем соответствующие меркаптаны. Этот факт интересен потому, что простые эфиры, содержащие кислород, в общем значительно более летучи, чем соответствующие им спирты. Явление это связано с тем, что спирты ассоциированы, а простые эфиры — нет. В ряду сернистых соединений не наблюдается значительной ассоциации ни у меркаптанов, ни у тиоэфиров, поэтому между их температурами кипения существует нормальное соотношение: более высокомолекулярные тиоэфиры менее летучи, чем соответствующие простые эфиры [18, 23, 24].
Реакции сернистых соединений В зависимости от строения сернистых соединений — меркаптаны, сульфиды алициклического или циклического строения, дисульфиды и простые тиофены при гидроочистке превращаются в парафиновые или ароматические углеводороды с выделением сероводорода:
1) меркаптаны:
RSH+H2 > RH = H2S (17).
- 2) сульфиды
- а) ациклические:
R-S-А + 2H2› RH + RH + H2S (18).
б) моноциклические :
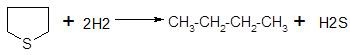
- (19)
- 3) бициклические:

- (20)
- 4) дисульфиды:
RSSR + 3H2 > 2RH + 2H2S (21).
5) тиофены:
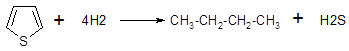
- (22)
- 6) Бензотиофены:
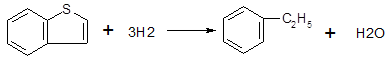
(23).
Процесс сероочистки нефтепродуктов должен быть простым и по возможности дешевым. Этим требованиям отвечает, разработанный компанией «UOP» процесс «MEROX» — окислительно-каталитический способ удаления меркаптанов из керосиновых фракций — демеркаптанизация [25, 27].