Промышленное применение электролиза

Гальванопластика. Это электролитическое осаждение металла на поверхности какого-либо предмета для воспроизведения его формы. Для этого с предмета сначала снимают слепок (из воска или гипса) и покрывают его токопроводящим слоем, например, слоем графита. Подготовленный таким способом предмет помещают в качестве катода в ванну с раствором соли соответствующего металла. При включении тока металл… Читать ещё >
Промышленное применение электролиза (реферат, курсовая, диплом, контрольная)
Электролизимеет ряд важных промышленных применений. Они включают извлечение и очистку металлов, нанесение гальванических покрытий, а также анодирование и получение различных химических веществ.
Извлечение металлов
Извлечение металлов первой и второй групп периодической системы осуществляется с помощью электролиза из расплавленных галогенидов этих металлов. Например, натрийполучают электролизом расплавленного хлорида натрия в электролизере Даунса. Магнийполучают электролизом хлорида магния, который в свою очередь получают из доломита и морской воды.
Очистка металлов
Очистка таких металлов, какмедьицинк, может осуществляться с помощью электролиза с растворимым анодом. Очистка металлов называется рафинированием. На рис. 7.10 схематически изображен процесс очистки меди. Неочищенная медь играет в этом процессе роль анода, а очищенная медь роль катода; в качестве электролита может использоваться раствор сульфата меди.
На аноде протекает полуреакция.
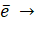
Cu0 2Cu2+.
Примеси, высвобождаемые при растворении неочищенноймедина аноде, опускаются на дно электролизера, образуя так называемый анодный ил. Этот ил может содержать драгоценные металлы, например золото и серебро. Переходящие в раствор ионы меди разряжаются и осаждаются на чистом медном катоде. Эта полуреакция описывается уравнением.
Cu2++ 2Cu0.
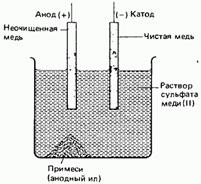
Рис. 10. Рафинированиемеди.
Нанесение гальванических покрытий (гальваностегия)
В этом процессе нанесение покрытия (электроосаждение) осуществляется на катоде. Катод погружают вэлектролит, который содержит ионы электроосаждаемого металла. В качестве анода используется пластина или стержень из того металла, которым наносят покрытие. Для успешного проведения электроосаждения следует тщательно контролировать силуэлектрическоготока, концентрацию электролита и температуру. Кроме того, необходимо предварительно подвергнуть очистке катод.
Нанесение гальванического покрытия может включать целый ряд стадий. Например, покрытие железа хромом включает четыре стадии:
- 1. Очистка железного предмета, играющего роль катода, при помощи серной кислоты с последующей промывкой деионизированной водой.
- 2. Покрытие железного катода медью.
- 3. Последующее покрытие катоданикелемс целью предотвращения коррозии.
- 4. Окончательное покрытие предмета хромом.
Гальванопластика.Это электролитическое осаждение металла на поверхности какого-либо предмета для воспроизведения его формы. Для этого с предмета сначала снимают слепок (из воска или гипса) и покрывают его токопроводящим слоем, например, слоем графита. Подготовленный таким способом предмет помещают в качестве катода в ванну с раствором соли соответствующего металла. При включении тока металл из электролита оседает на поверхности предмета. Гальванопластику используют для изготовления неограниченного числа точных копий того изделия, с которого был снят слепок.
Гальванополировка
Если резное металлическое изделие поместить в раствор электролита и включить ток, то наиболее сильное электрическое поле образуется у микроскопических выступов на поверхности этого изделия. Если оно подключено к «+» источника тока, то наиболее интенсивно ионы металла будут «вырываться» именно из выступов, и поверхность металла выровняется.
Анодирование
Так называется процесс покрытия алюминиевых предметов оксидом алюминия. В этом процессе покрываемый предмет играет роль анода, а в качестве электролита используется разбавленная сернаякислота. Покрытие изоксидаалюминияпредохраняет предмет от коррозии.
Получение химических веществ
Важнейшим примером подобного применения электролиза является получение гидроксиданатрия, водорода и хлора в электролизере с ртутным катодом.
Электрофорез
На поверхности коллоидных частиц, взвешенных в растворе, часто имеютсяэлектрическиезарядыиз-заадсорбцииионов или электронов. Например, частицы золота в водном золе золота адсорбируют на своей поверхности гидроксидные ионы. При пропусканииэлектрическоготокачерез золь отрицательно заряженные частицы золя мигрируют к аноду (рис. 7.11). Миграция заряженных коллоидных частиц к какому-либо электроду называется электрофорез. (Другое название электрофореза катафорез.).
Электрофорез находит важные применения в технике, медицине ибиохимии. Он может использоваться для разделения, идентификации и количественного определения белков и жиров.
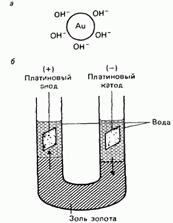
Рис. 11. Электрофорез, а адсорбцияионов на поверхности коллоидной частицы; б схема электрофореза
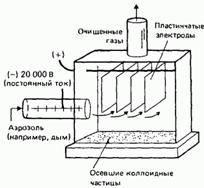
Электроосадитель Коттрелла.Электрофорез может использоваться также для удаления электрически заряженных частиц из различных аэрозолей, например из тумана, пыльного воздуха или дыма. С этой целью используется специальное устройство электроосадитель (электрофильтр) Коттрелла (рис. 7.12). Сначалааэрозольпропускают через отрицательно заряженное поле, в результате чего содержащиеся в нем частицы сильно электризуются, приобретая значительныеэлектрическиезаряды. Затем аэрозоль пропускают через положительно заряженное поле, в котором происходит осаждение отрицательно заряженных коллоидных частиц. Электроосадитель Коттрелла используется в промышленности для удаления частиц дыма из дымовых газов и для извлечения из отходов ценных продуктов, которые иначе могут быть потеряны. Электроосадители используются также в системах кондиционирования воздуха на промышленных предприятиях и в учреждениях.
Рис. 12. Электроосадитель Коттрелла
Электродиализ.
Диализ это отделение коллоидных частиц от электролитов или молекулярных частиц от дисперсионной среды, в которой они растворены. Простейшая установка для диализа представляет собой мешочек из полупроницаемого материала (например, целлофана или пергаментной бумаги), погруженный в дисперсионную среду. Ионные и молекулярные частицы способны диффундировать через стенки мешочка в дисперсионную среду. Коллоидные частицы остаются внутри мешочка.
Диализ может использоваться, например, для удаления избыточных ионовиз золя, содержащего коллоидные частицы оксидакоторый стабилизирован этими ионами (рис. 13).
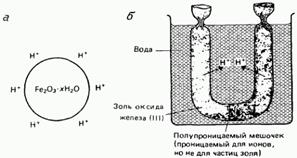
Рис. 13. а стабилизациягидратированных частиц золяв результатеадсорбциина их поверхности ионов; б удаление избыточных ионовиз электролита с помощью диализа.
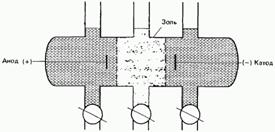
Диализ довольно медленный процесс. Чтобы добиться достаточно полного удаления неколлоидного вещества, приходится часто менять дисперсионную среду. Но если неколлоидное вещество представляет собойэлектролит, диализ можно ускорить, применяя вариант этой методики, который называется электродиализ (рис. 7.14). Электродиализ одно время использовали для промышленного получения пресной воды из засоленных грунтовых вод или из морской воды. Однако впоследствии были предложены более экономичные методы обессоливания воды.
Рис. 14. Электродиализ
Искусственная почка
Диализ находит применение в медицине для поддержания больных, почки которых не справляются со своей функцией. Процесс, основанный на использовании диализа для удаления токсичных продуктов обмена веществ из крови, называется гемодиализ. Этот процесс проводитси в специальном диализере, который и представляет собой искусственную почку. Поток крови, отведенный из артерии пациента, пропускают через искусственную почку, где он циркулирует по одну сторону полупроницаемой мембраны. По другую ее сторону циркулирует раствор электролита, который по своему составу близок к составу электролита в крови пациента. Токсичные продукты диффундируют через мембрану из крови в этот раствор. Поры мембраны настолько малы, что не пропускают кровяные тельца и белки в раствор. Очищенная кровь возвращается в тело пациента через вену.