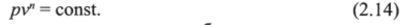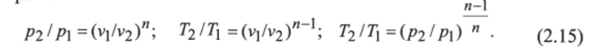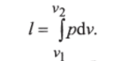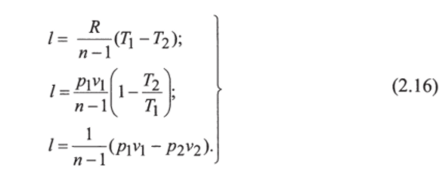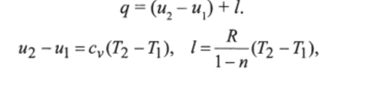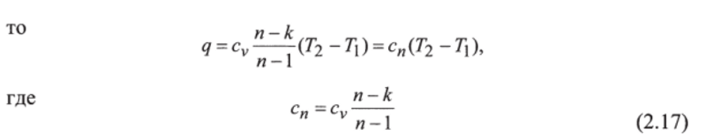Политропным называется процесс, который описывается уравнением:
Показатель политропы п может принимать любое численное значение в пределах отоо до +оо, но для данного процесса он является величиной постоянной.
Из уравнения (2.14) и уравнения Клапейрона нетрудно получить выражение, устанавливающее связь между р, v и Т в любых двух точках на политропе: 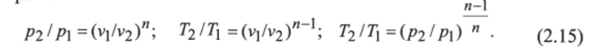
Работа расширения газа в политропном процессе:
В случае идеального газа можно преобразовать к виду:
Количество подведенного (или отведенного) в процессе теплоты можно определить с помощью уравнения первого закона термодинамики:
Поскольку 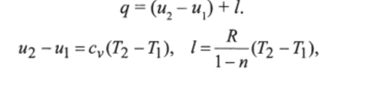
представляет собой теплоемкость идеального газа в политропном процессе. При су, кип = const сп = const, поэтому политропный процесс иногда определяют как процесс с постоянной теплоемкостью.
Политропный процесс имеет обобщающее значение, ибо охватывает всю совокупность основных термодинамических процессов (см. табл. 2.1).
Таблица 2.1
Характеристики основных термодинамических процессов
Название процесса. | Уравнение кривой процесса в диаграмме РУ | Показатель степени в уравнении кривой процесса. | Теплоемкость в процессе. | Величина а*,. | Уравнение кривой процесса в диаграмме 7> |
Политропный. | рР = const. | п | с | ?v_. ср | 7* v. 5 = Су In-+ К In-+ $ 0 =. То v0. = ср In — - R In — + sq 7*0 РО |
Изохорный. | v — const. | п = ±00. | СV. | | . Т = cv In—+0 Т0 |
Изобарный. | р = const. | о. II. | с. | ?v__ J_ ср к | 1 Т ^ S=CP 1п^Г + 50 у0. |
Изотермический. | pv = const. | п= 1. | | | Т= const. |
Адиабатный. | pv* = const. | п = к | | ±00. | s = const. |
а* = A u/q — отношение изменения внутренней энергии, А и к теплоте процесса.