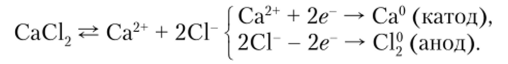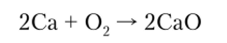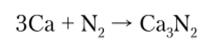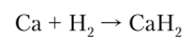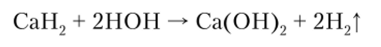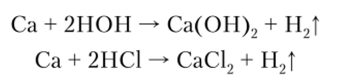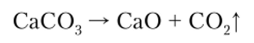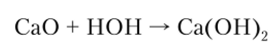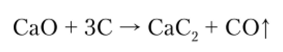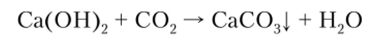Кальций относится к числу самых распространенных элементов. В земной коре содержание кальция достигает 3%. Из солей кальция образованы горные массивы и глинистые породы; он содержится в морской и речной воде, входит в состав растительных и животных организмов.
Наиболее важными природными соединениями кальция являются мел, мрамор, известняк, представляющие собой разновидности карбоната кальция СаС03; гипс CaS04-2H20; фосфориты Са3(Р04)2; флюорит CaF2; апатит Ca5(P04)3(F, Cl, ОН).
Кальций получают электролизом расплава хлорида кальция:
Свойства кальция и его соединений. По своим физическим свойствам кальций, как и остальные металлы этой группы, представляет собой легкий, твердый металл. В свежем разрезе имеет беловато-серый цвет. Кальций можно обтачивать на токарном станке, вытягивать в проволоку, ковать, прессовать.
В химическом отношении кальций чрезвычайно активен. Уже на воздухе он быстро покрывается слоем оксида, а если поджечь, то горит ярким кирпично-красным пламенем:
Кальций энергично реагирует с другими окислителями, такими как галогены, сера, фосфор и др. Большое значение имеет реакция взаимодействия кальция с азотом. При повышенных температурах эти элементы реагируют с образованием нитридов:
Этой реакцией обычно пользуются для удаления растворенного азота из сплавов, а также для связывания азота при получении благородных газов.
В атмосфере подогретого водорода кальций реагирует с образованием гидрида:
Гидрид кальция, как и остальные гидриды, активно реагирует с водой, образуя гидроксид кальция и водород:
Кальций очень легко окисляется водой и кислотами, восстанавливая из последних водород:
Оксид кальция СаО в промышленности получают термическим разложением карбоната кальция:
Оксид кальция (негашеная известь, жженая известь) реагирует с водой, образуя гашеную известь Са (ОН)2:
Этот процесс называется гашением извести.
При высоких температурах оксид кальция реагирует с коксом, образуя карбид и оксид:
Карбид кальция широко применяется для получения ацетилена.
Оксид кальция относится к основным оксидам.
Гидроксид кальция Са (ОН)2 — сильное основание. В 1 л воды растворяется 1,56 г гидроксида кальция. Насыщенный раствор гидроксида кальция в воде называется известковой водой и имеет щелочную реакцию. Гидроксид кальция применяется в строительном деле.
Карбонат кальция СаСОэ — самое распространенное соединение кальция. Он нерастворим в воде, поэтому известковая вода при стоянии на воздухе мутнеет вследствие взаимодействия с оксидом углерода (1У):
Карбонат кальция широко применяется для получения оксида кальция.
Важнейшие соли кальция — сульфаты, фосфаты, хлориды — и их применение будут рассмотрены при описании солей соответствующих кислот.