Вода.
Общая и неорганическая химия для медиков и фармацевтов

В результате этого образуется прочный каркас. Плотность льда 0,91 г/см3. Теплота плавления льда аномально высока, например, она в 13,5 раз выше, чем у свинца. Плавление льда приводит к разрушению каркаса за счет почти полного разрыва одной из водородных связей. Часть молекул воды, образовавшихся при разрушении ассоциатов, попадает внутрь оставшихся фрагментов каркаса. Это приводит к аномальному… Читать ещё >
Вода. Общая и неорганическая химия для медиков и фармацевтов (реферат, курсовая, диплом, контрольная)
Вода — главное и наиболее распространенное соединение водорода на Земле. Водная оболочка Земли — гидросфера — занимает около 71% всей поверхности.
Чистая (дистиллированная) вода — жидкость без запаха с несколько неприятным вкусом. В тонком слое вода бесцветна, в толстом — имеет голубоватую окраску, так как поглощает волны в красном диапазоне видимого света. Вода плохо проводит тепло и имеет самую высокую теплоемкость среди жидкостей — 4,218 кДж/(кг-К).
Все необычные свойства воды связаны со строением ее молекулы:
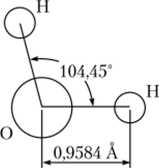
Атом кислорода находится в состоянии $/?3-ги6ридизации. Молекула имеет угловую форму, с углом между связями 104,5°. Две из четырех гибридных орбиталей кислорода образуют связи О—Н, на двух других находятся неподеленные пары электронов, причем одна из пар более активна при межмолекулярном взаимодействии, чем другая. Благодаря межмолекулярным водородным связям вода образует устойчивые ассоциаты.
В структуре льда каждая молекула воды связана с тремя соседними молекулами посредством двух водородных связей с участием обеих электронных пар:
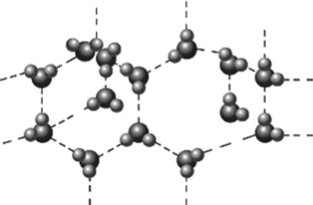
I I.
I I.
В результате этого образуется прочный каркас. Плотность льда 0,91 г/см3. Теплота плавления льда аномально высока, например, она в 13,5 раз выше, чем у свинца. Плавление льда приводит к разрушению каркаса за счет почти полного разрыва одной из водородных связей. Часть молекул воды, образовавшихся при разрушении ассоциатов, попадает внутрь оставшихся фрагментов каркаса. Это приводит к аномальному росту плотности в интервале температур от 0 до 4 °C. Плотность воды имеет максимум при 4 °C (1 г/мл). В жидкой воде выше этой температуры и вплоть до температуры кипения межмолекулярное взаимодействие обеспечивается лишь одной неподеленной парой электронов. Пар состоит из неассоциированных молекул воды.
Содержание воды в природе велико, проблема ее химического получения не стоит, однако существуют задачи по ее очистке.
- 1. Механическая фильтрация. Механическая очистка воды обеспечивается улавливанием частиц нерастворенных веществ за счет разницы размеров самих частиц и каналов фильтра, по которым протекает очищаемая вода. Колонки, заполненные гранулированным активированным углем с диаметром гранул 0,1 — 1 мм (100—1000 мк), способны эффективно задерживать частицы примерно такого же размера. Большая часть нерастворенных в воде частиц имеет гораздо меньший (0,1—20 мк) размер, не задерживаются при механической фильтрации и микроорганизмы, поэтому механическая фильтрация является лишь предварительной стадией очистки воды.
- 2. Сорбция, сорбенты и сорбционные фильтры. Сорбция — поглощение примесей из газа или жидкости твердыми телами, которые называют сорбентами. Процесс сорбционной очистки состоит в пропускании газа или жидкости через сосуд, заполненный сорбентом, — сорбционный фильтр. Если режим фильтрации и сорбент выбраны правильно, то достигается желаемый результат — удаление из газа или жидкости вредных примесей. Именно так работают противогазы и фильтры для воды.
Сорбционные фильтры — это в первую очередь угольные фильтры. Активированные угли — наиболее широко используемые сорбенты, производимые миллионами тонн в год. Эти универсальные сорбенты применяются для удаления примесей самой различной химической природы. Активация позволяет получить сорбент с площадью пор около 1000—1500 м2 на 1 г угля, что объясняет необычайно высокую эффективность активированных углей.
- 3. Ионный обмен — специфический способ сорбции заряженных частиц (ионов), когда поглощение одного иона сопровождается выходом в раствор другого иона, входящего в состав сорбента. При этом ион, присутствие которого в воде нежелательно, фиксируется на сорбенте. Таким образом, происходит «замещение» одних ионов на другие. Сорбенты, работающие по такому механизму, называются ионообменными материалами или ионитами. Иониты способны извлекать из воды одни растворенные соли, замещая их другими солями. Соли кальция и магния могут заменяться на соли натрия при смягчении жесткой воды. В процессе водоочистки ионный обмен используется для удаления из воды катионов тяжелых металлов, например свинца, представляющих опасность для здоровья человека, а также для избавления от нитратов.
- 4. Обратный осмос — это способ очистки воды с помощью обратноосмотической мембраны. Вода при таком способе очистки пропускается через мембрану («сито»), поры которой пропускают воду, но не пропускают растворенные в ней примеси. Система обратного осмоса позволяет получать воду очень высокой степени очистки. Обратным осмосом можно удалять из воды даже одновалентные ионы, например ионы Na+ и СГ. Обратноосмотические установки обязательно должны содержать активированный уголь, так как сама мембрана не задерживает низкомолекулярные высоколетучие органические соединения (хлороформ, СНС13 и др.), а также бактерии.
- 5. Дистилляция — процесс очистки жидкостей, заключающийся в испарении жидкости с последующей конденсацией пара. Дистилляцией можно отделить жидкость от растворенных в ней твердых веществ или разделить жидкости с сильно отличающимися температурами кипения. Дистиллированная вода относительно чистая, но процесс дистилляции достаточно дорог. Дистилляционные системы также должны обязательно содержать активированный уголь, необходимый для сорбции низкомолекулярных органических соединений, например СНС13.
- 6. Электрохимическая очистка основана на сложных окислительновосстановительных реакциях, которые происходят в воде под воздействием электрического тока и приводят к образованию так называемой живой и мертвой воды. Этот способ экономичен, так как позволяет достигнуть высокой производительности при небольших затратах. Электрохимическая очистка распространена в России, но не применяется в быту. В других странах этот вид очистки также используется только в промышленности. Электрохимическая очистка позволяет очистить воду от всех микроорганизмов, но при этом разрушается также часть органических веществ.
Вода в фармации: очищенная и апирогенная. В условиях аптеки и химико-фармацевтического производства вода широко используется для приготовления лекарственных препаратов, получения экстракционных препаратов, для мытья оборудования, тары и т. д. Качество используемой воды строго нормируется в зависимости от ее назначения. В Российской Федерации качество воды регламентирует Государственная фармакопея XI изд. (ГФ XI).
Вода очищенная (aqua purificata) используется для изготовления неинъекционных лекарственных средств: растворов внутреннего и наружного применения, офтальмологических растворов, лекарственных форм для новорожденных и др. Она применяется также для получения пара, санитарной обработки оборудования, помещений, мытья посуды (за исключением финишного ополаскивания), в лабораторной практике и др. На фармацевтическом производстве она является исходной при получении воды для инъекций.
Воду очищенную можно получить дистилляцией, ионным обменом, обратным осмосом, комбинацией этих методов или другим способом. Для оценки качества воды очищенной проводят испытания на содержание восстанавливающих веществ, диоксида углерода, хлоридов, сульфатов, аммиака, кальция, нитритов и нитратов, тяжелых металлов, определяются также сухой остаток, pH и микробиологическая чистота.
Вода для инъекций (aqua pro injectionibus) применяется для приготовления стерильных растворов лекарственных и диагностических средств, предназначенных для подкожного, внутримышечного, внутривенного введения, финишного ополаскивания тары и укупорки, обработки систем приготовления, хранения и распределения, непосредственно контактирующих с конечной продукцией.
К воде для инъекций предъявляют требование апирогенности (греч. а — отрицание + руг — огонь, жар + genes — порождающий). Апирогенная вода не содержит веществ (метаболитов или продуктов жизнедеятельности бактерий), вызывающих при введении в организм повышение температуры тела и другие нежелательные реакции. Такой эффект наблюдается при попадании в кровяное русло пирогенов — эндотоксинов грамотрицательных бактерий, представляющих собой липополисахарид наружной мембраны, а также компонентов клеточной стенки грамположительных бактерий (пептидоглюканы, липотейхоевые кислоты). В связи с этим особую опасность представляют инфузионные растворы, загрязненные бактериальными эндотоксинами, так как они вводятся человеку в больших объемах. Вода для инъекций должна отвечать требованиям, предъявляемым к воде очищенной, кроме того, в ней должны отсутствовать пирогенные вещества, антимикробные вещества и другие добавки.
Согласно ГФ XI тест на пирогенность проводится биологическим методом на кроликах. Он основан на измерении температуры тела животных после внутривенного введения испытуемого препарата. Отсутствие повышения температуры животных является доказательством апирогенности воды для инъекций. Однако этот метод обладает недостатками: длительностью выполнения процедур, значительной вариабельностью результатов, связанных с индивидуальной чувствительностью животных и сезонностью. От указанных недостатков свободны методы in vitro (лат. «в стекле»): люминесцентный, флуориметрический и LAL-тест. Люминесцентный метод основан на способности бактериальных эндотоксинов усиливать флуоресценцию родамина 6Ж и 1-анилинонафталин-8-сульфоната. Флуориметрический метод базируется на измерении собственной интегральной флуоресценции бактериальных пирогенов в пределах длин волн эмиссии от 310 до 400 нм. В основе LAL-теста лежит способность лизата амебоцитов (клеток крови) мечехвоста специфически реагировать с эндотоксинами грамотрицательных бактерий. В результате реакции происходит помутнение прозрачной реакционной смеси или образование твердого геля, что и служит индикатором присутствия эндотоксина.
В соответствии с требованиями ГФ XI конечной стадией получения воды для инъекций должна быть дистилляция или обратный осмос. В Европейской фармакопее VI изд. и Руководстве о качестве воды для фармацевтических целей Европейского агентства по оценке медицинской продукции (ЕМЕА) в качестве официального принят только один способ — метод дистилляции.
В случаях, когда для приготовления лекарственных препаратов необходима вода высшего качества, ее получают методом двойного обратного осмоса совместно с другими методами, например ультрафильтрацией и деионизацией. Для такой воды в Европейской фармакопее существует обозначение «Вода высокоочищенная» (aqua valde purificata).
Химические свойства воды. Вода — высокоактивное химическое вещество. Она способна к самоионизации (автопротолизу), но в чистом виде обладает очень слабой электрической проводимостью (Kw =110 14).
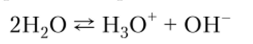
®.Автопротолиз — обратимый процесс образования равного числа катионов и анионов из незаряженных молекул жидкого индивидуального вещества за счет перехода протона от одной молекулы к другой.
Вода — амфотерное соединение, проявляющее свойства как основания:
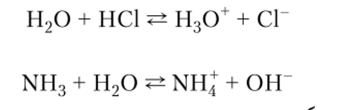
так и кислоты:
В своих многочисленных реакциях вода может Ьыть как окислителем, так и восстановителем.
1. Вода взаимодействует с некоторыми неметаллами, проявляя окислительные свойства или, благодаря полярности молекулы, способствуя протеканию реакции дисмутации:
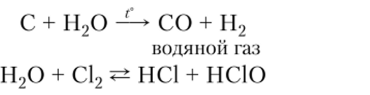
2. В реакции с металлами вода выступает как окислитель:
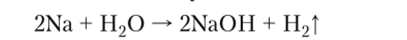
со всеми щелочными и щелочноземельными металлами.
3. Вода — восстановитель в реакции с фтором и некоторыми фторидами или в процессе фотосинтеза:
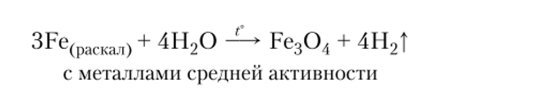
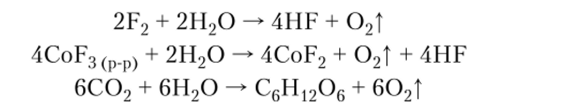
4. Вода реагирует с кислотными и основными оксидами с образованием кислот и щелочей: 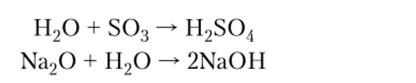
5. Многие соли, образованные слабыми кислотами и (или) слабыми основаниями, в воде подвергаются обратимому или полному гидролизу, например: 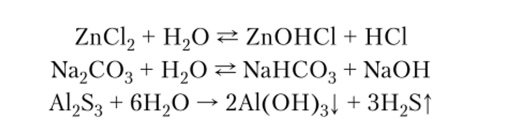
6. Вода является кислотой по теории Льюиса. Наличие у атома кислорода двух неиоделенных пар электронов делает молекулу воды активным лигандом, образующим с катионами-металлов устойчивые комплексные ионы: [Cu (H20)4]2*, [Cr (H20)6]3+, [Zn (H20)4]2+. Аквакомилексы многих d-металлов красиво окрашены: аквакомплексы меди (П) — в голубой цвет, никеля (Н) — в зеленый, кобальта (П) — в розовый. Аквакомплексы всех металлов, кроме щелочных и щелочноземельных, являются кислотами по Брёнстеду и выступают в водных растворах донорами протонов. Кислотные свойства обусловлены тем, что в молекуле воды, координированной по катиону, ослабляется связь О—Н и катион Н+ уходит из внутренней сферы. Кислотные свойства аквакомплексов тем сильнее, чем выше степень окисления ионакомплексообразователя. Так, катион [Fe (H20)G]3+ является более сильной кислотой, чем уксусная кислота. Вода обычно легко вытесняется из комплексов другими лигандами, образующими с ионом металла более прочную связь.
При выпаривании растворов некоторых солей они выпадают в виде кристаллогидратов, например
Na2C03— 10Н2О — кристаллическая сода (декагидрат карбоната натрия);
CuS04 -5H20 — медный купорос [пентагидрат сульфата меди (П)].
Кристаллогидраты образуются, если в кристаллической решетке связь между катионами и молекулами воды более прочная, чем с анионами в кристалле безводной соли. При низких температурах вода может связываться как с катионами, так и с анионами. Кристаллизационная вода обычно может быть удалена нагреванием, при этом удаление воды идет ступенчато.
7. Вода реагирует с большим числом органических соединений (реакции гидратации алкенов и алкинов, гидролиз сложных эфиров, дии полисахаридов, пептидов и белков и др.).