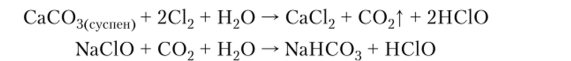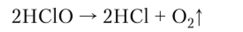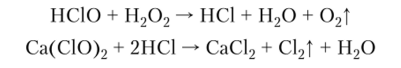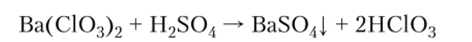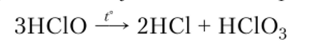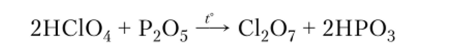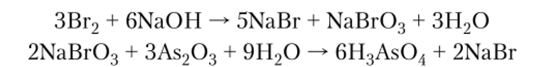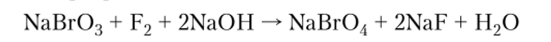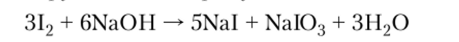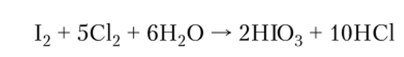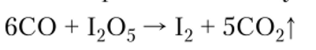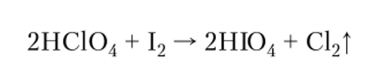Получение НСЮ:
Хлорноватистая кислота разлагается с выделением атомарного кислорода. На этом основан процесс отбеливания и стерилизации:
Кислота и ее соли проявляют окислительные свойства: 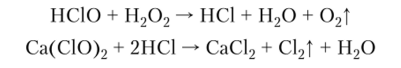
Хлорноватая кислота, хлораты
Получение НСЮ3 из солей:
При нагревании раствор НСЮ претерпевает глубокое диспропорционирование и также образуется более устойчивая хлорноватая кислота:
НС103 максимальной концентрации 40% является сильным окислителем, обугливает вату, бумагу.
Хлораты ядовиты; в расплавах являются сильными окислителями:  Хлорная кислота, перхлораты НС104 в свободном состоянии не очень устойчива, но устойчива в растворах. Одна из самых сильных неорганических кислот. Сильный окислитель, но в растворах окислительных свойств не проявляет (не окисляет HI и H2S). При действии Р205 из кислоты можно получить соответствующий оксид:
Хлорная кислота, перхлораты НС104 в свободном состоянии не очень устойчива, но устойчива в растворах. Одна из самых сильных неорганических кислот. Сильный окислитель, но в растворах окислительных свойств не проявляет (не окисляет HI и H2S). При действии Р205 из кислоты можно получить соответствующий оксид: 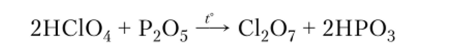
Перхлораты при нагревании разлагаются (в зависимости от природы металла) с образованием хлорида металла и 02 или с образованием оксида металла, 02 и С12, возможно также одновременное протекание этих двух процессов.
Кислородные соединения брома и иода
Кислородные соединения брома менее устойчивы по сравнению с кислородными соединениями хлора. Бромат натрия образуется при взаимодействии брома со щелочью уже при комнатной температуре и используется как окислитель в аналитической химии:
Бром трудно окислить до состояния (+7), впервые пербромат был выделен из реакции с фтором: 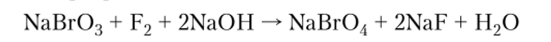
Кислородные соединения иода более устойчивы. В щелочном растворе иод диспропорционирует подобно брому:
При пропускании хлора в водную суспензию иода образуется йодноватая кислота:
Из раствора она выделяется в виде устойчивого кристаллического вещества, при ее обезвоживании получается оксид I2O5, устойчивый при обычных условиях. Он применяется при анализе воздуха на наличие СО.
Известна и йодная кислота, которая образуется при действии хлорной кислоты на иод: 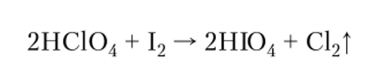
После испарения воды йодная кислота переходит в ортоиодную кислоту Н5Ю6, в которой все атомы водорода могут замещаться на металл — Ag5IOG.