Гидриды.
Галогениды.
Химия элементов

Ковалентные (молекулярные) галогениды. Большинство электроотрицательных элементов, а также металлы в высших степенях окисления образуют ковалентные галогениды. Эти соединения — либо газообразные, либо жидкие, либо легколетучие твердые вещества, молекулы которых удерживаются вместе благодаря вандерваальсовым силам. Считается, что существует взаимосвязь между увеличением ковалентности связи… Читать ещё >
Гидриды. Галогениды. Химия элементов (реферат, курсовая, диплом, контрольная)
Галогены образуют соединения с водородом (HHal), в которых связующая электронная пара смещена в сторону галогенов. Поэтому в молекулах HHal ковалентная связь нолярна. Поскольку электроотрицательность в ряду F — Cl — Br — I уменьшается от фтора к иоду, то в молекуле HF электронная пара будет смещена в сторону галогена в наибольшей степени, а у III — в наименьшей. Поэтому уменьшается и степень перекрывания взаимодействующих орбиталей, что, в свою очередь, приводит к ослаблению связи между водородом и галогеном в ряду FIF — НС1 — HBr — HI. С уменьшением прочности связи в молекулах HHal снижается их устойчивость к нагреванию. Так, термическая диссоциация при 1000 °C у HI составляет 33%, у НВг — 0,5, У НС1 — 0,014, а у HF заметной диссоциации не наблюдается.
Все галогеноводороды — бесцветные газы с резким запахом, легко растворимы в воде. При 0 °C в 1 объеме воды растворяется 500 объемов НС1, 600 объемов НВг и 450 объемов HI. Фтороводород смешивается с водой в любых соотношениях. Высокая растворимость соединений галогенов с водородом в воде позволяет получать растворы с высокой концентрацией этих веществ. При растворении в воде галогеноводороды диссоциируют по типу кислот. HF относится к слабо диссоциированным соединениям, что объясняется особо прочной связью в молекуле. Остальные же галогеноводороды относятся к числу сильных кислот. Галогеноводородные кислоты и их соли носят следующие названия: фтороводородная (плавиковая) кислота HF (фториды); хлороводородная (соляная) кислота НС1 (хлориды); бромоводородная кислота НВг (бромиды); иодисто-водородная кислота HI (иодиды). Сухие газообразные галогеноводороды не действуют на большинство металлов.
Плавиковая кислота разрушает стекло и силикаты:
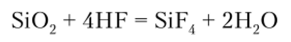
поэтому она не может храниться в стеклянной посуде. Кроме плагины и золота плавиковая кислота действует на все металлы, окисляя их. В большинстве случаев реакция взаимодействия HF с металлами протекает лишь на поверхности металла. Образующийся фторид предотвращает дальнейшее протекание реакции.
НС1, подобно другим сильным кислотам, энергично взаимодействует со многими металлами, их оксидами и гидроксидами. На металлы, стоящие в ряду стандартных электродных потенциалов после водорода, НС1 не действует. По химическим свойствам НВг и HI очень похожи на НС1: в газообразном состоянии они не действуют на большинство металлов, а в водных растворах проявляют свойства одноосновных кислот.
Существенное различие между галогеноводородными кислотами проявляется в их отношении к окислителям. Галогенид-ионы Hal, за исключением фторид-иона, — восстановители. Восстановительная способность галогеноводородных кислот и их солей повышается в ряду Cl — Br — I :
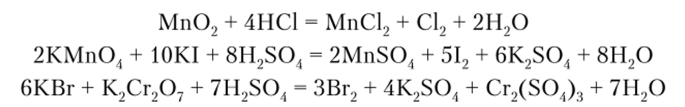
Взаимодействие молекул HHal с H2S04 осуществляется в соответствии с изменением энергии Гиббса. Для уравнения реакции.
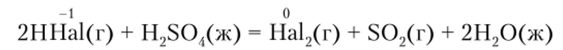
значения Д (?298 (в кДж/моль) равны: 456 для HF, 105 для НС1; 25 для НВг и -68 для HI. Следовательно, в такое взаимодействие могут вступать только НВг и HI: первый восстанавливает H2S04 до S02, а второй — до H2S:
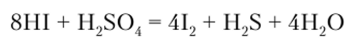
Из этого следует, что действием серной кислоты на бромиды и иодиды нельзя получить НВг и HI.
HF и НС1 с H2S04 не взаимодействуют.
Фтороводород HF получают действием концентрированной серной кислоты на плавиковый шпат:
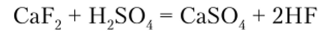
Раствор фтороводорода, содержащий 40% HF, называется плавиковой кислотой.
Хлороводород НС1 получают непосредственным взаимодействием водорода с хлором или сульфатным способом, который основан на реакции взаимодействия концентрированной серной кислоты с NaCl. На холоде реакция протекает с образованием НС1 и NaHS04.
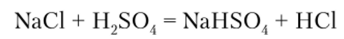
При нагревании протекает вторая стадия реакции:
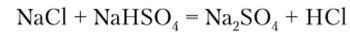
Сульфатный способ получения НС1 сопряжен с большими экономическими затратами, связанными в первую очередь со значительными расходами концентрированной серной кислоты. Поэтому в настоящее время основным способом получения НС1 является прямой синтез из водорода и хлора.
НС1 — газ с резким запахом, на воздухе при соприкосновении с парами воды образует капельки тумана (дымит). Водный раствор называется соляной кислотой.
В медицинской практике находит применение разбавленная соляная кислота.
Бромоводород и иодоводород получают гидролизом РВг3 и Р13:
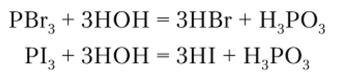
НВг при соприкосновении с кислородом воздуха легко окисляется до свободного брома: 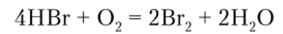
HI легко окисляется кислородом воздуха, образуя свободный иод:
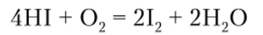
Водный раствор HI является сильным восстановителем.
Ионные галогениды. Большинство галогенидов металлов в состояниях окисления +1, +2 и +3 имеют преимущественно ионный характер. Между галогенидами, которые можно считать чисто ионными, и галогенидами с ковалентным типом связи существует непрерывный ряд соединений со связями промежуточного характера. Галогениды щелочных и щелочно-земельных элементов большинства лантаноидов и некоторые галогениды металлов-семейства и актиноидов можно рассматривать в основном как ионные соединения. Ковалентность усиливается по мере увеличения отношения заряд/радиус для иона металла. Например, в ряду хлоридов КС1, СаС12, ScCl3, ТеС14 характер связи изменяется от чисто ионной (КС1) к ковалентной (TiCl4). Аналогично галогениды металлов с переменной степенью окисления в низших состояниях окисления будут ионными, а в высших — ковалентными.
Большинство ионных галогенидов растворимо в воде и дает гидратированные ионы металла и галогенида. Лантаноиды и актиноиды в степенях окисления +3 и +4 образуют нерастворимые в воде фториды. Ограниченно растворимы в воде LiF, CaF2, SrF2 и BaF2. Свинец образует труднорастворимую соль PbClF. Нерастворимы также хлориды, бромиды и иодиды Ag (I), Cu (I), Hg (I) и РЬ (П). Растворимость ионных галогенидов для одного и того же элемента в ряду MeF" — МеС1я — MeBrw — Ме1я увеличивается от фторида к иодиду, поскольку определяющим фактором при этом являются энергии решеток, которые имеют наибольшее значение у фторидов и наименьшее — у иодидов. Такой порядок наблюдается для галогенидов щелочных, щелочно-земельных металлов и лантаноидов.
Ковалентные (молекулярные) галогениды. Большинство электроотрицательных элементов, а также металлы в высших степенях окисления образуют ковалентные галогениды. Эти соединения — либо газообразные, либо жидкие, либо легколетучие твердые вещества, молекулы которых удерживаются вместе благодаря вандерваальсовым силам. Считается, что существует взаимосвязь между увеличением ковалентности связи «металл — галоген» и повышением способности к образованию молекулярных соединений, поэтому их часто называют ковалентными галогенидами.
Важной особенностью строения ковалентных галогенидов является образование галогенидных мостиков между двумя или, реже, тремя другими атомами. Чаще всего между двумя атомами образуются мостики за счет двух атомов галогена, но известны соединения с одним и тремя мостиковыми атомами. Теория МО рассматривает связи во фрагменте Me — Hal — Me как трехцентровые четырехэлектронные (рис. 16.1).
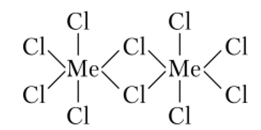
Рис. 16.1. Строение ковалентных галогенидов.
Хлори бромсодержащие мостики имеют угловую структуру, a F-мостики могут быть изогнутыми и линейными.
Ионные галогениды, как правило, не подвергаются гидролизу, а ковалентные галогениды гидролизуются очень легко:
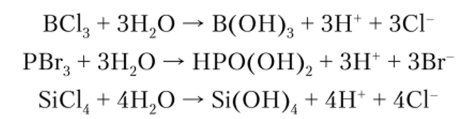
Такие галогениды, как SFG, СС14, очень устойчивы к воде и гидролизу не подвергаются. Это следствие влияния кинетических факторов.
При действии окислителей на галогениды наблюдаются те же закономерности, которые характерны для HHal.
Комплексные галогенид-анионы. Среди комплексных галогенид-анионов наиболее важные — фториды и хлориды. Они образуются при взаимодействии галогенида металла или неметалла, действующего в качестве кислоты Льюиса, с галогенид-ионом, который выступает как основание:
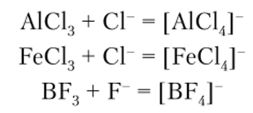
Большинство таких анионов может образоваться в водных растворах.
Комплексные соединения, образованные галогенид-ионами, характеризуются различной устойчивостью. Как правило, устойчивость понижается в ряду F — Cl — Br — I.
Комплексные галогенид-анионы образуются во многих реакциях, в которых принимают участие кислоты Льюиса, в частности А1С13 и BF3. Комплексные фториды весьма разнообразны. Для элементов второго периода координационное число по фтору равно 4, а для элементов остальных периодов оно равно 6. Известны также комплексные фториды, в которых координационное число центрального атома равно 7, 8, 9: KJBeFJ, K3[A1F6], K2[NbF7], K2[WF8], K2[ReF9|. Комплексные анионы фтора могут быть получены взаимодействием амфотерных фторидов с основными и кислотными фторидами:
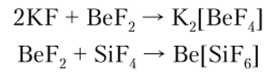
Комплексы типа [ЭНа14] имеют квадратную форму, что согласно теории МО отвечает двум взаимно перпендикулярным трехцентровым связям Hal —Э —Hal. Отрицательные ионы Вг" и I могут координировать вокруг себя нейтральные атомы галогенов, образуя комплексные ионы типа [Hal «-Hal®, получившие название полигалогениды или галогалогениды. Так, молекулярный 12, растворяясь в растворе KI, образует с ним комплексный дииодоиодат-ион:
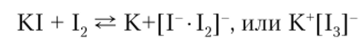
Координационная связь здесь относительно мало прочная, поэтому К[13] распадается на составные компоненты и указанная система находится в состоянии динамического равновесия, в связи с чем раствором 12 в KI можно пользоваться как свободным иодом. Известны и более сложные нолииодиды калия: К * 11″ • 1^ |, К * 11 • 18]".
Биологическая роль галогенов. Галогены в виде различных соединений входят в состав тканей человека и животных. Хлор и иод относятся к незаменимым элементам, а остальные являются постоянными составными частями тканей.
По содержанию в организме человека хлор (0,15%) относится к макроэлементам, в то время как остальные элементы этой группы являются микроэлементами (содержание ~10 5%).
В организме все галогены находятся в степени окисления -1, хлор и бром — в виде гидратированных ионов СГ и Вг", а фтор и иод — главным образом в связанной форме в составе некоторых биоорганических соединений.
Соединения фтора концентрируются в костной ткани, ногтях, зубах. В состав зубов входит около 0,01% фтора, причем большая часть приходится на эмаль, что связано с присутствием в ней труднорастворимого фторапатита Ca5(PO/i)3F. Недостаток фтора в организме приводит к кариесу зубов. Вреден не только недостаток, но и избыток фтора. При содержании фтора в питьевой воде выше предельно допустимой нормы (1,2 мг/л) зубная эмаль становится хрупкой, легко разрушается. Возникающее в этом случае заболевание называется флуорозом (фторозом).
Хлорид-ионы играют важную биологическую роль. Они активируют некоторые ферменты, создают благоприятную среду для действия протолитических ферментов желудочного сока, обеспечивают ионные потоки через клеточные мембраны, участвуют в поддержании осмотического равновесия.
Бром локализуется преимущественно в железах внутренней секреции, в первую очередь в гипофизе. Биологическая роль соединений брома в нормальной жизнедеятельности организма еще недостаточно выяснена. Имеются данные, что соединения брома угнетают функцию щитовидной железы и усиливают активность коры надпочечников. Бромид-ионы способствуют восстановлению нарушенного равновесия между процессами возбуждения и торможения.
Иод относится к числу незаменимых биогенных элементов, и его соединения играют важную роль в процессах обмена веществ. Имеются данные, что иод влияет на синтез некоторых белков, жиров, гормонов. Щитовидная железа способна концентрировать I в 25 раз по сравнению с содержанием его в плазме. Пониженная активность щитовидной железы (гипотиреоз) может быть связана с уменьшением ее способности накапливать иодид-ионы, а также с недостатком в пище иода (эндемический зоб).
Галогениды находят широкое применение в медицине и фармации.
Хлорид натрия (натрия хлорид) NaCl (поваренная соль) — см. параграф 3.4.
Хлорид калия КС1 (сильвин) применяют в качестве удобрения.
Хлорид кальция (кальция хлорид) СаС12 при получении кристаллизуется в виде гексагидрата СаС12-6Н20. При нагревании до 800 °C переходит в безводную соль, которая широко применяется для сушки различных химических соединений. СаС12 • 6Н20 гигроскопичен, на воздухе очень быстро поглощает влагу и расплывается. Хлорид кальция широко применяется в медицине как кровоостанавливающее средство, при аллергических заболеваниях, а также в качестве противоядия при отравлении солями магния.
Хлорид серебра AgCl применяется как светочувствительное вещество при изготовлении фотопленок, что основано на способности AgCl разлагаться под влиянием света с образованием свободного серебра.
Хлорид цинка ZnCl2 — ядовитое соединение. Применяется как средство, предохраняющее деревянные изделия от гниения, а также в целлюлознобумажной промышленности.
Бромид аммония (аммония бромид) NH4Br применяется, как и NaBr и КВг, при нервных расстройствах в качестве успокаивающего средства.
Иодид калия (калия иодид) KI получают взаимодействием Fel2 с иодом в щелочной среде:
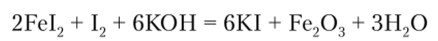
Раствор отделяют от оксида железа (Ш) и после упаривания кристаллизуют.
KI применяют для лечения глазных заболеваний — катаракты, глаукомы, при отравлениях солями ртути. В аналитической химии используют для приготовления индикатора — иодкрахмальной бумаги.
Обнаружение галогеноводородных кислот и их солей. Нитрат серебра в присутствии разбавленной азотной кислоты осаждает из растворов осадки солей серебра с анионами СП, Вг и I по реакциям.
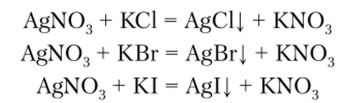
AgF в воде растворим.
AgCl — белый творожистый осадок, нерастворимый в воде и азотной кислоте, но растворимый в аммиаке:

При подкислении раствора комплекс разрушается и AgCl снова выпадает в осадок:
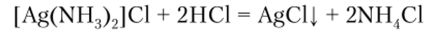
AgBr — осадок бледно-желтого цвета, нерастворим в воде и азотной кислоте. Частично растворим в аммиаке.
Agl — осадок желтого цвета. Нерастворим в воде, азотной кислоте и аммиаке. Хорошо растворяется в растворах цианида калия и тиосульфата натрия.
Хлорид серебра в отличие от бромида и иодида растворяется в карбонате аммония. Эта реакция позволяет открыть хлорид-ион при совместном присутствии с иодиди бромид-ионами.
Соединения галогенов друг с другом. Галогены образуют между собой бинарные соединения, которые могут быть нейтральными или ионными, например BrCl, IF5, Г3Вг3. Реже встречаются и тройные сочетания, например в полигалогенид-ионах типа IBrCl. Чем дальше галогены отстоят друг от друга в группе, тем легче они образуют между собой соединения. Большинство этих соединений неполярны, хотя некоторые из них имеют слабо выраженный полярный характер, например IC1, C1F3.
Галогены, расположенные рядом в группе, образуют соединения, в которых проявляют степень окисления +1 и -1; исключение составляет хлор, образующий с фтором соединение C1 °F,. Бром по отношению к фтору может проявлять степень окисления +3 и +5, а иод — +5 и +7. Иод по отношению к хлору имеет наивысшую степень окисления +3.
Соединения галогенов друг с другом образуют комплексные ионы (интергалогенид-ионы), которые могут быть как катионами, так и анионами. Фториды галогенов взаимодействуют с акцепторами фторид-ионов:
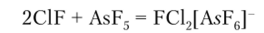
или донорами фторид-ионов:
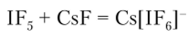
1С13 способен к комплексообразованию, давая комплекс [IC1,|, например К[1С14].