Хелаты и комплексы с макроциклическими лигандами

Это криптанд, «гость» — катион, входящий в полость криптанда и покидающий ее. Такие координационные системы обладают специфической избирательностью, но отношению к катионам того же размера, что и полость лиганда-хозяина. Избирательность проявляется в особой прочности комплекса с данным катионом, а сам акт образования комплекса может служить механизмом распознавания катиона биохимической системой… Читать ещё >
Хелаты и комплексы с макроциклическими лигандами (реферат, курсовая, диплом, контрольная)
Каждый из лигандов, перечисленных в табл. 13.1, может занимать только одно координационное место у центрального атома-комплексообразователя. Такие лиганды называют монодентатными. Число монодентатных лигандов в координационной сфере равно координационному числу комплексообразователя. Многие лиганды содержат два или более атомов, способных участвовать в координации. Такие атомы называют донорными (смысл этого названия станет ясен после рассмотрения природы химической связи в комплексных соединениях). Например, оксалат-ион С20~ имеет два донорных атома кислорода, а этилендиамин H2NCH2CH2NH2 — два донорных атома азота. Это примеры бидентатных лигандов. Бидентатный лиганд может занимать в комплексе два координационных места. Диэтилентриамин содержит три донорных атома азота и является тридентатиым лигандом. Анион четырехосновной этилендиаминтетрауксусной кислоты — этилендиаминтетраацетат-ион (ЭДТА) имеет два донорных атома азота и четыре донорных атома кислорода, являясь гексадентатным лигандом.
Дентатность лиганда равна числу донорных атомов, образующих связи с комплексообразователем.
Лиганды, содержащие два или более донорных атомов, объединяют под названием полидентатпые лиганды (табл. 13.2).
Многие комплексные соединения, содержащие полидентатные лиганды, являются хелатами. Па рис. 13.2, а и б видно, что бидентатные лиганды связываются с комплексообразователем сразу в двух точках, захватывают его подобно клешням рака, откуда и происходит название хелатов — клешневидные комплексы (от греч. chele — клешня). Характерная особенность хелатных соединений — образование циклических группировок атомов (хелатных циклов), включающих атом.
Полидентатные лиганды
Формула. | Название в координационной сфере. | Сокращенное обозначение. | Дентат; ность. |
ЮОС-СОО:; | Оксалато. | ох. | |
nh2—сн2—сн2—nh2 | Этилендиамин. | еп. | |
nh2-ch2ch2-nii-ch2ch2-nh2 | Диэтилен — триамин. | dien. | |
" :ООССН2, СН2СОО: :ООССН,>-СН'СН'ХСН, СООГ. | Этилендиаминтетраацетато. | ЭДТА. |
Примечание. Электронные пары указывают донорные атомы.
металла. Хелатообразующие лиганды или уже имеют, или приобретают в процессе образования комплексного соединения удобную для координации геометрическую форму — конформацию. Например, оксалат-ион (см. рис. 13.2, а)
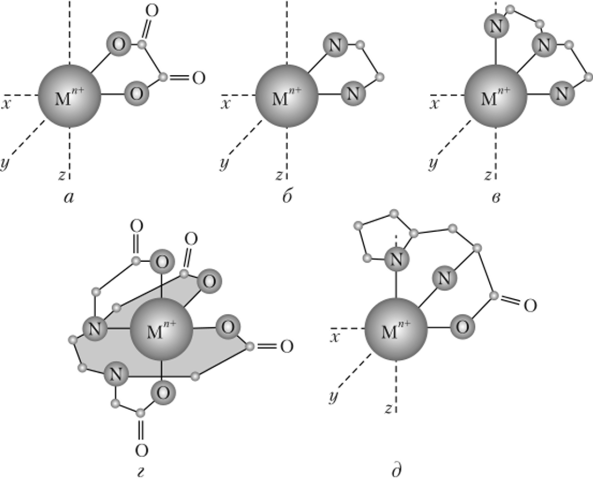
Рис. 13.2. Октаэдрические конфигурации комплексных ионов, содержащих в качестве лигандов:
а — оксалат-ион; б — этилендиамин; в — диэтилентриамин; г — этилендиамиитетраацетат-ион; д — анион аминокислоты гистидина сохраняет присущую ему плоскую геометрию и занимает своими донорными атомами кислорода две позиции в октаэдрической координационной сфере катиона М'7+. При этом образуется один пятичленный хелатный цикл, состоящий из катиона М"+ и цепочки —О—С—С—О—.
Несколько сложнее происходит координация этилендиамина (еп) и диэтилентриамина ((lien) (см. рис. 13.2, б, в). Эти лиганды имеют свободное осевое вращение вокруг связей С—С. При координации они принимают необходимые для нее конформации и также образуют иятичленные циклы: этилендиамин — один, а диэтилентриамин — два.
Еще более сложную конфирмационную перестройку при координации претерпевает этилендиаминтетраацетат-ион (ЭДТЛ), который в свободном состоянии имеет близкую к плоской развернутую конформацию, изображенную в табл. 13.2. При образовании комплекса он обертывается вокруг катиона М"+ (рис. 13.2, г). Свернутая конформация позволяет образовывать шесть связей и октаэдрическую координационную сферу. При этом ЭДТЛ образует с катионом М" + пять нятичленных хелатных циклов.
Способность к образованию сложных хелатных комплексов присуща не только специально разработанным лигандам типа этилендиамипа или этилендиаминтетраацетат-иона. Напротив, природные хелатообразующие лиганды очень многочисленны. Например, анион аминокислоты гистидина имеет два донорных атома азота и один атом кислорода:
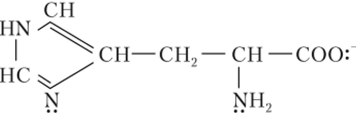
Октаэдрические координационные сферы многих двухзарядных катионов могут включать в свой состав два таких аниона. Фрагмент этой структуры показан на рис. 13.2, д.
Еще более сложны, чем хелатообразующие, макроциклические лиганды. В макроциклических комплексах донорные атомы располагаются внутри большого почти плоского кольца-цикла, в центре которого находится ион-комплексообразователь. Один из простых макроциклических комплексов — комплекс Ni2^ с тетраэтилентетраамином (рис. 13.3, а). Его дальний аналог — плоский комплекс магния — хлорофилл имеет гораздо более сложную структуру (рис. 13.3, в). Синтетические макроциклические полиэфирные лиганды — краун-
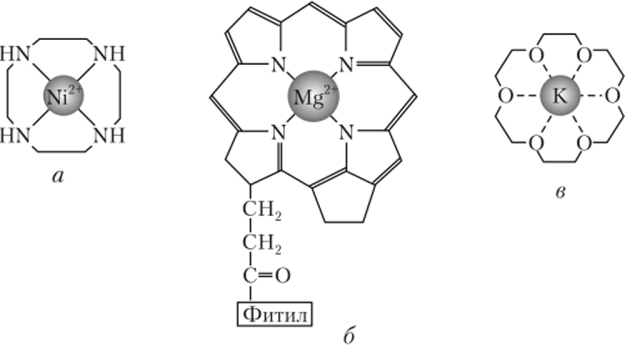
Рис. 13.3. Макроциклические комплексные соединения,
образованные:
а — циклическим тетраэтилентетраамином с катионом Ni, б — плоским порфириновым каркасом хлорофилла с катионом Mg, в — циклическим полиэфиром 18-краун-6 с катионом Ю.
эфиры (рис. 13.3, в) обладают необычным свойством образовывать устойчивые комплексы с катионами щелочных металлов.
И хелатообразующие, и макроциклические лиганды важны тем, что их комплексные соединения обладают высокой устойчивостью в водных растворах.
Еще большую устойчивость нередко проявляют макроциклические лиганды, имеющие в свободном виде структуру «корзины» или «клетки». Эти макроциклы называются криптандами. Их комплексы с катионами — криптаты (рис. 13.4) — относятся к типу «гость —хозяин». «Хозяин» —.
![Структура криптата [2.2.2] калия.](/img/s/8/11/1434711_4.png)
Рис. 13.4. Структура криптата [2.2.2] калия:
в плоскости рисунка расположены два донорных атома азота и катион калия, находящийся в нише криптата; над плоскостью — шесть хелатных циклов с четырьмя донорными атомами кислорода, отмеченными цифрами 1,2,3,4; под плоскостью — три хелатных цикла с двумя донорными атомами кислорода, отмеченными цифрами 5 и 6.
это криптанд, «гость» — катион, входящий в полость криптанда и покидающий ее. Такие координационные системы обладают специфической избирательностью, но отношению к катионам того же размера, что и полость лиганда-хозяина. Избирательность проявляется в особой прочности комплекса с данным катионом, а сам акт образования комплекса может служить механизмом распознавания катиона биохимической системой.