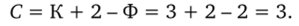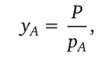При абсорбции распределяемое вещество, например, углекислый газ распределяется между двумя фазами. Таким образом, имеет место взаимодействие двух фаз (Ф = 2) и трех компонентов (К = 3).
Согласно правилу фаз такая система имеет три степени свободы: 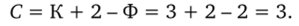
Основными параметрами, определяющими фазовое равновесие при абсорбции, являются давление р, температура t и концентрация.
При постоянных давлениях и температурах, что имеет место при абсорбции, каждой концентрации распределяемого вещества в одной фазе соответствует определенная концентрация в другой.
В условиях равновесия при постоянной температуре и общем давлении зависимость между равновесными концентрациями в фазах выражает закон Генри:
где р‘ — парциальное давление вещества А в газовой фазе, равновесной с жидкой; хА — мольная доля (концентрация) вещества А в жидкой фазе; Е — константа Генри.
Или.
Константа Генри зависит от природы абсорбтива и абсорбента, а также от температуры:
где q — теплота растворения газа; R — универсальная газовая постоянная; С — постоянная, зависящая от природы газа и жидкости.
Таким образом, из (8.3) следует, что при увеличении температуры растворимость газов в жидкостях снижается.
Парциальное давление вещества А в газовой фазе может быть заменено его концентрацией^ в соответствии с законом Дальтона:
или.
где Р — общее давление в системе.
Приравняв (8.4) и (8.1), получим:
где Е/Р — т — коэффициент распределения или константа физического равновесия.
Как следует из уравнения (8.5), зависимости между равновесными концентрациями в газовой (У) и жидкой (X) фазах представляет прямую линию, проходящую через начало координат, тангенс угла наклона которой равен коэффициенту т.
Закону Генри подчиняются разбавленные растворы, приближающиеся к идеальным. Для концентрированных растворов равновесные зависимости отклоняются от прямолинейных и определяются экспериментально.