Методы групповых составляющих

Молекулярный коэффициент активности разделяется на две части. Одна часть характеризует вклад, обусловленный различиями в размере молекул, а другая отражает вклад, обусловленный молекулярными взаимодействиями. В методе АСОГ первая часть определяется при использовании произвольно выбранного уравнения Флори — Хаггинса для атермических систем. Вторая часть определяется по уравнению Вильсона… Читать ещё >
Методы групповых составляющих (реферат, курсовая, диплом, контрольная)
При разработке корреляций термодинамических свойств часто бывает удобно рассматривать молекулу как агрегат функциональных групп; тогда некоторые термодинамические свойства чистых газов и жидкостей (например, теплоемкость или критический объем) могут быть рассчитаны путем суммирования групповых составляющих. Лэнгмюр очень давно предложил распространить эту концепцию на смеси. Было сделано несколько попыток создать методы расчета теплот смешения и коэффициентов активности по групповым составляющим. Рассмотрим только два метода (оба расчета для коэффициентов активности), которые дают приемлемые результаты даже для сильно неидеальных смесей, причем, когда данных почти или вовсе нет. Эти методы, носящие название АСОГ и ЮНИФАК[1], в принципе похожи, но разнятся в деталях.
В основе любого метода расчета по групповым составляющим лежит идея, заключающаяся в том, что, хотя химическая технология имеет дело с тысячами химических соединений, тем не менее число функциональных групп, из которых состоят эти соединения, значительно меньше. Поэтому если предположить, что физическое свойство газа или жидкости есть сумма вкладов функциональных групп молекулы, можно получить метод корреляции свойств большого количества газов и жидкостей через значительно меньшее число параметров, характеризующих вклады отдельных групп.
Любой метод групповых составляющих обязательно является приближенным, поскольку вклад данной группы в одной молекуле совсем необязательно будет таким же в другой молекуле. Основой методов групповых составляющих является предположение об аддитивности: вклад одной группы в молекуле предполагается независимым от любого из вкладов других групп молекул. Данное положение справедливо только в том случае, если на роль любой группы в молекуле не влияет природа других групп этой молекулы.
Например, мы не ожидаем, что вклад карбонильной группы в кетоне (допустим в ацетоне) будет таким же, как и вклад карбонильной группы в органической кислоте (например, в уксусной). С другой стороны, опыт показывает, что вклад карбонильной группы, например, в ацетоне близок (если не идентичен) вкладу карбонильной группы в другом кетоне (допустим в бутаноне-2).
Точность корреляции повышается с конкретизацией различий групп. Например, при рассмотрении алифатических спиртов в первом приближении не делается различия между гидроксильными группами, находящимися в различных позициях (первичных или вторичных), однако для второго приближения установить эти различия желательно. В пределе, делая все больше и больше таких различий, мы открываем лучшую «группу» — саму молекулу. В этом случае теряются преимущества метода групповых составляющих. Для пользы дела должен быть достигнут компромисс. Число различных групп должно оставаться небольшим, однако достаточным, чтобы учитывать существенное влияние молекулярной структуры на физические свойства.
Распространение концепции групповых составляющих на смеси чрезвычайно заманчиво, поскольку число чистых газов и жидкостей, используемых в химической промышленности, уже очень велико, а число различных смесей больше на несколько порядков. Тысячи, возможно миллионы жидких смесей, представляющих интерес для химической промышленности, могут быть составлены вероятно из 20, 50 или максимум из 100 функциональных групп.
Метод АСОГ.
Введение
в метод расчета коэффициентов активности по групповым составляющим АСОГ дан в работе Д. Палмера (Chem.Eng., 1975, р. 80).
Коэффициент активности /-го компонента в смеси у, складывается из конфигурационной (энтропийной) составляющей, обусловленной различиями в размере молекул, и составляющей, характеризующей групповое взаимодействие, которая обусловлена различиями в силах межмолекулярного взаимодействия: 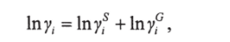
где индекс S обозначает размер, а индекс G — группу.
Коэффициент активности yf зависит только от числа размерных групп (например СНг, СО, ОН) в различных молекулах, из которых состоит смесь. По теории Флори-Хаггинса для атермических смесей молекул неодинаковых размеров: где.
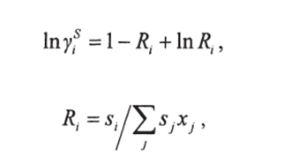
где Xj — мольная доля компонента у в смеси; - число размерных групп в молекуле у.
Параметр sj не зависит от температуры. Суммирование осуществляется по всем компонентам, включая компонент /.
Для расчета у? необходимо знать все групповые мольные доли Хк (индекс к относится к определенной группе в молекуле у):
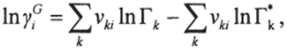
к к.
где Гк — коэффициент активности группы к в смеси; Г/ - коэффициент.
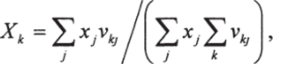
где vkJ — число взаимодействующих групп к в молекуле у.
Коэффициент активности yf определяется выражением активности группы к в стандартном состоянии. Это стандартное состояние зависит от молекулы /.
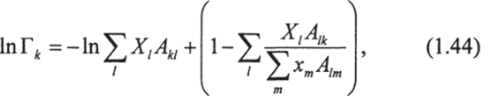
Коэффициент активности Г* дается уравнением Вильсона:
где суммирование распространяется на все группы, присутствующие в смеси.
Уравнение (1.44) используется также для определения Г**.
компонента /, однако в таком случае оно применяется для «смеси» групп, из которых состоит чистый компонент /. Например, если |-й компонент — вода, гексан1 или бензол, то имеется только один вид групп и In Г* равен нулю. Однако, Здесь предполагается, что в отношении групповых взаимодействий не делается различий между группами СН2 и СН3.
если /-й компонент — метанол, то In Г* имеет конечное значение как для гидроксильной, так и для метальной группы.
Параметры А и и A/к (А к/ * А/*) — это параметры групповых взаимодействий, которые зависят от температуры. Их значения получаются в результате обработки данных по равновесию пар — жидкость. Важным моментом является то, что при фиксированной температуре эти параметры зависят только от природы групп и, предположительно, не зависят от природы молекулы. Поэтому групповые параметры, полученные из имеющихся экспериментальных данных для одних смесей, могут быть использованы для расчета коэффициентов активности в других смесях, которые не содержат тех же молекул, но содержат те же самые группы.
Предположим, например, что мы хотим рассчитать коэффициенты активности в бинарной системе дибутилкетон — нитробензол. Для того чтобы это сделать, необходимо знать параметры групповых взаимодействий для метальных, фенильных, кетои нитрильных групп. Эти параметры могут быть получены по данным для других бинарных смесей, которые содержат такие группы, например ацетон — бензол, нитропропан — толуол и метилэтилкетон — нитроэтан.
Метод ЮНИФАК. Основная идея модели «раствора групп» заключается в использовании существующих данных по фазовому равновесию для расчёта фазового равновесия систем, по которым нет экспериментальных данных. В основной концепции метод ЮНИФАК следует методу АСОГ, в котором коэффициенты активности в смесях связаны со взаимодействиями между структурными группами. Для реализации этой концепции необходимо:
- 1. Произвести обработку экспериментально определенных значений коэффициентов активности для получения параметров, характеризующих взаимодействия между парами структурных групп в неэлектролитических системах.
- 2. Использовать эти параметры для расчета коэффициентов активности в других системах, которые экспериментально не исследовались, но содержат те же самые функциональные группы.
Молекулярный коэффициент активности разделяется на две части. Одна часть характеризует вклад, обусловленный различиями в размере молекул, а другая отражает вклад, обусловленный молекулярными взаимодействиями. В методе АСОГ первая часть определяется при использовании произвольно выбранного уравнения Флори — Хаггинса для атермических систем. Вторая часть определяется по уравнению Вильсона в приложении к функциональным группам. Подход становится значительно более строгим при соединении концепции «раствора групп» с уравнением ЮНИКВАК (табл. 1.3). Во-первых, модель ЮНИКВАК уже содержит комбинаторную часть, отражающую энергетические взаимодействия. Во-вторых, размеры функциональных групп и площади поверхностей взаимодействия рассчитываются по данным о молекулярной структуре чистых компонентов, которые определяются независимо.
Уравнение ЮНИКВАК хорошо представляет равновесие как пар — жидкость, так и жидкость — жидкость в многокомпонентных системах, содержащих разнообразные неэлектролиты, например, углеводороды, кетоны, сложные эфиры, воду, амины, спирты, нитрилы и т. д. Применительно к многокомпонентной смеси уравнение ЮНИКВАК для коэффициента активности (молекулярного) компонента / имеет вид:
где.
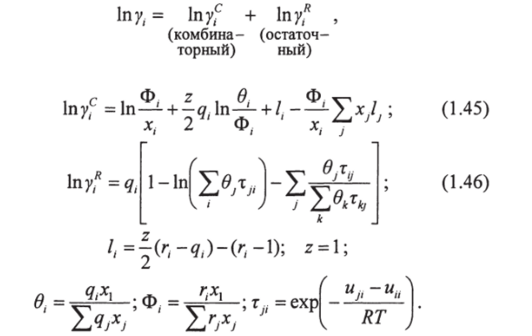
В этих уравнениях х, — мольная доля компонента /. В уравнениях (1.45) и (1.46) суммирование идет по всем компонентам, включая компонент /. Величина в, — доля площади, а Ф, — сегментная доля, которая похожа на объемную долю.
Номер группы. | Номер подгруппы. | Группа или подгруппа. | Наименование. | Rk | Qk | Примеры разбивки на группы. |
сн2 | Алканная группа. | |||||
1А. | СНз. | Конечная группа углеводородной цепи. | 0,9011. | 0,848. | Этан: 2СН3 | |
1 В. | сн2 | Средняя группа углеводородной цепи. | 0,6744. | 0,540. | н-Бутан: 2СН3, 2СН2 | |
1C. | сн. | Средняя группа углеводородной цепи. | 0,4469. | 0,228. | Изобутан: ЗСН3, 1СН. | |
с=с. | Олефиновая группа (только а-олефин). | 1,3454. | 1,176. | а-Бутен: 1С=С, 1СН2, 1СН3 | ||
АСН. | Ароматическая углеводородная группа. | 0,5313. | 0,400. | Бензол: 6АСН. | ||
ассн2 | Ароматическая углерод-алканная группа. | |||||
4А. | ассн2 | Общий случай. | 1,0396. | 0,660. | Этилбензол: 5АСН, 1АССН2, 1СН3 | |
4 В. | АССНз. | Толуольная группа. | 1,2663. | 0,968. | Толуол: 5АСН, 1АССН3 | |
СОН. | Спиртовая группа, включает ближайшую. | |||||
СН2 | ||||||
5А. | сон. | Общий случай. | 1,2044. | 1,124. | Этанол: 1СН3, 1СОН. | |
5 В. | мсон. | Метанол. | 1,4311. | 1,432. | Метанол: 1МСОН. | |
5С. | снон. | Вторичный спирт. | 0,9769. | 0,812. | Изопропанол: 2СН3, 1СНОН. | |
Н20. | Вода. | 0,9200. | 1,400. | Вода: 1Н20. | ||
АСОН. | Ароматическая углерод-спиртовая груп; | 0,8952. | 0,680. | Фенол: 5АСН, 1АСОН. | ||
со. | Карбонильная группа. | 0,7713. | 0,640. | Ацетон: 2СН3, ICO. | ||
сно. | Альдегидная группа. | 0,9980. | 0,948. | Пропионовый альдегид: 1СН3, 1СН2, 1СНО. |
п. | 1 з. | ||
соо. | Эфирная группа (сложные эфиры). | ||
о. | Эфирная группа (простые эфиры). | ||
cnh2 | Первичная аминная группа, включает ближайшую СН2 | ||
12А. | cnh2 | Общий случай. | |
12 В. | MCNHj. | Метиламин. | |
NH. | Вторичная аминная группа. | ||
acnh2 | Ароматическая углерод-аминная группа. | ||
CCN. | Нитрильная группа, включает ближайшую СН2 | ||
15А. | MCCN. | Ацетонитрил. | |
15 В. | CCN. | Общий случай. | |
Cl. | Хлоридная группа. | ||
16А. | Cl-1. | С1 в соединении с последним атомом углерода. | |
16 В. | Cl-2. | CI в соединении со средним атомом углерода. | |
CHC12 | Дихлоридная группа, только конечная. | ||
ACC1. | Ароматическая углерод-хлоридная группа. |
1 5. | 1 6. | 1 1 |
1,0020. | 0,880. | Метилацетат: 2СН3, 1СОО. |
0,2439. | 0,240. | Диэтиловый эфир: 2СН3, 2СН2, 10. |
1,3692. | 1,236. | н-Пропиламин: 1СН3, 1СН2, 1CN. |
1,5959. | 1,544. | Метиламин: 1MCNH3 |
0,5326. | 0,396. | Диэтиламин: 2СН3, 2СН2, 1NH. |
1,0600. | 0,816. | Анилин: 5АСН, 1ACNH2 |
1,8701. | 1,724. | Ацетонитрил: 1MCCN. |
1,6434. | 1,416. | Пропионитрил: 1CCN, 1СН3 |
0,7660. | 0,720. | 1,2-Дихлорэтан: 2СН2, 2CI-1. |
0,8069. | 0,728. | 1,2,3-Трихлорпропан: 2СН2, 1СН, 2С1−1, 1С1−2. |
2,0672. | 1,684. | 1,1-Дихлорэтан: 1СН3, 1СНС12 |
1,1562. | 0,844 Хлорбензол: 5АСН, 1АСС1. | |
Параметры чистых компонентов Г/ и q, характеризуют, соответственно, молекулярные вандерваальсовские объемы и площади поверхности молекул.
В модели ЮНИКВАК два настраиваемых бинарных параметра Ту и Xji, входящих в уравнение (1.46), должны рассчитываться по экспериментальным данным фазового равновесия. Для систем, содержащих три и более компонентов, не требуется параметров, характеризующих тройные или более множественные взаимодействия.
В методе ЮНИФАК непосредственно используется комбинаторная часть коэффициентов активности ЮНИКВАК — уравнение (1.45). Это уравнение включает только свойства чистых компонентов. Параметры г, и q, определяются суммированием групповых параметров объема и площади (/?* и Qk), приводимых в табл. 1.13. 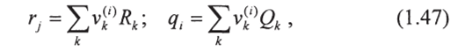
где v*(,) всегда является целым числом и определяет число групп типа к в молекуле Групповые параметры Rk и Qk рассчитываются по значениям вандерваальсовского группового объема V и по значениям площадей поверхности 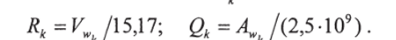 AVi, приводимых А. Бонди:
AVi, приводимых А. Бонди:
Коэффициенты нормализации 15,17 и 2,5−109 определены по значениям объема и площади внешней поверхности единичного СНг в полиэтилене.
Остаточная (энергетическая) часть коэффициента активности (1.46) заменяется на выражение, полученное при использовании концепции «растворов групп»:
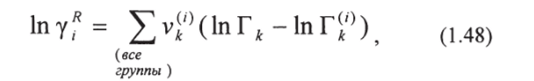
где Г* - остаточный коэффициент активности группы; Г*(,) — остаточный коэффициент активности группы к в некотором служащем для сравнения растворе, который содержит молекулы только типа i (Г*1* в методе ЮНИФАК похож на Г* в методе АСОГ).
В уравнении (1.48) член 1пГ*(,) необходим для достижения нормализации, т. е. все коэффициенты активности у, становятся равными 1 при х,—>1. Коэффициент активности группы к зависит от молекулы /, в которой к находится. Например, Гдля группы СОН (сокращенное обозначение для СНгОН) в этаноле относится к «раствору», содержащему 50 групповых процентов СОН и 50 групповых процентов СНз при температуре смеси, в то время, как Г*(,) для группы СОН в бутаноле относится к раствору, содержащему 25 групповых процентов СОН, 50 групповых процентов СНг и 25 групповых процентов СН3.
Коэффициент активности Г * определяется по выражению, сходному с уравнением (1.46):
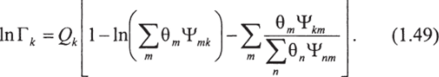
Уравнение (1.49) применимо и к Г*(,). 0т — поверхностная доля группы т, а суммы включают все различные группы. Величина 0″ рассчитывается подобно 9:
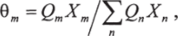
где Хт — мольная доля группы т в смеси.
Параметр группового взаимодействия Тт" определяется выражением:
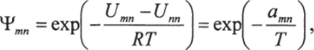
где Um" — мера энергии взаимодействия групп тип.
Параметры группового взаимодействия атп должны рассчитываться по экспериментальным данным о фазовом равновесии. Следует отметить, что ат" измеряется в кельвинах и атп * ат. Параметры атп и ат рассчитываются при использовании базы данных, содержащей экспериментальные результаты в широких диапазонах параметров состояния и составов. Некоторые значения параметров группового взаимодействия атп представлены в табл. 1.14.
Таблица 1.14. Параметры группового взаимодействия ат" | К | |||||||||
1 сн2 | C=C. | | АСН. | I acch2 | 1 сон. | Н20. | | АСОН. | 1 со. | | СНО. | | № п/п. | |
СН2 | — 200,0. | 32,08. | 26,78. | 931,2. | 685,9. | |||||
С=С. | 2520,0. | 651,6. | 943,3. | 578,3. | X. | X. | ||||
АСН. | 15,26. | — 144,3. | 167,0. | 705,9. | 860,7. | 651,1. | X. | |||
ассн2 | — 15,84. | — 309,2. | — 146,8. | 856,2. | 740,0. | X. | ||||
СОН. | 169,7. | 254,2. | 83,5. | 92,61. | — 320,8. | X. | 462,3. | 480,0. | ||
н2о. | 657,7. | 485,4. | 361,5. | 385,0. | 287,5. | 462,6. | 470,8. | 234,5. | ||
АСОН. | X. | X. | — 558,2. | X. | X. | |||||
СО. | 101,8. | 75,00. | — 106,5. | — 532,6. | X. | — 49,24. | ||||
СНО. | 343,2. | X. | X. | X. | — 226,4. | X. | 39,47. | |||
СОО. | 348,0. | X. | 325,5. | 167,5. | X. | — 266,5. | 333,6. | X. | ||
О. | X. | — 75,50. | — 13,44. | X. | X. | — 39,81. | X. | |||
cnh2 | — 16,74. | 90,37. | — 38,64. | X. | — 109,8. | — 527,7. | X. | X. | X. | |
NH. | 8,922. | 37,94. | X. | — 700,0. | — 882,7. | X. | X. | X. | ||
acnh2 | X. | X. | 236,6. | X. | X. | X. | ||||
CCN. | 27,31. | 43,03. | — 66,44. | — 150,0. | 337,9. | 227,0. | X. | 447,7. | X. | |
Cl. | — 119,6. | 242,1. | — 90,43. | 52,69. | 357,0. | 618,2. | X. | 62,00. | X. | |
CHC12 | 31,06. | — 72,88. | X. | X. | X. | 467,0. | X. | 37,63. | X. | |
ACC1. | 121,1. | X. | X. | 586,3. | X. | X. | X. | |||
О о. о. | I cnh2 | NH. | I acnh2 | I CCN. | 1 Cl. | | CHC12 | I ACC1. | | № n/n. | ||
сн2 | 687,5. | 472,6. | 422,1. | 800,0. | 601,6. | 523,2. | 60,45. | 194,2. | ||
с=с. | X. | X. | 349,9. | 515,2. | X. | 691,3. | 253,8. | 259,5. | X. | |
АСН. | 159,1. | 37,24. | 179,7. | 487,2. | 680,0. | 290,1. | 124,0. | X. | — 99,9. | |
ассн2 | 110,0. | 680,0. | X. | X. | 640,0. | 33,84. | X. | X. | ||
сон. | 174,3. | — 204,6. | — 166,8. | X. | 79,85. | 194,6. | X. | 69,97. | ||
н2о. | X. | X. | 385,3. | 743,8. | — 314,6. | 118,5. | 158,4. | 247,2. | 190,6. | |
АСОН. | — 482,2. | X. | X. | X. | X. | X. | X. | X. | X. | |
СО. | — 180,1. | 475,5. | X. | X. | X. | — 307,4. | 628,0. | 874,5. | X. | |
сно. | X. | X. | X. | X. | X. | X. | X. | X. | X. | |
соо. | — 26,15. | X. | X. | X. | X. | X. | X. | X. | ||
О. | — 290,0. | X. | X. | X. | X. | X. | X. | X. | ||
cnh2 | X. | X. | X. | X. | X. | X. | X. | — 10,0. | ||
NH. | X. | X. | X. | X. | X. | X. | X. | — 60,0. | ||
acnh2 | X. | X. | X. | X. | X. | X. | X. | |||
CCN. | X. | X. | X. | X. | X. | — 100,0. | X. | 25,0. | ||
Cl. | X. | X. | X. | X. | X. | 100,0. | — 308,5. | X. | ||
CHC12 | X. | X. | X. | X. | X. | X. | 790,0. | X. | ||
ACC1. | X. | X. | 110,0. | X. | X. |
Примечание: Знак «к» означает недостаточность или отсутствие данных
Комбинаторная составляющая коэффициента активности у. (1.45) зависит только от размера и формы присутствующих молекул. С увеличением координационного числа z для.
д
больших цепных молекул отношение — -> 1, и в таких пре;
г
дельных случаях уравнение (1.45) переходит в уравнение Флори-Хаггинса, используемое в методе АСОГ.
Остаточная составляющая коэффициента активности у? (1.48) и (1.49) зависит от размеров площадей групп и от характера групповых взаимодействий. Если все группы одинаковы, то уравнения (1.48) и (1.49) становятся похожими на уравнения, используемые в методе АСОГ.
Функциональные группы, упоминавшиеся в этом разделе, даны в табл. 1.13. Поскольку каждая из перечисленных в таблице групп имеет свои собственные значения R и Q, то предполагается, что подгруппы, входящие в состав основных групп, т. е. например 1А, 1 В и 1C, имеют одинаковые энергетические параметры взаимодействия. Далее приводятся два примера, которые иллюстрируют, во-первых, состав и применение табл. 1.13 и, во-вторых, использование метода ЮНИФАК для расчёта коэффициентов активности.
Пример 5. Рассмотрим эквимольную бинарную смесь бензола (1) с н-пропанолом (2). У бензола шесть групп АСН (группа 3). Поэтому V30 = 6; Лз=0,5313; (9з=0,400;
г =из‘) • Л3= 3,1878; =и1) • (93 = 2,400. У н-пропанола одна группа СНз (1А), одна группа СНг (1 В) и одна группа СОН (5А). ПОЭТОМУ V|A = 1, vm = 1, Vsa = 1; /?1А = 0,9011,.
Я, в = 0,6744; /г5А = 1,2044; гг = (1)(0,9011) + (1)(0,6744) +.
+ (1)(1,2044) = 2,7799; подобно и q2 = (1)(0,848) + (1)(0,540) + + (1)(1,124) = 2,512. Необходимые параметры групповых взаимодействий из табл. 1.14:
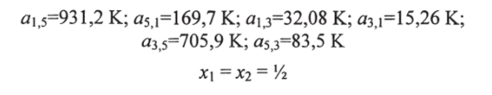
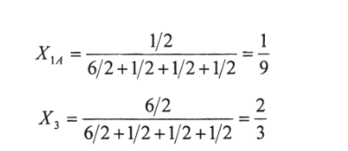
Подобно этому 
При постоянной температуре коэффициенты активности группы к (к = 1 А, 1 В, 3 или 5А) являются функцией группового состава: 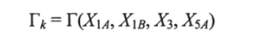
Для эквимолярной смеси 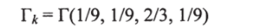 В чистом бензоле (1)
В чистом бензоле (1) 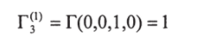
В чистом н-пропаноле:
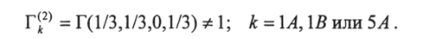
Пример 6. Рассчитать коэффициенты активности для системы ацетон (1) — н-пентан (2) при 307 К и х = 0,047.


Для чистого ацетона:


Используя ту же процедуру расчета для пентана, находим, что у2=1,02.
Соответствующие экспериментальные значения по Т. Ло и др. равны 4, 41 и 1, 11.
- [1] АСОГ = ASOG (Analytical Solution of Groups — аналитический растворгрупп), ЮНИФАК = UNIFAC.