Экстракция.
Органическая химия

Пятых экспериментальных условиях. К этим условиям нередко относятся не только временные и механические факторы, но и реальные растворители. Растворитель S| содержит растворенный в нем S2, и наоборот. При этом реально взаимное их содержание далеко от насыщения, так как обычно выбираемые растворители (вода, спирты, водно-спиртовые смеси, солевые, кислые или щелочные растворы) и S2 (простые… Читать ещё >
Экстракция. Органическая химия (реферат, курсовая, диплом, контрольная)
Под экстракцией понимается извлечение соединений из жидкой или твердой фазы в жидкую фазу растворителя, называемого экстраг ентом.
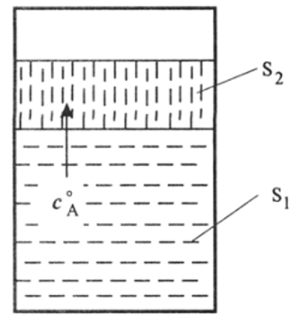
Рис. 3.1. Экстрактор.
В ходе экстракции юггенсивно перемешиваются две несмсшивающисся жидкости S| и S2, одна из которых содержит соединение А, которое подлежит извлечению и отделению от других веществ, также находящихся в фазе S| (рис. 3.1). Экстрагент S2 может быть или легче или тяжелее рабочего раствора, из которого ведется экстракция. В качестве экстрагента выбирается жидкость S2, растворяющая нужное соединение лучше, чем S|. Чем больше будет разница в сольватации экстрагируемого вещества (А) двумя жидкостями, т. е. = Д6^(S,) — (S,), тем боль;
ше эффект экстракции.
Скорость извлечения зависит от скорости пе;
V|.
ресольватащш молекул A (S,)" ?" ~~ A (S2)".
V2.
на 1ранице раздела фаз между двумя жидкостями, а также от фазовой поверхности, разделяющей жидкости S| и S2. Величина фазовой поверхности контролируется формой сосуда (делительной воронки, экстрактора и т. д.), скоростью перемешивания, которое обычно производится путем встряхивания, природой и соотношением объемов жидкостей. В благоприятных условиях экстракции более или менее быстро наступает равновесие между двумя фазами, которое описывается консташчж распределения:

Равновесная концентрация вещества, А в рабочем растворе [сА ]S ( после первой экстракции в состоянии равновесия.

характеризует остаточную концентрацию вещества. Если она мала, то можно ограничиться одной экстракцией. При cj = 0,1 моль/л и /Гр|Спр * 100 потери вещества, А составят 1%, что обычно допустимо, если вещество, А не представляет экологической угрозы и стоимость его не слишком велика.
В реальных условиях распределение вещества между двумя жидкими фазами редко достигает состояния равновесия, поэтому используются эмпирические коэф;
cA(S2).
фициенты распределения, а =-— вещества между двумя растворителями в при;
са (?).
пятых экспериментальных условиях. К этим условиям нередко относятся не только временные и механические факторы, но и реальные растворители. Растворитель S| содержит растворенный в нем S2, и наоборот. При этом реально взаимное их содержание далеко от насыщения, так как обычно выбираемые растворители (вода, спирты, водно-спиртовые смеси, солевые, кислые или щелочные растворы) и S2 (простые и сложные эфиры, углеводороды и их галогенопроизводные) трудно растворимы друг в друге.
Экстракция вещества растворителем из твердой фазы сложной смеси определяется химическим сродством растворителя к целевому продукту, концентрацией этого продукта в твердой фазе и условиями его внутренней диффузии. Этот вид экстракции часто используется в органической химии для извлечения природных соединений из биологических объектов (хлорофилла и каротиноидов из зеленого листа, кофеина из кофейной или чайной массы, алкалоидов из растительного сырья и др.). В ряде случаев растворяют путем экстракции не целевой продукт, а содержащиеся в нем примеси. С этой целью берут экстрагент, который растворяет только примеси. Операции проводят либо в колбах, либо в специальных приборах для экстракции (экстрактор Сокслета и др.). Теория экстракции из твердой фазы базируется на явлениях растворимости, межмолекулярной ассоциации, диффузии и в общем виде недостаточно разработана.