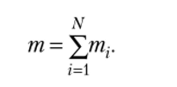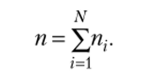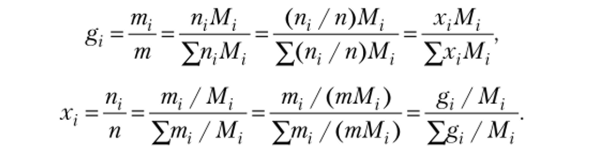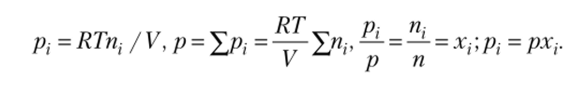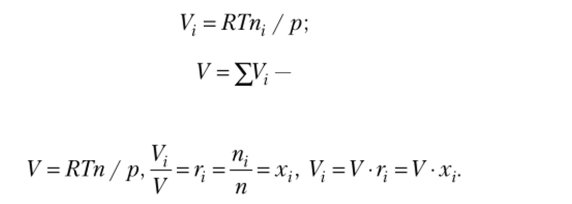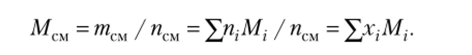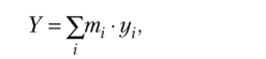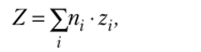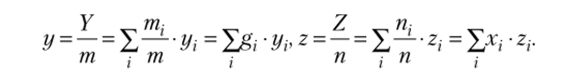Чистое вещество — вещество, состоящее из частиц одного сорта (атомов или молекул) независимо от агрегатного состояния. Примерами чистого вещества являются вода и водяной пар, находящиеся в равновесии.
Раствор — смесь, состоящая из нескольких чистых веществ. Под раствором понимают обычно гомогенную (однородную) фазу. Растворы бывают жидкие, твердые и газообразные. Состав раствора характеризуется массовыми или мольными долями компонентов.
Если раствор содержит тл кг вещества 1, т2 кг вещества 2, …, mN кг вещества N, то масса раствора, очевидно, равна сумме.
Массовая доля определяется отношением gi=mi / т, очевидно, что.
N
?g,-=l. Таким образом, чтобы определить состав раствора, достаточно /=1.
задать массовые доли (N- 1) компонента. В частности, для бинарной смеси Аналогично для смеси, состоящей из п{ молей вещества 1, п2 молей вещества 2, …, nN молей вещества N, количество (число молей) раствора равна сумме.
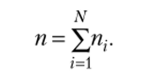
N.
Мольная доля i-ro компонента раствора х{ — пх /п, =1. Для бинар;
1=1.
ной смеси х2 = l-xt. Нетрудно показать, что массовые и мольные доли взаимосвязаны:
Смеси идеальных газов. Закон Дальтона.
Модель идеального газа часто применяется в науке и технике в силу своей простоты и универсальности. Не менее часто используется модель идеальной смеси идеальных газов. Основным законом, определяющим поведение идеально-газовой смеси, является закон Дальтона: каждый газ ведет себя в газовой смеси так, как будто он один занимает весь объем смеси при температуре смеси. Иными словами, каждый газ (компонент смеси) имеет такое давление, какое он имел бы, если бы он один занимал весь объем. Это давление называется парциальным и обозначается р:
Иногда в расчетах используется объемная доля rl-Vi /V:
закон Амага; 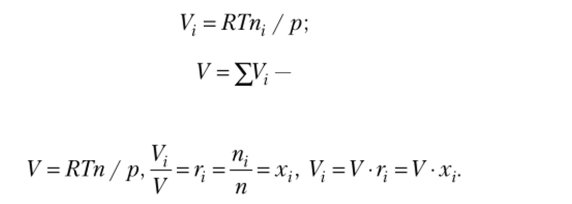
Для идеального газа мольная доля равна объемной доле rt = хг Кажущаяся молярная масса смеси определяется соотношением.
Аналогично определяются и другие удельные и мольные свойства смеси:
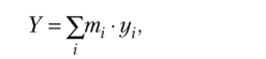
yt — удельное свойство (щ, hr $,);
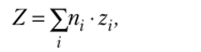
Zj — мольное свойство;