ТЯЖЕЛЫЕ ПЕРЕХОДНЫЕ МЕТАЛЛЫ (Переходные элементы второго и третьего рядов)

Из 20 тяжелых переходных металлов три — золото, серебро и ртуть — относятся к числу семи металлов древности. Золото было, по-видимому, первым металлом, с которым познакомились люди. Это произошло еще в эпоху неолита — в IV или даже V тысячелетии до н. э. Хотя эти три металла относятся к числу редких, они оказались раньше многих других доступными для человека, так как встречаются в природе… Читать ещё >
ТЯЖЕЛЫЕ ПЕРЕХОДНЫЕ МЕТАЛЛЫ (Переходные элементы второго и третьего рядов) (реферат, курсовая, диплом, контрольная)
В этой главе мы познакомимся с тяжелыми переходными металлами -^-элементами второго и третьего рядов. Эти элементы имеют много общего с переходными элементами первого ряда: все они — металлы, все склонны к образованию комплексных соединений. В то же время тяжелые переходные металлы во многих отношениях заметно отличаются от легких: сами металлы более тугоплавки, в соединениях они проявляют более высокие состояния окисления, причем высшая степень окисления достигает восьми, кроме того, для них менее характерны катионные аквакомплексы в водных растворах, в том числе практически отсутствуют ионы М2+ (водн), зато широко распространены полиядерные формы, относительно редкие для переходных элементов первого ряда. Существенно отличаясь от 3d-элементов, второй и третий ряды очень близки между собой, поэтому их удобно рассматривать совместно.
СОДЕРЖАНИЕ В ПРИРОДЕ
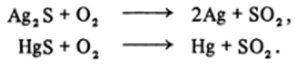
Из 20 тяжелых переходных металлов три — золото, серебро и ртуть — относятся к числу семи металлов древности. Золото было, по-видимому, первым металлом, с которым познакомились люди. Это произошло еще в эпоху неолита — в IV или даже V тысячелетии до н. э. Хотя эти три металла относятся к числу редких, они оказались раньше многих других доступными для человека, так как встречаются в природе в самородном виде. Для химически очень устойчивого золота именно простое вещество — металл — представляет основную форму существования в природе, менее инертные серебро и ртуть входят в основном в состав сульфидных руд, например, аргенита AgS (серебряный блеск) или киновари HgS, из которых они легко выплавляются в виде металлов при нагревании на воздухе:
Золото, благодаря своей химической стойкости, редкости и, конечно, внешнему виду издревле было наиболее драгоценным металлом[1] и служило меновым эквивалентом в торговле у многих народов. Стремление превратить неблагородные металлы в золото способствовало развитию алхимии. Хотя алхимики и не достигли этой цели, они сделали много полезных открытий в области химии, минералогии, медицины и, главное, подготовили становление химии как отрасли естествознания.
Серебро и золото относят к благородным металлам — наиболее химически стойким и трудноокислясмым. К благородным металлам принадлежат также платиновые металлы, к которым относятся шесть переходных элементов: триада из второго ряда — рутений, родий, палладий или легкие платиновые металлы, имеющие плотность около 12 г/см[1] (табл. 32.1), и триада из третьего ряда — осмий, иридий,.
Элемент. | Плотность, г/CM3 (20 °C). | 7roi.°C. | Реагенты, переводящие металлы в раствор |
Y. | 4,47. | Разб. НС1, разб. HNO, разб. H2S04, гор. КОН. | |
Zr. | 6,50. | 1 855. | Царская водка, конц. H2S04, гор. HF, расплавы щелочей. |
Nb. | 8,57. | HF + HNO, гор. Н2S04, расплавы щелочей. | |
Mo. | 10,22. | Царская водка, HN03, гор. конц. H2S04, гор. НС1. | |
Тс. | 11,49. | 2 200. | Царская водка, HN03, H3S04 |
Ru. | 12,4. | 2 250. | Расплавы щелочей + окислитель. |
Rh. | 12,44. | Царская водка, гор. конц. H2S04, гор. НВг, распл. KHS04, Na202 | |
Pd. | 12,02. | 1 554. | Царская водка, гор. HN03, гор. конц. H2S04 |
Ag. | 10,50. | Конц. HNO, KCN + H202, гор. конц. H2S04 | |
Cd. | 8,65. | Кислоты. | |
La. | 6,16. | Н20, кислоты. | |
Hf. | 13,31. | 2 230. | Царская водка, конц. HF. |
Та. | 16,6. | HF + HNO, расплавы щелочей. | |
W. | 19,35. | 3 420. | конц. HN03 + конц. HF. |
Re. | 21,04. | HNO, Н2 02, гор. конц. Н2 S04, гор. НС104, щелочи. | |
Os. | 22,5. | 3 027. | Гор. царская водка, гор. HNO, расплав КОН + + KNOj. |
Ir. | 22,4. | 2 447. | Расплав K2S207, расплав Na0H + Na202, расплав KOH + KNO,. |
Pt. | 21,45. | Царская водка, расплавы щелочей. | |
Au. | 19,3. | Царская водка, KCN + 02, гор. H2Se04 | |
Hg. | 13,5. | — 38,9. | Царская водка, HN03, гор. конц. Н2 S04 |
платина или тяжелые платиновые металлы с плотностью, превышающей 21 г/см3. Свое название эти металлы получили от наиболее широко применяемого из них элемента — платины, открытой ранее других.
К наиболее редким элементам, содержание которых в земной коре не превышает 10'7-10″ в % (по массе), принадлежат золото, рений и три платиновых металла — рутений, родий и иридий.
Менее редкими из платиновых металлов являются палладий, осмий и сама платина — их содержание в земной коре, так же как и содержание серебра и ртути, составляет 10'5 -10″ * %. Все платиновые металлы относятся к рассеянным элементам, обычно они не образуют собственных руд, а содержатся в виде изоморфных примесей в минералах медно-никелевых руд.
В относительно больших количествах, на уровне 10″ *-10″ 4 %. в земной коре содержатся тяжелые переходные металлы III-VI дополнительных подгрупп периодической системы: иттрий и лантан (но не лантаноиды), цирконий и гафний, ниобий и тантал, молибден и вольфрам. Они встречаются в основном в виде кислородных соединений — смешанных оксидов (например, (Fc, Mn)(Nb, Та)204 — минералы группы танталита — колумбита), солей кислородных кислот (CaW04 — шеелит), фосфатов и силикатов (например, ZrSi04 — циркон), сульфидов и полисульфидов (например, MoS5 — молибденит).
Получение тяжелых переходных металлов из руд принципиально не отличается от получения переходных металлов первого ряда. Основное различие заключается в том, что непосредственно восстановлению тех или иных соединений до металла (чаще всего водородом при повышенных температурах) предшествуют более сложная процедура обогащения руд, электрохимическое разделение металлов и химическое концентрирование целевых соединений. Особенно сложной очистка от примесей (аффинаж) оказывается в случае платиновых металлов, так как их содержание обычно много ниже, чем содержание других металлов в обрабатываемых рудах. Современная технология аффинажа опирается на детальное знание свойств комплексных соединений переходных металлов.
Один из тяжелых переходных металлов — технеций — отсутствует в природе. Его существование и свойства предсказал в 1871 г. Менделеев, описав его как экамарганец; получен же он был искусственно в результате бомбардировки ядер молибдена дейтронами — ядрами тяжелого водорода (дейтерия) — в 1937 г. итальянскими учеными К. Перрье и Э. Сегрэ. В настоящее время известен 21 изотоп технеция. Все они радиоактивны, наиболее долгоживущий среди них **Тс имеет период полураспада 2,12 • 105 лет. Этот изотоп выделяют из продуктов деления урана в килограммовых количествах.
- [1] В Египте до середины II тысячелетия до н. э. серебро ценилось дороже золота. В наши дни в связи с истощением разведанных запасов серебра его цена. догоняет" цену золота.
- [2] В Египте до середины II тысячелетия до н. э. серебро ценилось дороже золота. В наши дни в связи с истощением разведанных запасов серебра его цена. догоняет" цену золота.